Clear Sky Science · es
El diálogo neuroinflamatorio entre microglía y astrocitos aumenta la replicación viral en un modelo derivado de iPSC de la infección por VIH en el SNC
Por qué la inflamación cerebral en el VIH sigue siendo importante
Con los tratamientos modernos contra el VIH, muchas personas viven ahora vidas largas y saludables y mantienen el virus en niveles indetectables en sangre. Sin embargo, persiste un problema: un gran número de personas con VIH aún experimentan dificultades de memoria, lentitud de pensamiento o problemas de concentración, incluso con terapia eficaz. Este estudio plantea una pregunta clave para pacientes y clínicos: si el virus está mayormente controlado, ¿por qué la inflamación cerebral —y la niebla mental que a menudo la acompaña— persiste con tanta frecuencia?
Las células de soporte del cerebro bajo la lupa
En lugar de centrarse en las neuronas, las células nerviosas que transmiten señales, los investigadores pusieron la atención en dos tipos de células “de soporte” del cerebro: microglía y astrocitos. La microglía actúa como las células inmunitarias residentess del cerebro, mientras que los astrocitos ayudan a mantener un entorno sano para las neuronas. El equipo utilizó tecnología con células madre humanas para cultivar versiones de laboratorio de estas células, llamadas microglía inducida y astrocitos inducidos, a partir de células de la piel de donantes. Este enfoque les permitió imitar de cerca la biología cerebral humana sin necesidad de tejido cerebral de pacientes.
Primero confirmaron que su microglía cultivada en laboratorio se comportaba como microglía genuina: presentaba la morfología adecuada, expresaba genes característicos y poseía los receptores que el VIH usa para entrar en las células. Estas microglías podían infectarse por el VIH y permitían la replicación viral, aunque no con la misma eficiencia que las células inmunitarias derivadas de sangre conocidas como macrófagos. A diferencia de los macrófagos, la microglía mostró solo una respuesta inflamatoria débil ante la infección, produciendo pocas de las moléculas de alarma clásicas que suelen acompañar una reacción antiviral intensa.
Un aumento sorprendente del crecimiento viral
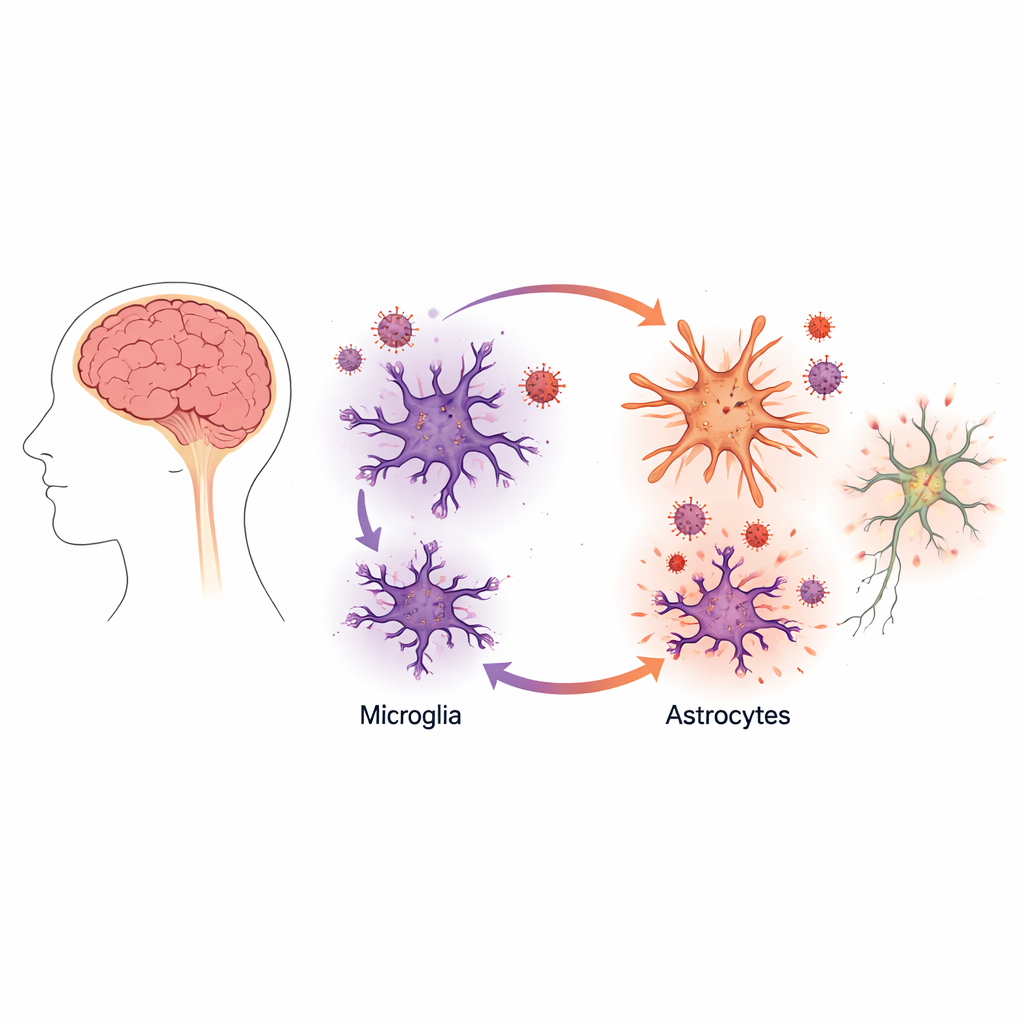
El panorama cambió de forma drástica cuando los científicos combinaron microglía con astrocitos en el mismo cultivo. En estas culturas mixtas, la producción viral por parte de la microglía se disparó aproximadamente diez veces, aunque los astrocitos en sí no se convirtieron en células productivamente infectadas. Imágenes cuidadosas y mediciones de proteínas virales mostraron que el VIH seguía replicándose principalmente en la microglía. La presencia de astrocitos, sin embargo, convirtió a esas microglías infectadas en fábricas virales mucho más activas.
Para entender por qué, el equipo examinó las señales químicas liberadas en el fluido del cultivo. Cuando los astrocitos fueron expuestos a material procedente de microglías infectadas, cambiaron hacia un estado reactivo e inflamatorio que se asemeja a los cambios observados en muchas enfermedades cerebrales. Estos astrocitos comenzaron a liberar niveles más altos de mensajeros inflamatorios, incluida una molécula llamada factor de necrosis tumoral alfa (TNFα), que desde hace tiempo se vincula con la activación del VIH.
Cómo las señales inflamatorias aumentan el volumen viral
Los investigadores preguntaron entonces si el TNFα estaba realmente ayudando a que el VIH se replicara en la microglía. Cuando añadieron TNFα purificado a microglías infectadas cultivadas solas, la producción viral aumentó de forma significativa. Bloquear el TNFα en cultivos mixtos de microglía y astrocitos con un anticuerpo redujo los niveles de virus, aunque no hasta los valores iniciales, lo que sugiere que otros factores inflamatorios también contribuyen. Experimentos adicionales apuntaron a un interruptor maestro dentro de la microglía llamado NF-kB, un complejo proteico que se desplaza al núcleo celular y activa muchos genes relacionados con la inmunidad y el estrés, incluidos los que impulsan la transcripción del VIH.
Usando una pequeña molécula que bloquea la activación de NF-kB, el equipo consiguió reducir la replicación viral aumentada en cultivos mixtos hasta el nivel observado en microglía sola. Este mismo tratamiento también disminuyó la liberación de TNFα. Las imágenes mostraron que, durante la infección, NF-kB se desplazó al núcleo con más intensidad en microglías rodeadas de astrocitos que en microglías solas, y este desplazamiento se revirtió cuando estaba presente el inhibidor de NF-kB. En conjunto, estos hallazgos describen un circuito de retroalimentación: la microglía infectada altera su entorno, los astrocitos responden liberando señales inflamatorias como TNFα, y esas señales a su vez empujan a la microglía a aumentar la producción viral a través de NF-kB.
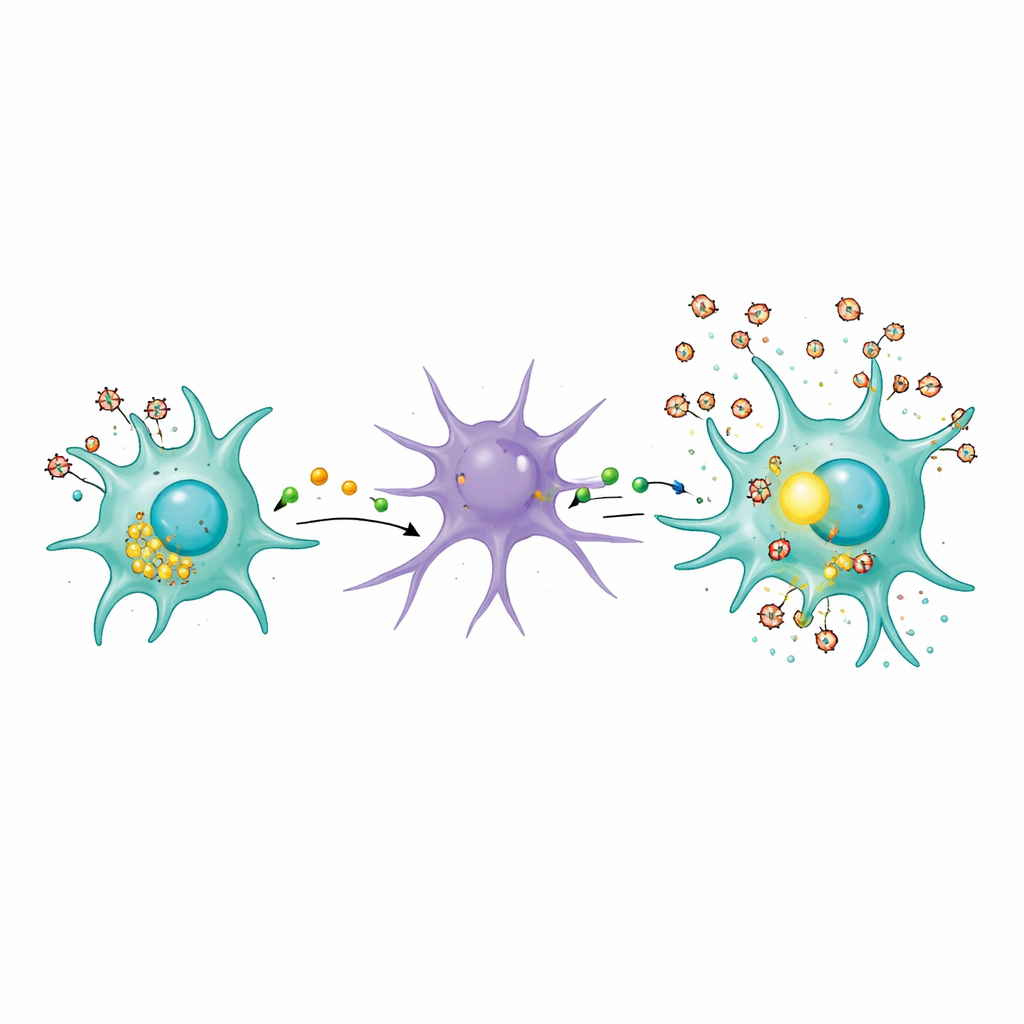
Lisosomas, basura celular y un vecindario tóxico
El estudio también investigó cómo las microglías infectadas podrían inicialmente irritar a los astrocitos. Los autores se centraron en los lisosomas, los centros de eliminación y reciclaje de desechos de la célula. En microglías infectadas, los lisosomas se desplazaron hacia la superficie celular y marcadores de su contenido, como una enzima llamada catepsina B, aparecieron en el fluido circundante. Esto sugiere que la infección por VIH induce a la microglía a volcar material parcialmente digerido en su entorno. Incluso el virus inactivado por calor —incapaz de replicarse pero que aún porta proteínas virales— fue suficiente para perturbar este tráfico lisosomal. Tal filtración puede contribuir a crear un vecindario crónicamente irritante para las células próximas, empujando a los astrocitos hacia un estado reactivo dañino que retroalimenta el ciclo inflamatorio.
Qué significa esto para las personas que viven con VIH
Para un público no especialista, el mensaje principal es que los problemas cerebrales observados en muchas personas con VIH pueden no reflejar simplemente la cantidad de virus presente, sino cómo las células de soporte del cerebro se comunican entre sí. En este trabajo, microglías infectadas y astrocitos reactivos forman un círculo vicioso: una actividad viral sutil altera el manejo de residuos de la microglía, eso inquieta a los astrocitos, los astrocitos liberan señales inflamatorias como TNFα, y esas señales empujan a la microglía a producir más virus. Incluso cuando la terapia estándar mantiene bajos los niveles virales globales, este circuito local podría sostener la inflamación y un daño cerebral lento y continuo. Los hallazgos señalan nuevas dianas terapéuticas —como dirigir TNFα, la señalización de NF-kB o la liberación anómala de lisosomas— que podrían algún día ayudar a proteger el pensamiento y la memoria en personas cuyo VIH está por lo demás bien controlado.
Cita: Gesualdi, J., Prah, J., Solomon, S. et al. Neuroinflammatory crosstalk between microglia and astrocytes increases viral replication in an iPSC-derived model of CNS HIV infection. Sci Rep 16, 13047 (2026). https://doi.org/10.1038/s41598-026-43248-7
Palabras clave: déficit neurocognitivo por VIH, microglía, astrocitos, inflamación cerebral, TNF alfa