Clear Sky Science · zh
基于线粒体凋亡基因的病理组学用于卵巢癌预后
一种读取癌症线索的新方法
卵巢癌常被称为“沉默的杀手”,因为它通常在已扩散后才被发现,这使得治疗困难且难以预测患者预后。该研究提出了一种新方法:让计算机读懂显微镜下肿瘤图像中的隐含模式,并将其与肿瘤细胞如何决定生死的机制联系起来。通过这样做,研究人员旨在比现有方法更准确地将患者分为高风险和低风险组,并发现可供新疗法针对的薄弱环节。
更深入地观察肿瘤图像
病理学家传统上通过在显微镜下观察染色的组织切片来判断癌症,并对所见内容进行描述。尽管这一方法很有力量,但也带有主观性,并且难以捕捉细微特征。该研究团队使用了卵巢肿瘤的数字“整片切片”图像,并将每张大图像切成许多小的图块。名为ResNet50的深度学习系统扫描这些图块以提取数千个数学特征,这些特征描述了细胞形状、纹理以及细胞与支持组织的排列模式。与此同时,专门的软件量化了更经典的图像特征,例如细胞核大小和组织结构,从而构建出每个肿瘤外观的丰富图谱。 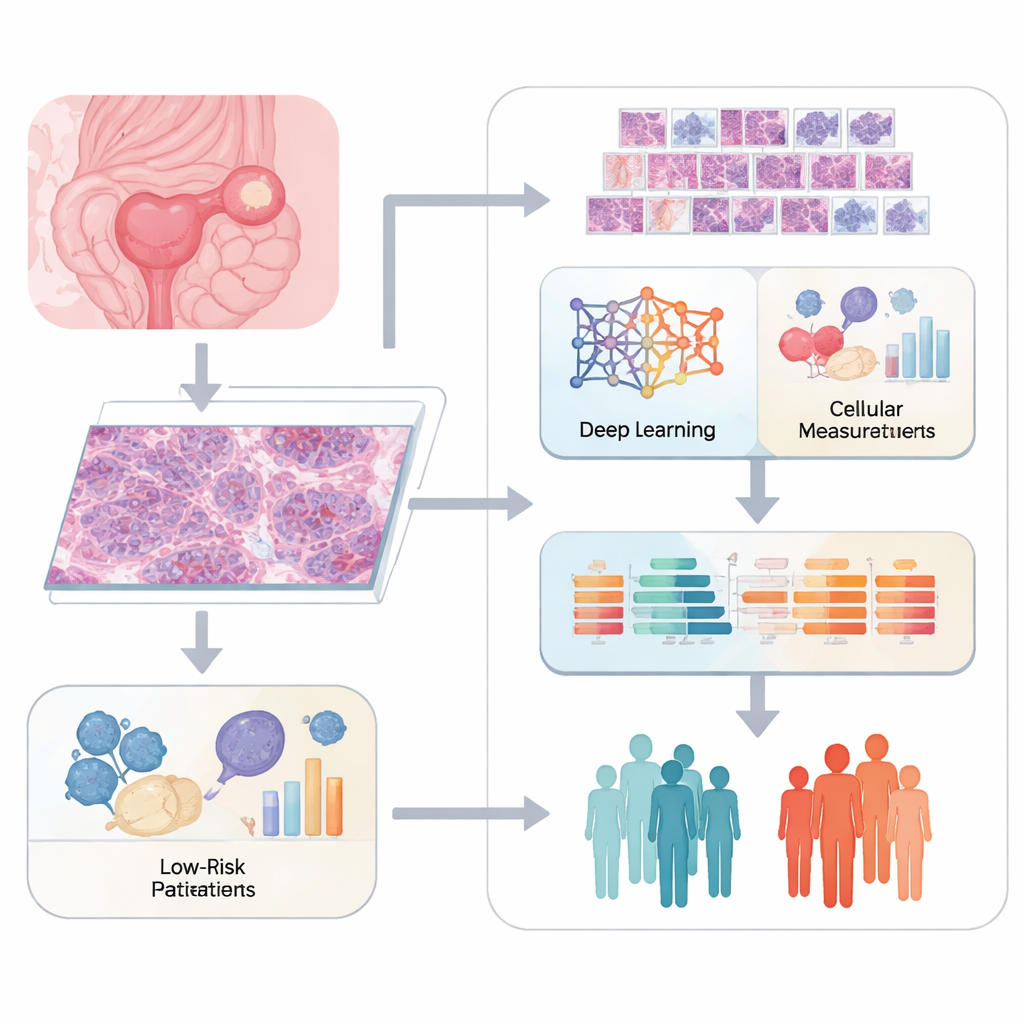
将图像与细胞死亡信号相连接
研究人员没有止步于肿瘤的外观,而是将这些图像特征与细胞内一个关键的生死开关——线粒体凋亡联系起来。该过程由一类蛋白质家族控制,这些蛋白质要么推动受损细胞自我毁灭,要么帮助其抵抗死亡,这也是某些肿瘤对化疗产生耐受的重要原因。研究团队利用数百份卵巢癌样本的基因表达数据,对每位患者线粒体死亡通路的激活程度进行了评分。然后他们仅保留那些与该通路明显相关的图像特征,搭建起肿瘤外观与内部通路之间的“病理组学”桥梁。
构建患者风险评分
从数千个初始测量中,研究人员通过多层统计筛选和机器学习逐步缩减特征集,最终得到12个能最好预测患者生存时间的核心图像特征。这些特征被合并为一个单一数值——他们称之为MAR-PTL模型的风险评分。基于该评分,患者被分为高风险组和低风险组。该模型在训练组和独立的测试组中均能正确区分预后,优于诸如疾病分期和年龄等常规临床指标。换句话说,一旦被解码,肿瘤的隐性视觉指纹就携带了关于患者未来的重要信息。
一个关键的生存蛋白及其“邻里”
进一步挖掘后,研究突出了一个基因BCL2L2作为核心角色。该基因有助于抑制线粒体介导的细胞死亡,其较高的表达水平与较差的生存率相关。有趣的是,来自组织图像的特定深度学习特征与BCL2L2的表达呈同向或反向变化,这表明计算机可以“看到”这一分子抑制器如何重塑肿瘤结构。单细胞分析(逐一考察数千个单细胞)显示,富含BCL2L2的癌细胞具有独特的能量相关代谢特征,并与周围的支持细胞(如成纤维细胞和血管内皮细胞)进行密切交流。这些相互作用似乎形成了一个滋养性的“邻里”,帮助肿瘤抵抗压力并扩散。 
这对患者可能意味着什么
总体来看,这项工作表明显微镜图像中蕴含的信息远超肉眼所见。通过将数字病理与肿瘤细胞生死选择的生物学结合,MAR-PTL模型提供了一种更敏锐的方法来识别卵巢癌中最高风险的患者。将BCL2L2确立为一个关键枢纽,以及其与肿瘤代谢及周围支持细胞的紧密联系,为新的治疗思路指明了方向——例如,开发能解除这一生存开关或破坏其与邻近组织通讯的药物。尽管这些发现仍需在前瞻性研究和实验室实验中验证,但它们为更个性化的护理铺平了道路,最终可能为面对此类挑战性疾病的女性带来更好的生存机会。
引用: Qin, Lh., Huang, X., Yang, C. et al. Mitochondrial apoptosis gene-based pathomics for ovarian cancer prognosis. Sci Rep 16, 13231 (2026). https://doi.org/10.1038/s41598-026-40121-5
关键词: 卵巢癌, 数字病理, 深度学习, 线粒体凋亡, 肿瘤微环境