Clear Sky Science · nl
Pathomics op basis van mitochondriale apoptosegenen voor prognose bij ovariumkanker
Een nieuwe manier om kankerverwijzingen te lezen
Eierstokkanker wordt vaak een "stille moordenaar" genoemd omdat het meestal onopgemerkt blijft totdat het zich al heeft verspreid, waardoor behandeling en voorspelling van wie het goed zal doen moeilijk zijn. Deze studie biedt een frisse benadering: computers worden geleerd verborgen patronen in microscoopbeelden van tumoren te lezen en deze te koppelen aan de manier waarop tumorcellen beslissen te leven of te sterven. Daarmee proberen de onderzoekers patiënten nauwkeuriger in hoger- en lagerisicogroepen in te delen dan bestaande methoden, en zwakke plekken te vinden die nieuwe behandelingen zouden kunnen aanwenden.
Dieper kijken in tumorbeelden
Pathologen beoordelen kanker traditioneel door gekleurde weefselsneden onder een microscoop te bekijken en te beschrijven wat ze zien. Hoewel deze methode krachtig is, is ze ook subjectief en moeite heeft met subtiele details. Het team achter deze studie gebruikte digitale "whole-slide"-beelden van eierstoktumoren en knipte elk groot beeld in vele kleinere tegels. Een deep-learningsysteem genaamd ResNet50 scande deze tegels om duizenden wiskundige kenmerken te extraheren die patronen beschrijven in celvorm, textuur en de rangschikking van cellen en ondersteunend weefsel. Tegelijkertijd kwantificeerde gespecialiseerde software meer klassieke beeldkenmerken, zoals kernmaat en weefselstructuur, om een rijk beeld van het uiterlijk van elke tumor op te bouwen. 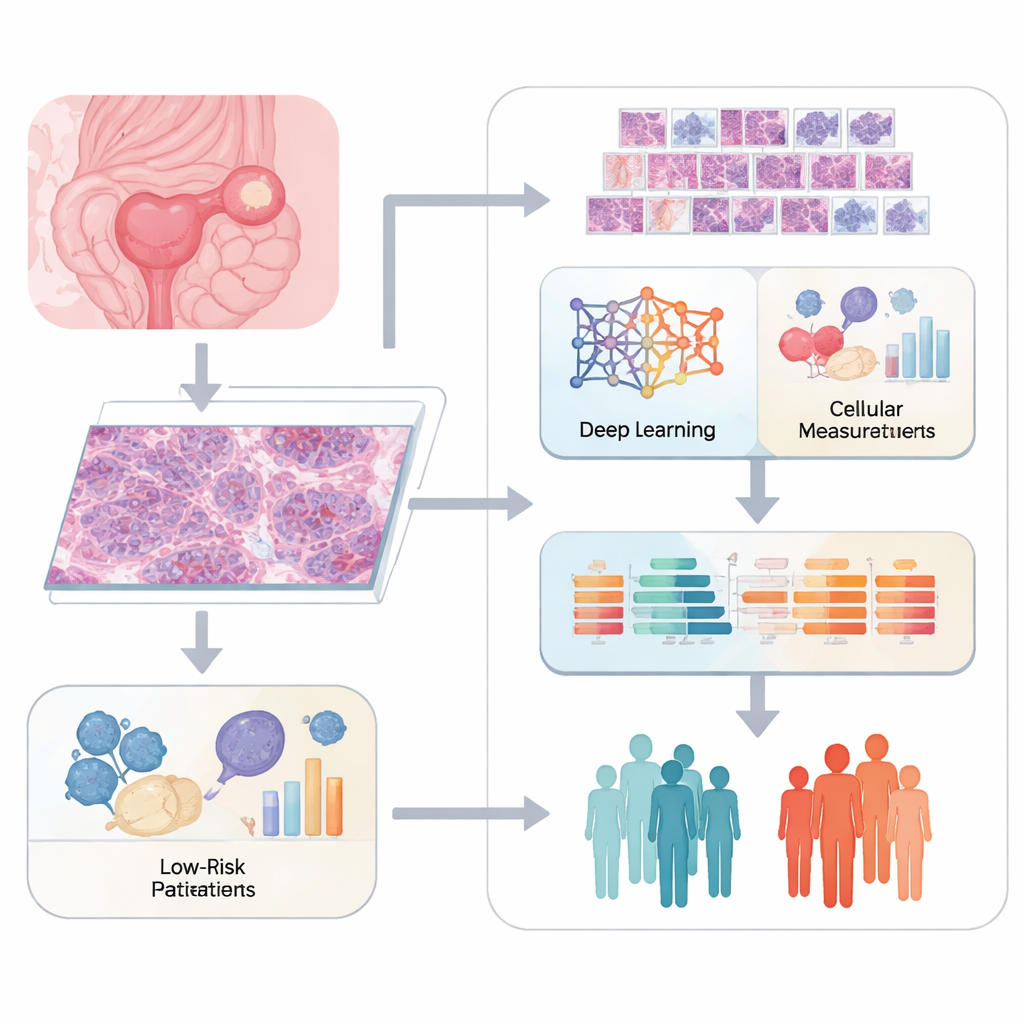
Beelden koppelen aan signalen voor celdood
In plaats van te stoppen bij hoe de tumor eruitziet, verbonden de onderzoekers deze beeldkenmerken met een vitaal leven‑dood‑schakelaar in cellen, bekend als mitochondriale apoptose. Dit proces wordt geregeld door een familie van eiwitten die een beschadigde cel kunnen aanzetten tot zelfvernietiging of juist helpen weerstand te bieden tegen celdood, een belangrijke reden dat sommige tumoren chemotherapie weerstaan. Met genexpressiegegevens van honderden eierstokkankermonsters beoordeelde het team hoe sterk deze mitochondriale doodspad in elke patiënt geactiveerd was. Daarna hielden ze alleen die beeldkenmerken over die duidelijk aan dit pad gekoppeld waren, en bouwden zo een "pathomics"-brug tussen het uiterlijk van de tumor en de interne bedrading.
Een risicoscore voor patiënten opbouwen
Uit duizenden initiële metingen filterden de onderzoekers de set door meerdere lagen statistische selectie en machine learning, en kwamen uit op 12 kernbeeldkenmerken die het beste voorspelden hoe lang patiënten overleefden. Deze kenmerken werden gecombineerd tot één getal, een risicoscore die zij het MAR-PTL-model noemen. Patiënten werden in hoge- en lage-risicogroepen verdeeld op basis van deze score. Het model wist uitkomsten correct te onderscheiden in zowel een trainingsgroep als een aparte testgroep en presteerde beter dan standaard klinische maatstaven zoals ziektestadium en leeftijd. Met andere woorden: de verborgen visuele vingerafdrukken van een tumor, eenmaal ontcijferd, bevatten krachtige informatie over de toekomst van een patiënt.
Een sleuteleiwit voor overleving en zijn omgeving
Dieper gravend belichtte de studie één gen, BCL2L2, als een centrale speler. Dit gen helpt mitochondriale celdood te blokkeren, en hogere niveaus daarvan werden gekoppeld aan slechtere overleving. Intrigerend was dat specifieke deep-learningkenmerken uit de weefselbeelden in overeenstemming stegen of daalden met BCL2L2, wat suggereert dat de computer kon "zien" hoe deze moleculaire rem op celdood de tumorarchitectuur verandert. Single-cellanalyse, die duizenden individuele cellen één voor één bekijkt, toonde dat BCL2L2-rijke kankercellen een kenmerkend energiegerelateerd metabolisme hadden en intens communiceerden met nabijgelegen steuncellen zoals fibroblasten en cellen die bloedvaten bekleden. Deze interacties leken een verzorgende omgeving te vormen die tumoren helpt weerstand te bieden tegen stress en zich te verspreiden. 
Wat dit voor patiënten kan betekenen
Samen genomen laten deze bevindingen zien dat microscoopbeelden veel meer bevatten dan op het eerste gezicht zichtbaar is. Door digitale pathologie te combineren met kennis over hoe tumorcellen leven of sterven, biedt het MAR-PTL-model een scherper middel om eierstokkankerpatiënten met het hoogste risico te signaleren. De ontdekking van BCL2L2 als een belangrijk knooppunt, en de nauwe verbindingen met zowel tumormetabolisme als de omliggende steuncellen, wijst op nieuwe behandelideeën — bijvoorbeeld medicijnen die deze overlevingsschakel uitschakelen of de communicatie met nabijgelegen weefsels verstoren. Hoewel deze bevindingen nog moeten worden getest in prospectieve studies en laboratoriumexperimenten, effenen ze het pad naar meer gepersonaliseerde zorg en uiteindelijk betere kansen voor vrouwen die met deze moeilijke ziekte worden geconfronteerd.
Bronvermelding: Qin, Lh., Huang, X., Yang, C. et al. Mitochondrial apoptosis gene-based pathomics for ovarian cancer prognosis. Sci Rep 16, 13231 (2026). https://doi.org/10.1038/s41598-026-40121-5
Trefwoorden: eierstokkanker, digitale pathologie, deep learning, mitochondriale apoptose, tumor-micro-omgeving