Clear Sky Science · ru
Патомика, основанная на генах митохондриального апоптоза, для прогноза при раке яичников
Новый способ читать подсказки рака
Рак яичников часто называют «тихим убийцей», потому что он обычно остается незамеченным до тех пор, пока не распространился, что затрудняет лечение и прогнозирование исхода. В этом исследовании предложен свежий подход: обучить компьютеры распознавать скрытые шаблоны на микроскопических изображениях опухолей и связывать их с тем, как клетки опухоли принимают решения о жизни или смерти. Делая это, авторы стремятся точнее, чем нынешние методы, разделить пациентов на группы с высоким и низким риском и выявить уязвимые места, на которые можно нацелить новые терапии.
Глубже в изображения опухоли
Патологи традиционно оценивают рак, рассматривая окрашенные срезы ткани под микроскопом и описывая увиденное. Хотя этот метод силен, он субъективен и плохо улавливает тонкие детали. Команда использовала цифровые «целостные слайды» опухолей яичников и разрезала каждое большое изображение на множество маленьких плиток. Система глубокого обучения ResNet50 просканировала эти плитки и извлекла тысячи математических признаков, описывающих форму клеток, текстуру и организацию клеток и поддерживающей ткани. Параллельно специализированное программное обеспечение количественно оценивало более классические признаки изображения, такие как размер ядра и структура ткани, чтобы создать богатое описание внешнего вида каждой опухоли. 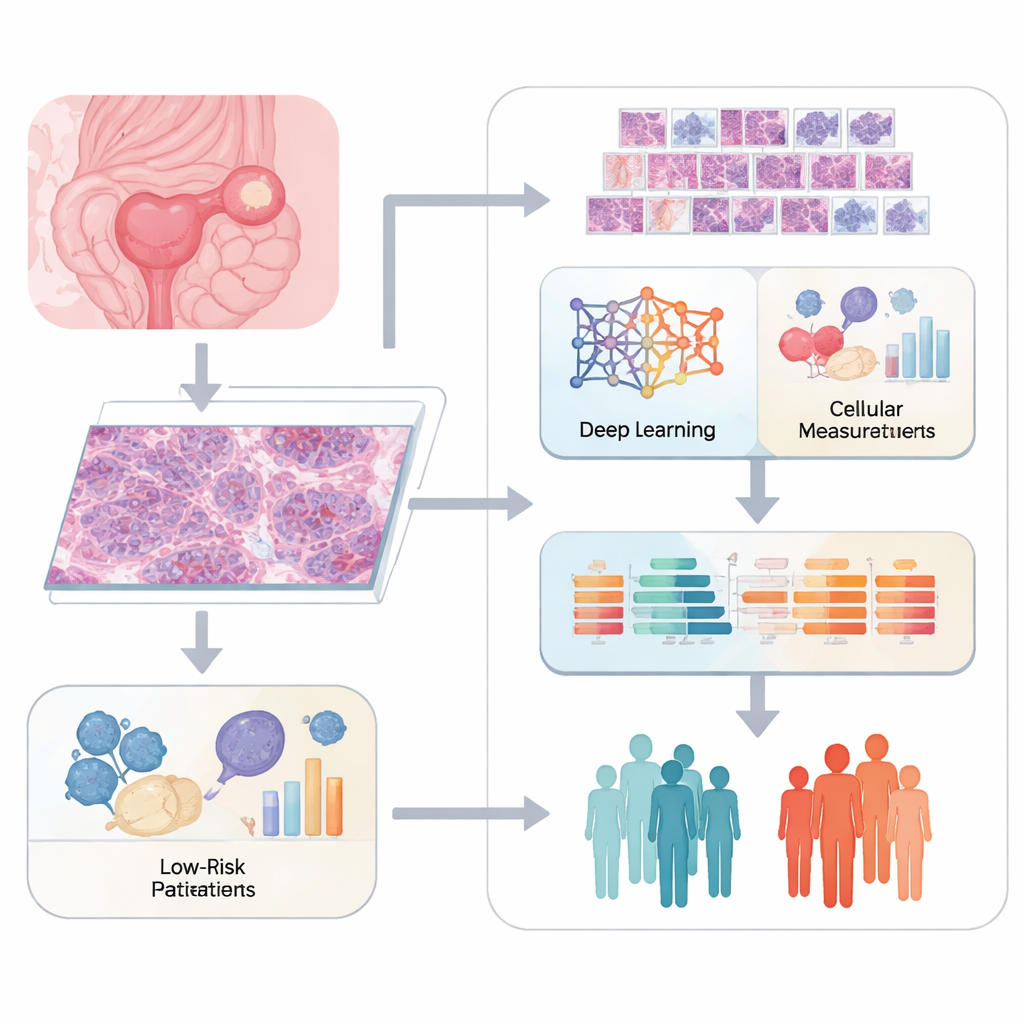
Связывание изображений с сигналами клеточной смерти
Вместо того чтобы останавливаться на внешнем облике опухоли, исследователи связали эти признаки изображения с жизненно важным переключателем «жизнь–смерть» в клетке, известным как митохондриальный апоптоз. Этот процесс регулируется семейством белков, которые либо толкают поврежденную клетку к самоуничтожению, либо помогают ей сопротивляться смерти — ключевая причина, по которой некоторые опухоли не поддаются химиотерапии. Используя данные об экспрессии генов сотен образцов рака яичников, команда оценила степень активации митохондриального пути смерти у каждого пациента. Затем оставили только те признаки изображения, которые были явно связаны с этим путем, построив «патомический» мост между внешним видом опухоли и ее внутренней схемой.
Создание риска для пациентов
Из тысяч исходных измерений исследователи отобрали набор с помощью нескольких уровней статистической фильтрации и машинного обучения, пришли к 12 ключевым признакам на основе изображения, которые лучше всего предсказывали выживаемость пациентов. Эти признаки объединили в одно число — риск‑скор, который они назвали моделью MAR-PTL. Пациентов разделили на группы высокого и низкого риска на основе этого показателя. Модель корректно различала исходы как в обучающей, так и в отдельной тестовой выборке, превосходя стандартные клинические показатели, такие как стадия заболевания и возраст. Иными словами, скрытые визуальные отпечатки опухоли, однажды расшифрованные, несли мощную информацию о будущем пациента.
Ключевой белок выживания и его окружение
При более глубоком анализе исследование выделило один ген — BCL2L2 — в качестве центрального участника. Этот ген помогает блокировать митохондриальную смерть клеток, и более высокий уровень его экспрессии был связан с худшей выживаемостью. Любопытно, что определенные признаки глубокого обучения, извлеченные из тканевых изображений, повышались или снижались синхронно с уровнем BCL2L2, что указывает на то, что компьютер мог «видеть», как этот молекулярный тормоз клеточной смерти перестраивает архитектуру опухоли. Анализ на уровне одной клетки, который рассматривает тысячи индивидуальных клеток по одной, показал, что опухолевые клетки, богатые BCL2L2, обладают характерным метаболизмом, связанным с энергией, и интенсивно взаимодействуют с окружающими поддерживающими клетками, такими как фибробласты и клетки, выстилающие кровеносные сосуды. Эти взаимодействия, по-видимому, формируют благоприятное «окружение», которое помогает опухолям противостоять стрессу и распространяться. 
Что это может значить для пациентов
В совокупности эта работа показывает, что микроскопические изображения содержат гораздо больше, чем кажется на первый взгляд. Объединив цифровую патологию с пониманием того, как опухолевые клетки выбирают жизнь или смерть, модель MAR-PTL предлагает более точный способ отмечать пациенток с раком яичников, находящихся в наивысшем риске. Открытие BCL2L2 в роли ключевого узла и его тесные связи как с метаболизмом опухоли, так и с окружающими поддерживающими клетками указывают на новые идеи для терапии — например, препараты, которые отключают этот «переключатель» выживания или разрушают его коммуникацию с окружающими тканями. Хотя эти выводы еще нужно проверить в проспективных исследованиях и лабораторных экспериментах, они прокладывают путь к более персонализированной помощи и, в конечном счете, к лучшим шансам для женщин, столкнувшихся с этим сложным заболеванием.
Цитирование: Qin, Lh., Huang, X., Yang, C. et al. Mitochondrial apoptosis gene-based pathomics for ovarian cancer prognosis. Sci Rep 16, 13231 (2026). https://doi.org/10.1038/s41598-026-40121-5
Ключевые слова: рак яичников, цифровая патология, глубокое обучение, митохондриальный апоптоз, микроокружение опухоли