Clear Sky Science · fr
Pathomique basée sur les gènes d'apoptose mitochondriale pour le pronostic du cancer de l'ovaire
Une nouvelle façon de lire les indices du cancer
Le cancer de l'ovaire est souvent qualifié de « tueur silencieux » car il reste généralement discret jusqu'à ce qu'il se soit déjà propagé, ce qui rend le traitement difficile et complique la prédiction du pronostic. Cette étude propose une approche nouvelle : apprendre aux ordinateurs à lire des motifs cachés dans des images microscopiques de tumeurs et à les relier aux mécanismes par lesquels les cellules tumorales choisissent de vivre ou de mourir. Ce faisant, les chercheurs visent à classer les patientes en groupes à plus ou moins haut risque de manière plus précise que les méthodes actuelles, et à dévoiler des vulnérabilités que de nouveaux traitements pourraient cibler.
Regarder plus profondément dans les images tumorales
Les pathologistes évaluent traditionnellement le cancer en examinant des coupes de tissu colorées au microscope et en décrivant ce qu'ils observent. Bien que cette méthode soit puissante, elle reste subjective et peine à saisir les détails subtils. L'équipe de cette étude a utilisé des images numériques « lames entières » de tumeurs ovariennes et a découpé chaque grande image en de nombreuses petites tuiles. Un système d'apprentissage profond appelé ResNet50 a scanné ces tuiles pour extraire des milliers de caractéristiques mathématiques décrivant des motifs de forme cellulaire, de texture, et l'organisation des cellules et des tissus de soutien. En parallèle, des logiciels spécialisés ont quantifié des traits d'image plus classiques, tels que la taille des noyaux et la structure tissulaire, afin de dresser une image riche de l'apparence de chaque tumeur. 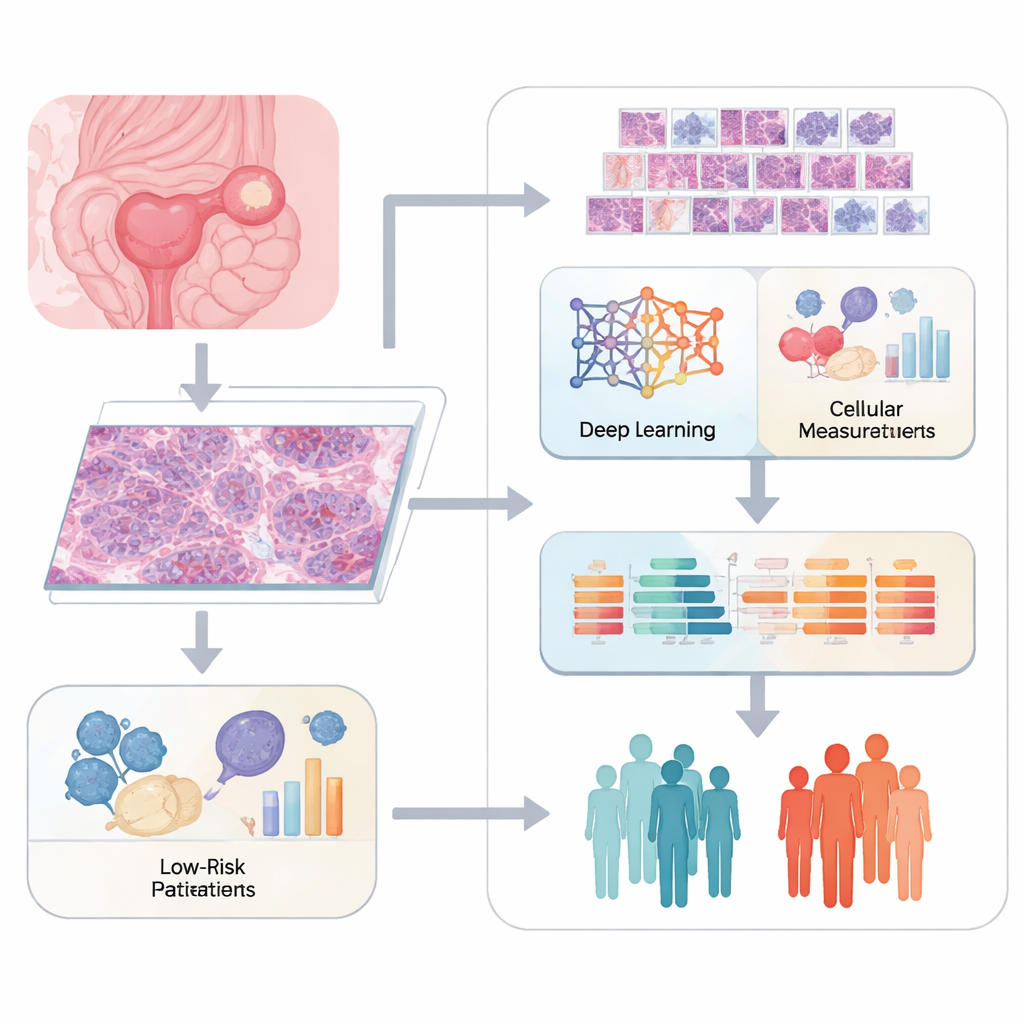
Relier les images aux signaux de mort cellulaire
Plutôt que de s'arrêter à l'aspect externe de la tumeur, les chercheurs ont relié ces caractéristiques d'image à un interrupteur vital de vie–mort à l'intérieur des cellules connu sous le nom d'apoptose mitochondriale. Ce processus est contrôlé par une famille de protéines qui peuvent soit pousser une cellule endommagée à s'autodétruire, soit l'aider à résister à la mort — une raison majeure pour laquelle certaines tumeurs se montrent insensibles à la chimiothérapie. En utilisant des données d'expression génique provenant de centaines d'échantillons de cancer de l'ovaire, l'équipe a évalué l'intensité d'activation de la voie de mort mitochondriale chez chaque patiente. Ils n'ont ensuite conservé que les caractéristiques d'image clairement liées à cette voie, construisant ainsi un pont « pathomique » entre l'apparence tumorale et son câblage interne.
Construire un score de risque pour les patientes
À partir de milliers de mesures initiales, les chercheurs ont réduit l'ensemble via plusieurs niveaux de filtrage statistique et d'apprentissage automatique, pour aboutir à 12 caractéristiques d'image centrales qui prédisaient le mieux la durée de survie des patientes. Ces caractéristiques ont été combinées en un nombre unique, un score de risque qu'ils appellent le modèle MAR-PTL. Les patientes ont été réparties en groupes à risque élevé et faible sur la base de ce score. Le modèle a correctement distingué les issues tant dans un groupe d'entraînement que dans un groupe de test distinct, surpassant des mesures cliniques standard telles que le stade de la maladie et l'âge. Autrement dit, les empreintes visuelles cachées d'une tumeur, une fois décodées, portaient des informations puissantes sur l'avenir d'une patiente.
Une protéine clé de survie et son voisinage
En creusant davantage, l'étude a mis en lumière un gène, BCL2L2, comme acteur central. Ce gène aide à bloquer la mort mitochondriale des cellules, et des niveaux plus élevés de son expression étaient associés à une survie plus faible. Fait intrigant, certaines caractéristiques extraites par apprentissage profond des images tissulaires augmentaient ou diminuaient en parallèle avec BCL2L2, suggérant que l'algorithme pouvait « voir » comment ce frein moléculaire à la mort cellulaire modifie l'architecture tumorale. L'analyse en cellule unique, qui examine des milliers de cellules individuelles, a montré que les cellules cancéreuses riches en BCL2L2 présentaient un métabolisme énergétique distinct et communiquaient intensément avec des cellules de soutien voisines telles que les fibroblastes et les cellules endothéliales. Ces interactions semblaient former un microenvironnement nourricier qui aide les tumeurs à résister au stress et à se propager. 
Ce que cela pourrait signifier pour les patientes
Pris dans leur ensemble, ces travaux montrent que les images microscopiques recèlent bien plus que ce que l'oeil perçoit. En fusionnant la pathologie numérique avec la connaissance de la façon dont les cellules tumorales choisissent la vie ou la mort, le modèle MAR-PTL offre un moyen plus précis d'identifier les patientes atteintes d'un cancer de l'ovaire à risque élevé. La découverte de BCL2L2 comme nœud clé, et ses liens étroits avec le métabolisme tumoral et les cellules de soutien environnantes, ouvre des pistes thérapeutiques — par exemple des médicaments qui désarment cet interrupteur de survie ou perturbent sa communication avec les tissus voisins. Bien que ces résultats doivent encore être validés par des études prospectives et des expériences en laboratoire, ils ouvrent la voie à des soins plus personnalisés et, en définitive, à de meilleures chances pour les femmes confrontées à cette maladie difficile.
Citation: Qin, Lh., Huang, X., Yang, C. et al. Mitochondrial apoptosis gene-based pathomics for ovarian cancer prognosis. Sci Rep 16, 13231 (2026). https://doi.org/10.1038/s41598-026-40121-5
Mots-clés: cancer de l'ovaire, pathologie numérique, apprentissage profond, apoptose mitochondriale, microenvironnement tumoral