Clear Sky Science · es
Patómica basada en genes de apoptosis mitocondrial para el pronóstico del cáncer de ovario
Una nueva manera de leer las pistas del cáncer
El cáncer de ovario suele llamarse un «asesino silencioso» porque por lo general pasa inadvertido hasta que ya se ha extendido, lo que dificulta el tratamiento y la predicción de quién tendrá un buen pronóstico. Este estudio ofrece un enfoque novedoso: enseña a las máquinas a leer patrones ocultos en imágenes microscópicas de tumores y a relacionarlos con la forma en que las células tumorales deciden vivir o morir. Al hacerlo, los investigadores buscan clasificar a los pacientes en grupos de mayor y menor riesgo con más precisión que los métodos actuales y descubrir puntos débiles que puedan ser dianas de nuevos tratamientos.
Profundizando en las imágenes tumorales
Los patólogos tradicionalmente evalúan el cáncer observando cortes de tejido teñido bajo el microscopio y describiendo lo que ven. Aunque este método es potente, también es subjetivo y tiene dificultades para captar detalles sutiles. El equipo de este estudio empleó imágenes digitales de «lámina completa» de tumores de ovario y dividió cada imagen grande en muchos mosaicos más pequeños. Un sistema de aprendizaje profundo llamado ResNet50 escaneó esos mosaicos para extraer miles de características matemáticas que describen patrones en la forma celular, la textura y la organización de células y tejidos de sostén. En paralelo, software especializado cuantificó rasgos de imagen más clásicos, como el tamaño del núcleo y la estructura tisular, para construir un retrato detallado de la apariencia de cada tumor. 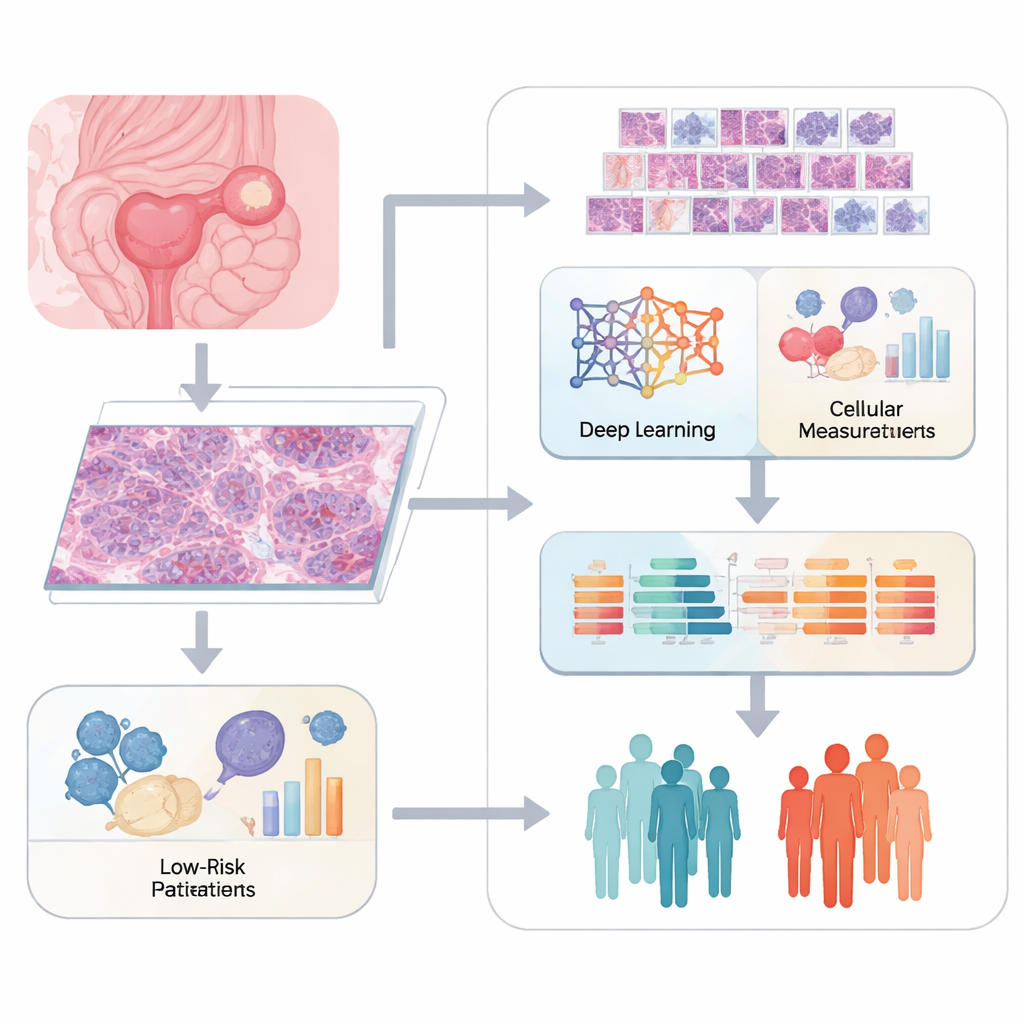
Conectando las imágenes con las señales de muerte celular
En lugar de detenerse en el aspecto del tumor, los investigadores vincularon estas características de imagen con un interruptor vital de vida o muerte dentro de las células conocido como apoptosis mitocondrial. Este proceso está gobernado por una familia de proteínas que pueden empujar a una célula dañada a autodestruirse o ayudarla a resistir la muerte, una razón clave por la que algunos tumores hacen caso omiso de la quimioterapia. Usando datos de actividad génica de cientos de muestras de cáncer de ovario, el equipo puntuó cuánto estaba activado el camino mitocondrial de muerte en cada paciente. Luego conservó solo aquellas características de imagen que mostraron una relación clara con esta vía, construyendo un puente «patómico» entre la apariencia del tumor y su cableado interno.
Construyendo una puntuación de riesgo para los pacientes
A partir de miles de mediciones iniciales, los investigadores redujeron el conjunto mediante varias capas de filtrado estadístico y aprendizaje automático, llegando a 12 características principales basadas en la imagen que mejor predijeron la supervivencia de los pacientes. Estas características se combinaron en un único número, una puntuación de riesgo que denominaron modelo MAR-PTL. Los pacientes se dividieron en grupos de alto y bajo riesgo según esta puntuación. El modelo distinguió correctamente los resultados tanto en un grupo de entrenamiento como en un grupo de prueba independiente, superando a medidas clínicas estándar como el estadio de la enfermedad y la edad. En otras palabras, las huellas visuales ocultas de un tumor, una vez descifradas, aportaron información poderosa sobre el futuro del paciente.
Una proteína clave para la supervivencia y su vecindario
Al profundizar más, el estudio destacó un gen, BCL2L2, como un actor central. Este gen ayuda a bloquear la muerte mitocondrial, y niveles más altos del mismo se asociaron con peor supervivencia. De forma intrigante, características específicas extraídas por el aprendizaje profundo de las imágenes de tejido aumentaban o disminuían en paralelo con BCL2L2, lo que sugiere que la máquina podía «ver» cómo este freno molecular a la muerte celular remodela la arquitectura tumoral. El análisis a nivel de célula única, que examina miles de células individuales una por una, mostró que las células cancerosas ricas en BCL2L2 presentaban un metabolismo distintivo relacionado con la energía y se comunicaban intensamente con células de soporte cercanas como fibroblastos y células que recubren los vasos sanguíneos. Estas interacciones parecían formar un vecindario protector que ayuda a los tumores a resistir el estrés y a diseminarse. 
Lo que esto podría significar para los pacientes
En conjunto, este trabajo demuestra que las imágenes de microscopio contienen mucho más de lo que parece a simple vista. Al fusionar la patología digital con el conocimiento de cómo las células tumorales eligen la vida o la muerte, el modelo MAR-PTL ofrece una forma más afinada de identificar a las pacientes con cáncer de ovario con mayor riesgo. El hallazgo de BCL2L2 como un centro clave, y sus estrechos vínculos tanto con el metabolismo tumoral como con las células de soporte circundantes, apunta a nuevas ideas terapéuticas —por ejemplo, fármacos que desactiven este interruptor de supervivencia o que interrumpan su comunicación con los tejidos vecinos. Aunque estos hallazgos aún deben probarse en estudios prospectivos y experimentos de laboratorio, abren el camino hacia una atención más personalizada y, en última instancia, mejores opciones para las mujeres que enfrentan esta enfermedad desafiante.
Cita: Qin, Lh., Huang, X., Yang, C. et al. Mitochondrial apoptosis gene-based pathomics for ovarian cancer prognosis. Sci Rep 16, 13231 (2026). https://doi.org/10.1038/s41598-026-40121-5
Palabras clave: cáncer de ovario, patología digital, aprendizaje profundo, apoptosis mitocondrial, microambiente tumoral