Clear Sky Science · pl
Pathomika oparta na genach apoptozy mitochondrialnej w prognozowaniu raka jajnika
Nowy sposób odczytywania wskazówek o raku
Rak jajnika bywa nazywany „cichym zabójcą”, ponieważ zwykle pozostaje niezauważony, dopóki się nie rozprzestrzeni, co utrudnia leczenie i prognozowanie przebiegu choroby. Niniejsze badanie proponuje świeże podejście: uczy komputery rozpoznawać ukryte wzory w mikroskopowych obrazach guzów i powiązywać je z decyzjami komórek o życiu lub śmierci. Dzięki temu badacze dążą do dokładniejszego podziału pacjentek na grupy o wysokim i niskim ryzyku niż obecne metody oraz do odkrycia słabych punktów, które mogą stać się celem nowych terapii.
Bardziej wnikliwe spojrzenie na obrazy guzów
Patolodzy tradycyjnie oceniają raka, oglądając barwione skrawki tkanek pod mikroskopem i opisując to, co widzą. Choć ta metoda jest potężna, ma charakter subiektywny i trudno jej wychwycić subtelne cechy. Zespół stojący za tym badaniem wykorzystał cyfrowe obrazy całych preparatów tkanek jajnika i pociął każdą dużą fotografię na wiele mniejszych płytek. System uczenia głębokiego o nazwie ResNet50 przeskanował te płytki, wydobywając tysiące matematycznych cech opisujących wzory w kształcie komórek, teksturze oraz ułożeniu komórek i tkanek wspierających. Równolegle specjalistyczne oprogramowanie skwantyfikowało bardziej klasyczne cechy obrazu, takie jak rozmiar jądra i struktura tkanki, aby zbudować bogaty opis wyglądu każdego guza. 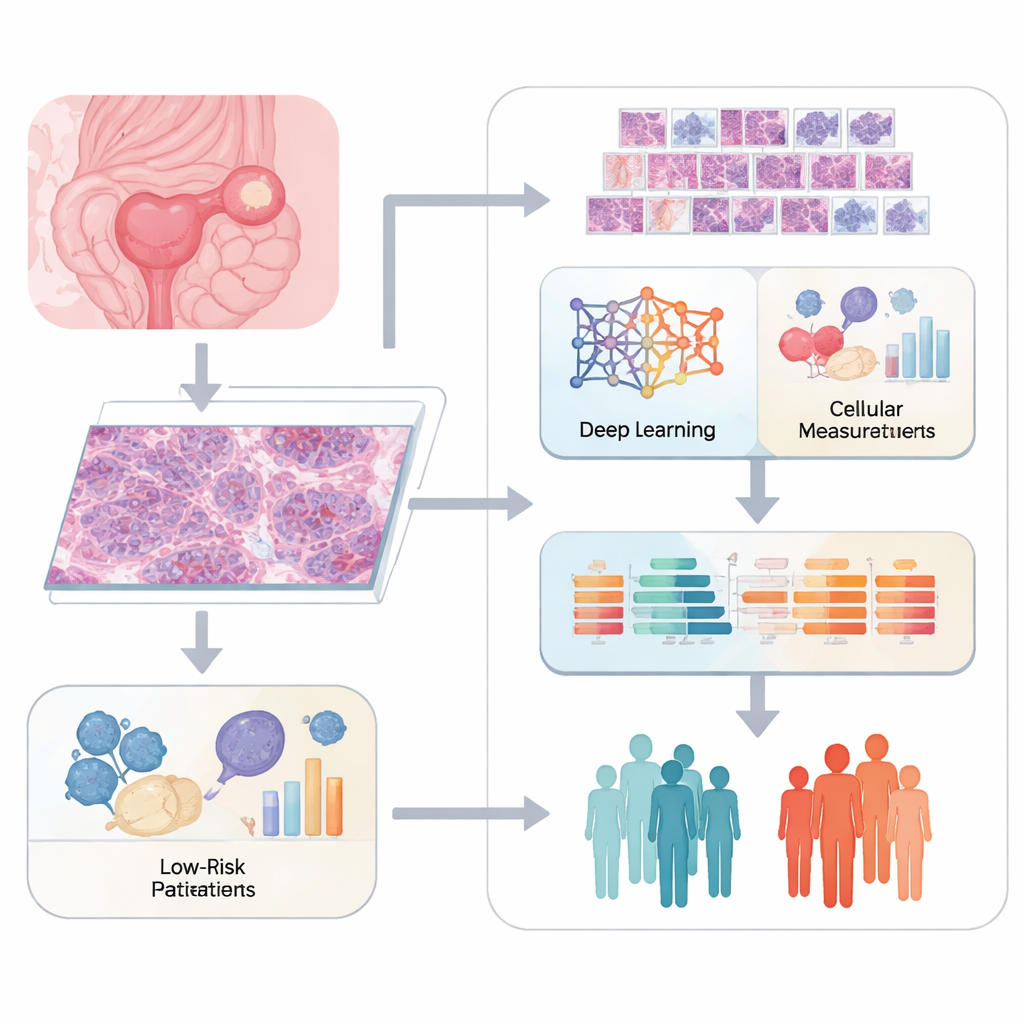
Łączenie obrazów z sygnałami śmierci komórkowej
Zamiast zatrzymywać się na wyglądzie guza, badacze powiązali cechy obrazu z kluczowym przełącznikiem życia i śmierci w komórkach znanym jako apoptoza mitochondrialna. Proces ten jest regulowany przez rodzinę białek, które mogą skłaniać uszkodzoną komórkę do autodestrukcji lub pomagać jej w opieraniu się śmierci — to ważny powód, dla którego niektóre nowotwory są oporne na chemioterapię. Wykorzystując dane o aktywności genów z setek próbek raka jajnika, zespół ocenił, jak silnie w danym pacjencie był aktywowany szlak śmierci mitochondrialnej. Następnie zachowano tylko te cechy obrazu, które były wyraźnie powiązane z tym szlakiem, budując „pathomikowy” most między wyglądem guza a jego wewnętrznym okablowaniem.
Budowanie wskaźnika ryzyka dla pacjentek
Z tysięcy początkowych pomiarów badacze odfiltrowali zestaw przez kilka warstw selekcji statystycznej i uczenia maszynowego, dochodząc do 12 kluczowych cech obrazowych, które najlepiej przewidywały długość przeżycia pacjentek. Cechy te połączono w jedną liczbę — wskaźnik ryzyka nazwany modelem MAR-PTL. Pacjentki podzielono na grupy wysokiego i niskiego ryzyka w oparciu o ten wynik. Model poprawnie rozróżniał wyniki zarówno w zbiorze uczącym, jak i w odrębnym zbiorze testowym, przewyższając standardowe miary kliniczne, takie jak stopień zaawansowania choroby i wiek. Innymi słowy, ukryte wizualne odciski guza, po ich odkodowaniu, niosły silne informacje o przyszłości pacjentki.
Kluczowe białko przeżycia i jego otoczenie
Idąc dalej, badanie wyodrębniło jeden gen, BCL2L2, jako centralnego gracza. Gen ten pomaga blokować mitochondrialną śmierć komórkową, a jego wyższe poziomy wiązały się z gorszym przeżyciem. Co interesujące, konkretne cechy wyuczone przez sieć głębokiego uczenia z obrazów tkankowych wzrastały lub malały zgodnie z poziomami BCL2L2, co sugeruje, że komputer mógł „widzieć”, jak ten molekularny hamulec śmierci komórkowej przekształca architekturę guza. Analiza pojedynczych komórek, która bada tysiące pojedynczych komórek, wykazała, że komórki nowotworowe bogate w BCL2L2 miały charakterystyczny metabolizm związany z energią i intensywnie komunikowały się z pobliskimi komórkami wspierającymi, takimi jak fibroblasty i komórki wyściełające naczynia krwionośne. Interakcje te wydawały się tworzyć sprzyjające sąsiedztwo, które pomaga guzom opierać się stresowi i rozprzestrzeniać się. 
Co to może znaczyć dla pacjentek
Podsumowując, ta praca pokazuje, że obrazy mikroskopowe zawierają znacznie więcej informacji, niż widać na pierwszy rzut oka. Poprzez połączenie patologii cyfrowej z wiedzą o tym, jak komórki nowotworowe wybierają życie lub śmierć, model MAR-PTL oferuje ostrzejszy sposób identyfikacji pacjentek z najsłabszym rokowaniem w raku jajnika. Odkrycie BCL2L2 jako kluczowego węzła oraz jego ścisłe powiązania zarówno z metabolizmem guza, jak i z otaczającymi komórkami wsparcia, wskazują na nowe pomysły terapeutyczne — na przykład leki, które unieszkodliwią ten przełącznik przeżycia lub przerwą jego komunikację z otaczającymi tkankami. Chociaż te ustalenia wymagają jeszcze potwierdzenia w badaniach prospektywnych i eksperymentach laboratoryjnych, torują drogę ku bardziej spersonalizowanej opiece i ostatecznie lepszym szansom dla kobiet zmagających się z tą trudną chorobą.
Cytowanie: Qin, Lh., Huang, X., Yang, C. et al. Mitochondrial apoptosis gene-based pathomics for ovarian cancer prognosis. Sci Rep 16, 13231 (2026). https://doi.org/10.1038/s41598-026-40121-5
Słowa kluczowe: rak jajnika, patologia cyfrowa, uczenie głębokie, apoptoza mitochondrialna, mikrośrodowisko guza