Clear Sky Science · it
Mitochondrial apoptosis gene-based pathomics for ovarian cancer prognosis
Un nuovo modo di leggere gli indizi del cancro
Il cancro ovarico è spesso definito un “killer silenzioso” perché di solito resta inosservato fino a quando non si è già diffuso, rendendo difficile il trattamento e la previsione dell’andamento clinico. Questo studio propone un approccio nuovo: addestrare i computer a leggere modelli nascosti nelle immagini al microscopio dei tumori e collegarli a come le cellule tumorali decidono di vivere o morire. In questo modo i ricercatori intendono classificare i pazienti in gruppi a rischio più alto o più basso con maggiore precisione rispetto ai metodi attuali e scoprire punti deboli che nuovi trattamenti potrebbero colpire.
Esplorare più in profondità le immagini tumorali
I patologi giudicano tradizionalmente il cancro osservando fette di tessuto colorato al microscopio e descrivendo ciò che vedono. Sebbene questo metodo sia potente, è anche soggettivo e fatica a cogliere dettagli sottili. Il gruppo di ricerca ha usato immagini digitali “whole-slide” di tumori ovarici e ha suddiviso ogni immagine di grandi dimensioni in molte piccole tessere. Un sistema di deep learning chiamato ResNet50 ha analizzato queste tessere per estrarre migliaia di caratteristiche matematiche che descrivono pattern nella forma cellulare, nella texture e nell’organizzazione di cellule e tessuti di supporto. Parallelamente, software specializzati hanno quantificato tratti d’immagine più classici, come la dimensione del nucleo e la struttura tissutale, per costruire un quadro ricco dell’aspetto di ciascun tumore. 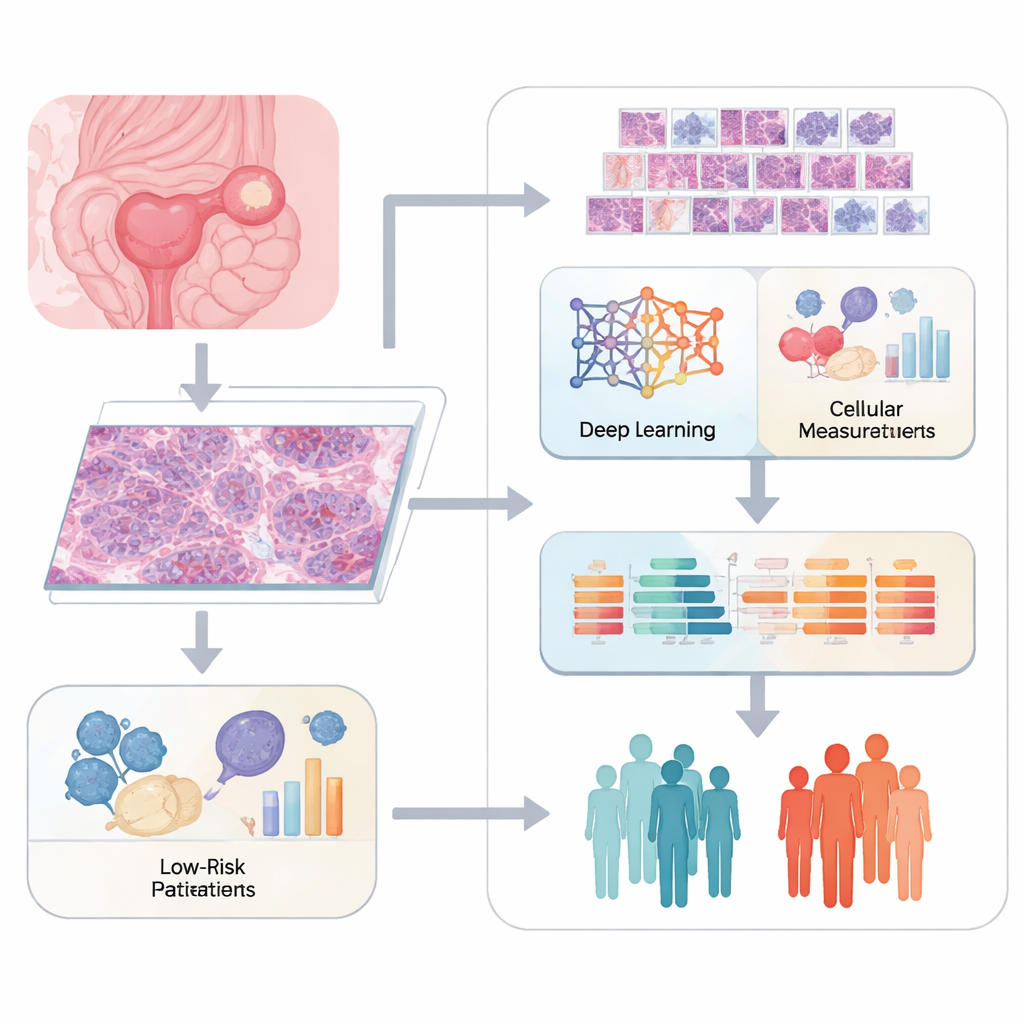
Collegare le immagini ai segnali di morte cellulare
Invece di fermarsi all’aspetto del tumore, i ricercatori hanno legato queste caratteristiche d’immagine a un interruttore vitale di vita–morte nelle cellule noto come apoptosi mitocondriale. Questo processo è regolato da una famiglia di proteine che possono spingere una cellula danneggiata all’autodistruzione o aiutarla a resistere alla morte, motivo chiave per cui alcuni tumori sopportano la chemioterapia. Utilizzando dati di espressione genica provenienti da centinaia di campioni di cancro ovarico, il team ha valutato quanto fosse attivata la via di morte mitocondriale in ciascun paziente. Hanno quindi mantenuto solo quelle caratteristiche d’immagine chiaramente collegate a questa via, costruendo un ponte “pathomico” tra l’aspetto del tumore e la sua cablatura interna.
Costruire un punteggio di rischio per i pazienti
Partendo da migliaia di misure iniziali, i ricercatori hanno ridotto il set attraverso diversi livelli di filtraggio statistico e apprendimento automatico, arrivando a 12 caratteristiche principali basate sull’immagine che meglio prevedevano la sopravvivenza dei pazienti. Queste caratteristiche sono state combinate in un unico valore, un punteggio di rischio che chiamano modello MAR-PTL. I pazienti sono stati divisi in gruppi a rischio alto e basso sulla base di questo punteggio. Il modello ha distinto correttamente gli esiti sia in un gruppo di addestramento sia in un gruppo di test separato, superando misure cliniche standard come lo stadio della malattia e l’età. In altre parole, le impronte visive nascoste di un tumore, una volta decodificate, contenevano informazioni potenti sul futuro del paziente.
Una proteina chiave per la sopravvivenza e il suo vicinato
Indagando più a fondo, lo studio ha messo in evidenza un gene, BCL2L2, come giocatore centrale. Questo gene contribuisce a bloccare la morte mitocondriale cellulare, e livelli più alti di esso sono stati associati a una peggiore sopravvivenza. In modo intrigante, caratteristiche specifiche estratte tramite deep learning dalle immagini tissutali aumentavano o diminuivano in parallelo con BCL2L2, suggerendo che il computer potesse “vedere” come questo freno molecolare alla morte cellulare rimodelli l’architettura del tumore. L’analisi a singola cellula, che osserva migliaia di cellule individuali una per una, ha mostrato che le cellule tumorali ricche di BCL2L2 presentavano un metabolismo distinto legato all’energia e comunicavano intensamente con cellule di supporto vicine come i fibroblasti e le cellule endoteliali. Queste interazioni sembravano formare un quartiere di sostegno che aiuta i tumori a resistere allo stress e a diffondersi. 
Cosa potrebbe significare per i pazienti
Nel complesso, questo lavoro dimostra che le immagini al microscopio contengono molto più di quanto appaia a un primo sguardo. Fondendo la patologia digitale con la conoscenza di come le cellule tumorali scelgono tra vita e morte, il modello MAR-PTL offre un modo più preciso per individuare i pazienti con cancro ovarico a rischio più elevato. La scoperta di BCL2L2 come nodo chiave, e i suoi forti legami sia con il metabolismo tumorale sia con le cellule di supporto circostanti, indica nuove idee terapeutiche — per esempio farmaci che disarmano questo interruttore di sopravvivenza o ne ostacolano la comunicazione con i tessuti vicini. Sebbene questi risultati debbano ancora essere verificati in studi prospettici e in esperimenti di laboratorio, aprono la strada a cure più personalizzate e, in ultima analisi, a migliori prospettive per le donne affette da questa malattia impegnativa.
Citazione: Qin, Lh., Huang, X., Yang, C. et al. Mitochondrial apoptosis gene-based pathomics for ovarian cancer prognosis. Sci Rep 16, 13231 (2026). https://doi.org/10.1038/s41598-026-40121-5
Parole chiave: cancro ovarico, patologia digitale, apprendimento profondo, apoptosi mitocondriale, microambiente tumorale