Clear Sky Science · de
Mitochondriale Apoptose-Gen-basierte Pathomik für die Prognose von Ovarialkarzinom
Eine neue Art, Krebs-Hinweise zu lesen
Ovarialkarzinom wird oft als „stiller Killer“ bezeichnet, weil es meist unbemerkt bleibt, bis es sich bereits ausgebreitet hat, was die Behandlung erschwert und Vorhersagen über den Verlauf schwierig macht. Diese Studie schlägt einen neuen Ansatz vor: Sie bringt Computern bei, verborgene Muster in Mikroskopbildern von Tumoren zu erkennen und diese mit der Frage zu verknüpfen, wie Tumorzellen über Leben und Tod entscheiden. Auf diese Weise wollen die Forschenden Patientinnen genauer in höher- und niedrigrisiko-Gruppen einteilen als mit den aktuellen Methoden und zugleich Schwachstellen aufdecken, die neue Therapien anvisieren könnten.
Tiefer blicken in Tumoraufnahmen
Pathologen beurteilen Krebs traditionell, indem sie gefärbte Gewebeschnitte unter dem Mikroskop betrachten und beschreiben, was sie sehen. Zwar ist dieses Verfahren leistungsfähig, es ist aber auch subjektiv und erfasst subtile Details oft nicht zuverlässig. Das Team dieser Studie nutzte digitale „Whole-Slide“-Bilder von Ovarialtumoren und zerteilte jedes große Bild in viele kleinere Kacheln. Ein Deep-Learning-System namens ResNet50 durchsuchte diese Kacheln und extrahierte Tausende mathematischer Merkmale, die Muster in Zellform, Textur und der Anordnung von Zellen und Stützgewebe beschreiben. Parallel dazu quantifizierte spezialisierte Software klassischere Bildmerkmale wie Kerngröße und Gewebestruktur, um ein detailliertes Bild des Erscheinungsbilds jedes Tumors zu erstellen. 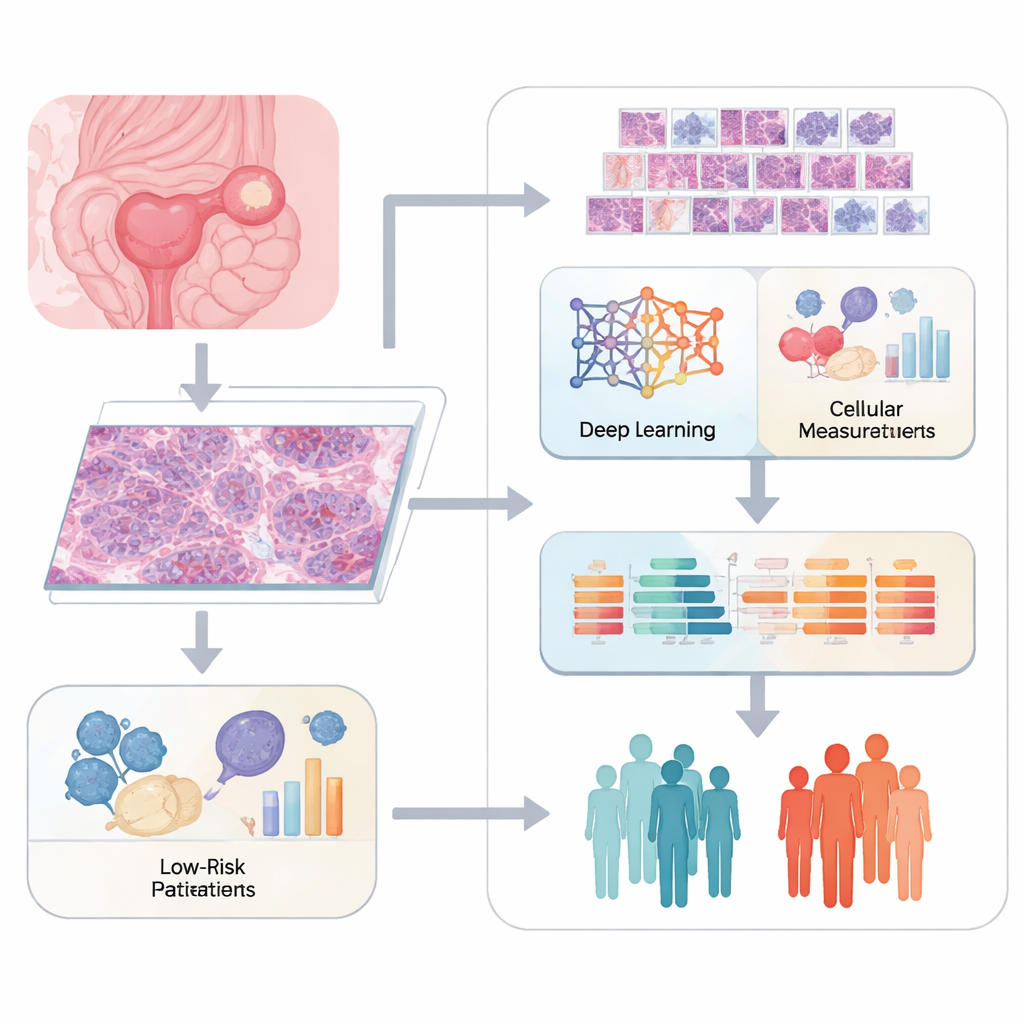
Bilder mit Todes-Signalen der Zellen verknüpfen
Anstatt bei der äußeren Erscheinung des Tumors stehen zu bleiben, verbanden die Forschenden diese Bildmerkmale mit einem lebensentscheidenden Schalter in der Zelle, der als mitochondriale Apoptose bekannt ist. Dieser Prozess wird von einer Proteinfamilie gesteuert, die eine geschädigte Zelle entweder zur Selbstzerstörung drängt oder ihr hilft, dem Tod zu widerstehen — ein zentraler Grund, warum manche Tumoren Chemotherapien trotzen. Mithilfe von Genexpressionsdaten aus Hunderten Ovarialkarzinom-Proben bewertete das Team, wie stark der mitochondriale Todesweg bei jeder Patientin aktiviert war. Anschließend behielten sie nur jene Bildmerkmale bei, die eindeutig mit diesem Weg verknüpft waren, und bauten so eine „Pathomik“-Brücke zwischen Tumoroptik und interner Signalgebung.
Ein Risikoscore für Patientinnen
Aus den anfänglich tausenden Messgrößen reduzierten die Forschenden das Merkmalset mithilfe mehrerer Stufen statistischer Filterung und Machine-Learning-Verfahren auf zwölf Kernbildmerkmale, die die Überlebenszeit am besten vorhersagten. Diese Merkmale wurden zu einer einzigen Zahl kombiniert, einem Risikoscore, den sie MAR-PTL-Modell nennen. Anhand dieses Scores teilten sie Patientinnen in Hoch- und Niedrigrisikogruppen ein. Das Modell unterschied die Outcomes sowohl in einer Trainingsgruppe als auch in einer separaten Testgruppe korrekt und übertraf dabei standardmäßige klinische Kennwerte wie Krankheitsstadium und Alter. Anders gesagt: Die verborgenen visuellen Fingerabdrücke eines Tumors lieferten, einmal entschlüsselt, starke Hinweise auf die Zukunft einer Patientin.
Ein zentrales Überlebensprotein und seine Nachbarschaft
Bei genauerer Betrachtung hob die Studie ein Gen hervor, BCL2L2, als zentralen Akteur. Dieses Gen hilft, den mitochondrialen Zelltod zu blockieren, und höhere Expressionswerte waren mit schlechterem Überleben verbunden. Auffällig war, dass bestimmte Deep-Learning-Merkmale aus den Gewebebildern parallel zu BCL2L2 anstiegen oder abnahmen, was darauf hindeutet, dass der Computer „sehen“ konnte, wie diese molekulare Bremse des Zelltods die Tumorarchitektur verändert. Einzelzellanalysen, die Tausende einzelner Zellen getrennt betrachten, zeigten, dass BCL2L2-reiche Krebszellen einen charakteristischen energiebezogenen Stoffwechsel aufwiesen und intensiv mit benachbarten Stützzellen wie Fibroblasten und Gefäßauskleidungszellen kommunizierten. Diese Interaktionen schienen eine förderliche Nachbarschaft zu bilden, die Tumoren hilft, Stress zu widerstehen und sich auszubreiten. 
Was das für Patientinnen bedeuten könnte
In der Summe zeigt diese Arbeit, dass Mikroskopbilder weit mehr verraten, als man auf den ersten Blick sieht. Durch die Verschmelzung digitaler Pathologie mit dem Wissen darüber, wie Tumorzellen über Leben oder Tod entscheiden, bietet das MAR-PTL-Modell eine schärfere Methode, Ovarialkarzinom-Patientinnen mit dem höchsten Risiko zu identifizieren. Die Entdeckung von BCL2L2 als zentralem Knotenpunkt und seine engen Verbindungen sowohl zum Tumorstoffwechsel als auch zu den umgebenden Stützzellen weist auf neue Therapieideen hin — etwa Wirkstoffe, die diesen Überlebensschalter deaktivieren oder seine Kommunikation mit dem umliegenden Gewebe stören. Obwohl diese Befunde noch in prospektiven Studien und Laborexperimenten bestätigt werden müssen, ebnen sie den Weg zu stärker personalisierter Versorgung und letztlich besseren Chancen für Frauen, die mit dieser herausfordernden Krankheit konfrontiert sind.
Zitation: Qin, Lh., Huang, X., Yang, C. et al. Mitochondrial apoptosis gene-based pathomics for ovarian cancer prognosis. Sci Rep 16, 13231 (2026). https://doi.org/10.1038/s41598-026-40121-5
Schlüsselwörter: Eierstockkrebs, digitale Pathologie, Deep Learning, mitochondriale Apoptose, tumorales Mikroumfeld