Clear Sky Science · zh
用于转移性癌症精确免疫治疗的 AND 逻辑纳米颗粒
更聪明的癌症治疗:会判断何时启动的疗法
当今许多最有前途的癌症疗法通过动员免疫系统识别并消灭肿瘤而起作用。但这些强效药物也可能激发健康器官的炎症,引发严重副作用。本研究描述了一种“智能”纳米颗粒,其行为更像微小的逻辑电路而非简单的药物胶囊:只有在同时探测到两种侵袭性肿瘤的标志时才会启动强大的免疫通路。目标既简单又雄心勃勃——在尽量保护机体其他部位的前提下,打击广泛且难以治疗的转移灶。
为何把免疫随处激活会成为问题
转移性癌症,即肿瘤细胞播散到肺等远端器官,是导致大多数癌症死亡的原因。一个有吸引力的药物靶点是称为 STING 的细胞警报系统,它帮助免疫细胞感知危险并发动抗病毒和抗肿瘤防御。在合适的部位被激活时,STING 能唤醒沉睡的免疫反应,帮助 T 细胞攻击癌症。但如果触发得过于广泛或过于强烈,可能会使免疫细胞疲惫甚至死亡,并引发健康组织炎症。早期用于临床试验的小分子 STING 激动剂带来了有限的益处但显著的副作用,部分原因是它们对作用地点和细胞类型缺乏精确控制。
为肿瘤信号构建微小的 AND 门
为了解决这个问题,研究人员设计了像电子 AND 逻辑门一样工作的纳米颗粒:仅当同时存在两种独立的肿瘤条件时,才释放其激活 STING 的货物。颗粒由一种对 pH 敏感的聚合物制成,可在血液中性环境下组装为稳定的胶束——纳米级球体。小分子 STING 激动剂通过一种在低氧条件下可断裂的连接子化学地连接到该聚合物上。许多实体肿瘤,尤其是转移性“免疫冷”肿瘤,比正常组织同时更酸性且更缺氧。只有在这种联合条件下,颗粒才会解体并释放其药物载荷。试管实验验证了 AND 门的完整真值表:在无酸性、无缺氧或仅有其中一项的情况下,几乎没有药物释放;当两者同时存在时,释放迅速且几乎完全。 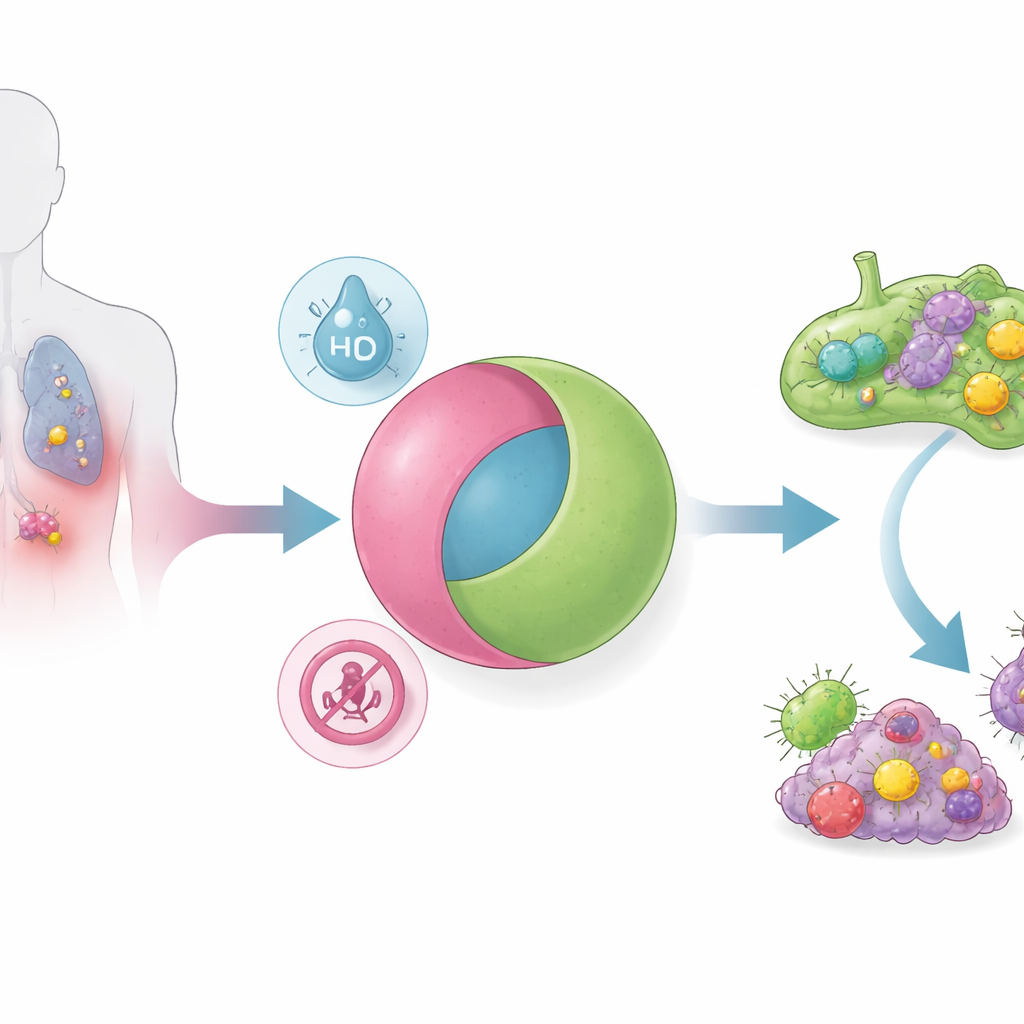
将火花引导到正确的免疫细胞
在小鼠体内,这些 AND 门控颗粒循环数小时而不聚集,并倾向性地积聚在脾脏、淋巴结和肺转移灶中。流式细胞术分析表明,它们主要被关键免疫哨兵细胞——树突状细胞和巨噬细胞吞噬,而不是被 T 细胞或癌细胞本身摄取。在缺氧条件下,树突状细胞自然提高一种可剪断氧敏连接子的酶的水平,进一步增强了对肿瘤的偏向性反应。一旦在这些细胞内被激活,颗粒会驱动强烈的干扰素-β 和其他警报信号的产生,但只有在局部环境既酸性又缺氧时才会发生,从而有助于将 STING 激活局限于病变组织。
从逻辑门到小鼠中的肿瘤控制
随后,作者在几种侵袭性小鼠癌症模型中测试了他们的主要配方,称为 PHM 纳米颗粒,包括来自 Lewis 肺癌的小鼠肺转移、三阴性乳腺癌和黑色素瘤。单次静脉注射显著降低了可见肺肿瘤结节的数量,相较于游离药物或仅对单一刺激响应的颗粒,效果更好。在同时监测肝肾损伤标志物和炎性细胞因子的对比实验中,AND 门设计在强效肿瘤控制与低系统毒性之间提供了最佳平衡。详细的免疫研究揭示了原因:这种治疗依赖于完整的 STING 通路、一种专门的树突状细胞亚群(cDC1)以及杀伤性 CD8 T 细胞。在被治疗的肿瘤中,这些树突状细胞显示出高水平的激活 STING,并且常常与成簇的 CD8 T 细胞直接接触,而这些 CD8 细胞已获得强大的肿瘤杀伤和记忆特征。 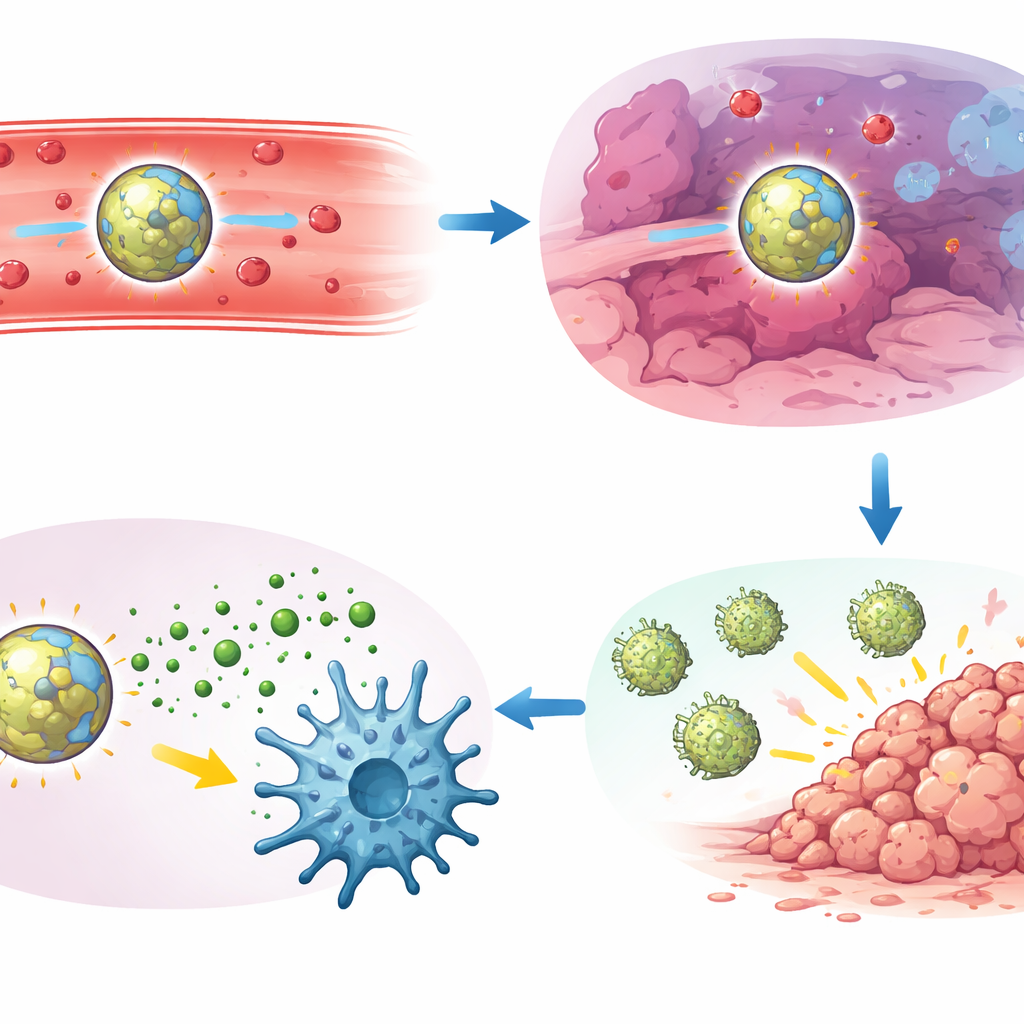
持久保护与与其他疗法的协同
除了缩小已有的转移灶外,纳米颗粒还帮助训练免疫系统以获得长期保护。存活于初次治疗的小鼠在随后再次接种相同癌细胞时表现出抵抗力,表明存在持久的免疫记忆。在黑色素瘤模型中,将这些颗粒与免疫检查点抑制剂联合使用进一步延长了生存期,提示精确的 STING 激活可与现有免疫疗法协同。在一个严酷的乳腺癌模型中,单独使用这些颗粒显著减少了转移并改善了生存,尽管与检查点抑制联合并未带来额外收益,表明最佳组合可能取决于肿瘤类型。
这对未来癌症护理可能意味着什么
对非专业读者而言,关键讯息是这项工作将一个强大但粗糙的免疫开关变得更有分辨力。通过构建一个在分子层面监听酸性和低氧这两种信号的 AND 门——这些条件在危险肿瘤中常见但在大多数健康组织中罕见——作者创建了一种可以巡逻全身但主要在转移灶聚集并点燃强烈免疫活性的纳米颗粒。尽管仍处于动物研究阶段,这一策略有望使未来的癌症免疫疗法在更安全的同时更有效,并且相同的基于逻辑的设计可以拓展到癌症之外的其他药物与疾病信号上。
引用: Ye, S., Chen, S., Basava, V. et al. AND logic nanoparticle for precision immunotherapy of metastatic cancers. Nat. Nanotechnol. 21, 606–616 (2026). https://doi.org/10.1038/s41565-026-02130-3
关键词: 癌症免疫治疗, 纳米颗粒, STING 通路, 肿瘤微环境, 转移