Clear Sky Science · pl
Nanocząsteczka typu AND dla precyzyjnej immunoterapii przerzutowych nowotworów
Inteligentniejsze terapie przeciwnowotworowe, które wiedzą, kiedy się włączyć
Wiele z dziś najbardziej obiecujących terapii przeciwnowotworowych działa przez pobudzenie układu odpornościowego do rozpoznania i zniszczenia guza. Jednak te silne leki mogą też zapalać zdrowe organy, powodując poważne skutki uboczne. W badaniu opisano „inteligentną” nanocząsteczkę, która zachowuje się bardziej jak maleńki obwód logiczny niż zwykła kapsułka leku: aktywuje silny szlak immunologiczny tylko wtedy, gdy jednocześnie wykryje dwa znaki rozpoznawcze agresywnych nowotworów. Cel jest prosty, ale ambitny — zaatakować rozległe, trudne do leczenia przerzuty, oszczędzając przy tym resztę organizmu.
Dlaczego uruchamianie odporności wszędzie jest problemem
Nowotwór przerzutowy, w którym komórki nowotworowe zasiewają odległe narządy, takie jak płuca, odpowiada za zdecydowaną większość zgonów z powodu raka. Atrakcyjnym celem dla nowych leków jest komórkowy system alarmowy znany jako szlak STING, który pomaga komórkom odpornościowym wyczuwać zagrożenie i uruchamiać obronę przeciwwirusową i przeciwnowotworową. Gdy zostanie włączony we właściwym miejscu, STING może pobudzić uśpione odpowiedzi odpornościowe i pomóc limfocytom T atakować nowotwór. Jednak gdy jest aktywowany zbyt szeroko lub zbyt silnie, może prowadzić do wyczerpania lub nawet śmierci komórek odpornościowych oraz zapalenia zdrowych tkanek. Wcześniejsze małocząsteczkowe stymulatory STING w próbach klinicznych dały umiarkowane korzyści, ale znaczące skutki uboczne, częściowo dlatego, że brakowało im precyzyjnej kontroli miejsca i rodzaju komórek, w których działały.
Budowa maleńkiej bramki AND dla sygnałów nowotworowych
Aby to rozwiązać, badacze zaprojektowali nanocząsteczki działające jak elektroniczna bramka logiczna AND: uwalniają swoją aktywującą STING zawartość tylko wtedy, gdy jednocześnie wystąpią dwa oddzielne warunki nowotworowe. Cząsteczki są wykonane z polimeru wrażliwego na pH, który samoorganizuje się w micele — nanometrowe kule stabilne w obojętnym środowisku krwi. Małocząsteczkowy agonista STING jest chemicznie przywiązany do tego polimeru przez łącznik, który ulega rozkładowi w warunkach niskiego natlenowania. Wiele guzów litych, zwłaszcza przerzutowych „zimnych immunologicznie”, jest jednocześnie bardziej kwaśnych i bardziej hipoksycznych niż tkanki prawidłowe. Tylko w tym połączonym środowisku cząsteczka rozpada się i uwalnia ładunek leku. Doświadczenia in vitro potwierdziły pełną tabelę prawdy bramki AND: bez kwaśności, bez hipoksji lub przy obecności tylko jednego z tych warunków wydzielanie leku było praktycznie zerowe; przy obu warunkach uwalnianie było szybkie i niemal kompletne. 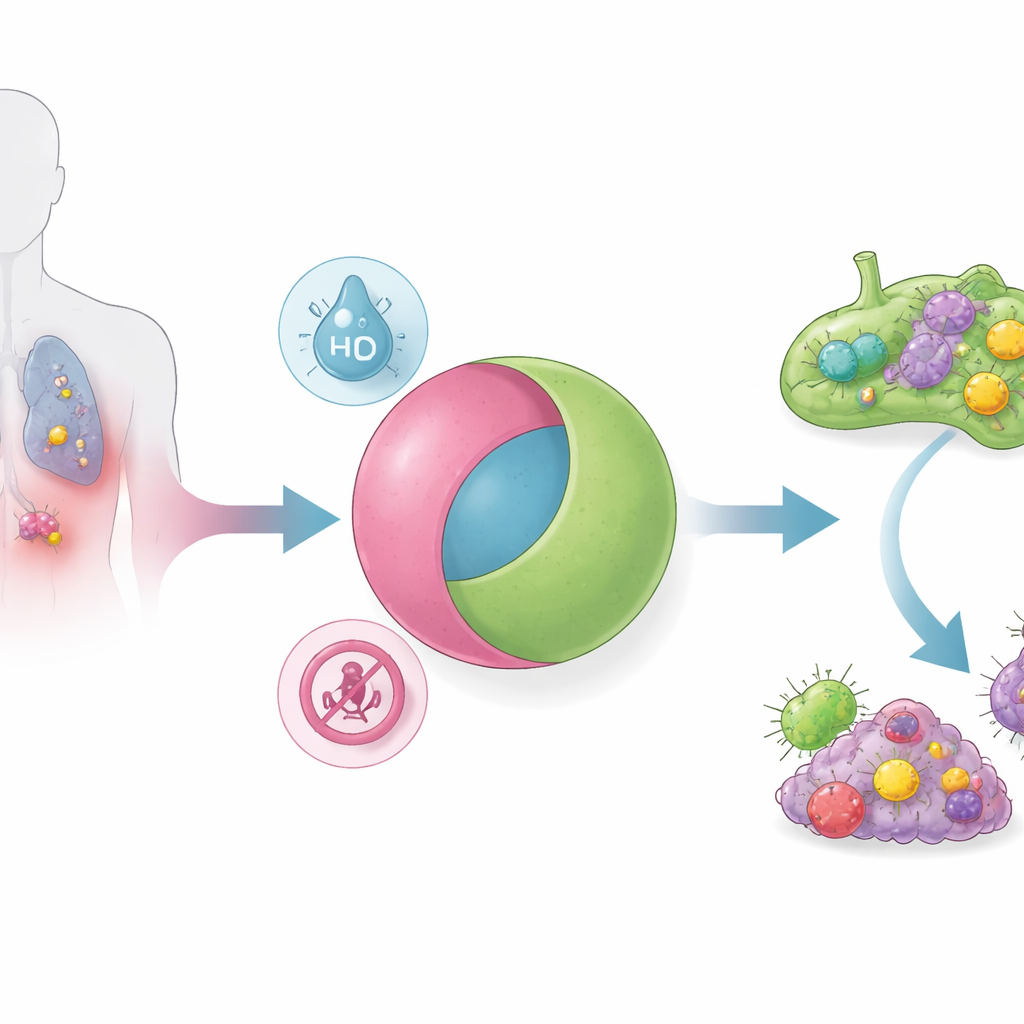
Kierowanie iskry do właściwych komórek odpornościowych
U myszy te cząsteczki z bramką AND krążyły przez godziny bez agregacji i preferencyjnie akumulowały się w śledzionie, węzłach chłonnych i przerzutach płucnych. Analizy cytometrii przepływowej wykazały, że były głównie pobierane przez kluczowe komórki strażnicze układu odpornościowego — komórki dendrytyczne i makrofagi — a nie przez limfocyty T ani same komórki nowotworowe. W warunkach hipoksji komórki dendrytyczne naturalnie podnosiły poziom enzymu, który przecina łącznik wrażliwy na tlen, co dodatkowo zaostrzało odpowiedź ukierunkowaną na guz. Po aktywacji wewnątrz tych komórek cząsteczki indukowały silną produkcję interferonu-β i innych sygnałów alarmowych, ale tylko gdy lokalne środowisko było jednocześnie kwaśne i ubogie w tlen, co pomagało ograniczyć aktywację STING do tkanek chorych.
Od bramki logicznej do kontroli guza u myszy
Autorzy przetestowali następnie swoją wiodącą formulację, nazwaną nanocząsteczkami PHM, w kilku agresywnych modelach nowotworowych u myszy, w tym przerzutach płucnych pochodzących z raka płuca Lewisa, trójnuległego raka piersi i czerniaka. Pojedyncza dawka dożylna znacznie zmniejszyła liczbę widocznych guzków nowotworowych w płucach w porównaniu z wolnym lekiem lub z cząsteczkami reagującymi tylko na jeden bodziec. W porównaniach bezpośrednich, które monitorowały także markery uszkodzenia wątroby i nerek oraz cytokiny zapalne, konstrukcja z bramką AND zapewniła najlepszą równowagę silnej kontroli guza i niskiej toksyczności systemowej. Szczegółowe badania immunologiczne wyjaśniły dlaczego: leczenie opierało się na nienaruszonym szlaku STING, na wyspecjalizowanej podgrupie komórek dendrytycznych (cDC1) oraz na cytotoksycznych limfocytach CD8. W leczonych guzach te komórki dendrytyczne wykazywały wysokie poziomy aktywowanego STING i często obserwowano je w bezpośrednim kontakcie z klastrami komórek CD8, które nabyły silne cechy zabijania nowotworu i pamięci immunologicznej. 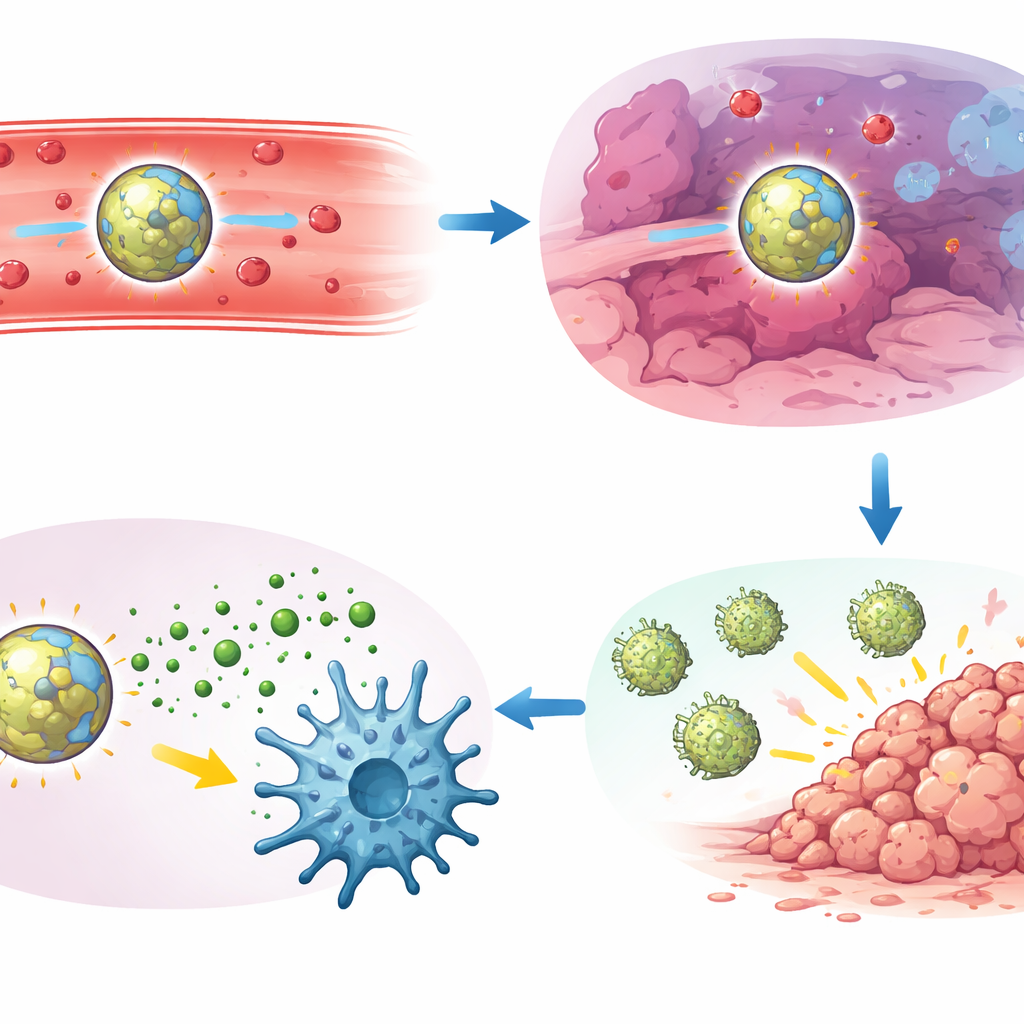
Trwała ochrona i współpraca z innymi terapiami
Ponad zmniejszaniem istniejących przerzutów, nanocząsteczki pomogły wyszkolić układ odpornościowy na dłuższą metę. Myszy, które przeżyły początkowe leczenie, były odporne na późniejsze ponowne wyzwanie tymi samymi komórkami nowotworowymi, co wskazuje na trwałą pamięć immunologiczną. W modelach czerniaka łączenie cząsteczek z inhibitorem punktów kontrolnych immunologicznych dodatkowo wydłużało przeżycie, sugerując, że precyzyjna aktywacja STING może współdziałać z istniejącymi immunoterapiami. W surowym modelu raka piersi same cząsteczki znacząco zmniejszały przerzuty i poprawiały przeżywalność, choć ich połączenie z blokadą punktów kontrolnych nie przyniosło dodatkowej korzyści, co podkreśla, że optymalne połączenia terapeutyczne mogą zależeć od typu guza.
Co to może znaczyć dla przyszłej opieki onkologicznej
Dla osób niebędących specjalistami kluczowa myśl jest taka, że ta praca zamienia potężny, lecz tępy wyłącznik odpornościowy w coś bardziej dyskryminującego. Budując molekularną bramkę AND, która nasłuchuje jednocześnie kwaśności i niskiego poziomu tlenu — warunków powszechnych w niebezpiecznych guzach, ale rzadkich w większości zdrowych tkanek — autorzy stworzyli nanocząsteczkę, która może patrolować cały organizm, a jednak zapalać silną aktywność immunologiczną głównie tam, gdzie czyhają przerzuty. Choć nadal jest to etap badań na zwierzętach, ta strategia może przyczynić się do uczynienia przyszłych immunoterapii przeciwnowotworowych bezpieczniejszymi i bardziej skutecznymi, a ten oparty na logice projekt można dostosować do innych leków i sygnałów chorobowych wykraczających poza raka.
Cytowanie: Ye, S., Chen, S., Basava, V. et al. AND logic nanoparticle for precision immunotherapy of metastatic cancers. Nat. Nanotechnol. 21, 606–616 (2026). https://doi.org/10.1038/s41565-026-02130-3
Słowa kluczowe: immunoterapia nowotworów, nanocząsteczki, szlak STING, mikrośrodowisko guza, przerzuty