Clear Sky Science · de
AND‑Logik‑Nanopartikel für präzise Immuntherapie metastasierter Krebserkrankungen
Intelligentere Krebsbehandlungen, die wissen, wann sie aktiv werden sollen
Viele der vielversprechendsten Krebsbehandlungen mobilisieren das Immunsystem, damit es Tumoren erkennt und zerstört. Diese starken Wirkstoffe können jedoch auch gesunde Organe entzünden und schwerwiegende Nebenwirkungen auslösen. Die vorliegende Studie beschreibt ein „intelligentes“ Nanopartikel, das eher wie eine winzige Logikschaltung als wie eine einfache Medikamentenkapsel funktioniert: Es schaltet einen wirkstarken Immunweg nur dann ein, wenn es gleichzeitig zwei Kennzeichen aggressiver Tumoren erkennt. Das Ziel ist einfach, aber ehrgeizig – weitverbreitete, schwer behandelbare Metastasen anzugreifen und zugleich den Rest des Körpers zu schonen.
Warum eine flächendeckende Immunaktivierung problematisch ist
Metastasierender Krebs, bei dem Tumorzellen in entfernte Organe wie die Lunge aussäen, verursacht die überwiegende Mehrheit der Krebstodesfälle. Ein attraktives Ziel für neue Wirkstoffe ist ein zelluläres Alarmsystem, das als STING‑Signalweg bekannt ist und Immunzellen hilft, Gefahr zu erkennen und antivirale sowie antitumorale Abwehrreaktionen zu starten. Wird STING am richtigen Ort aktiviert, kann es ruhende Immunantworten rekrutieren und T‑Zellen beim Angriff auf Krebs unterstützen. Wird es jedoch zu breit oder zu stark ausgelöst, kann es Immunzellen erschöpfen oder sogar schädigen und gesunde Gewebe entzünden. Frühere kleine STING‑Stimulanzien in klinischen Studien zeigten nur moderate Vorteile bei deutlich spürbaren Nebenwirkungen – zum Teil, weil sie nicht präzise steuern konnten, wo und in welchen Zellen sie wirken.
Eine winzige AND‑Schaltung für Tumorsignale bauen
Um dieses Problem zu lösen, entwarfen die Forscher Nanopartikel, die wie ein elektronisches AND‑Gatter arbeiten: Sie setzen ihre STING‑aktivierende Fracht nur frei, wenn gleichzeitig zwei verschiedene Tumorbedingungen vorliegen. Die Partikel bestehen aus einem pH‑empfindlichen Polymer, das sich zu Mizellen zusammenlagert – nanoskalige Kugeln, die im neutralen Milieu des Blutkreislaufs stabil sind. Ein kleiner STING‑Agonist ist chemisch an dieses Polymer über eine Bindung gekoppelt, die unter sauerstoffarmen Bedingungen gespalten wird. Viele solide Tumoren, insbesondere metastasierende „immun‑kalte“ Tumore, sind zugleich saurer und hypoxischer als normales Gewebe. Nur in diesem kombinierten Umfeld zerfällt das Partikel und gibt seine Wirkstoffladung frei. Im Reagenzglas bestätigten Experimente die vollständige Wahrheitstabelle eines AND‑Gatters: Ohne Säure, ohne Hypoxie oder mit nur einem der beiden Reize wurde kaum Wirkstoff freigesetzt; bei beiden Reizen wurde die Freisetzung schnell und nahezu vollständig. 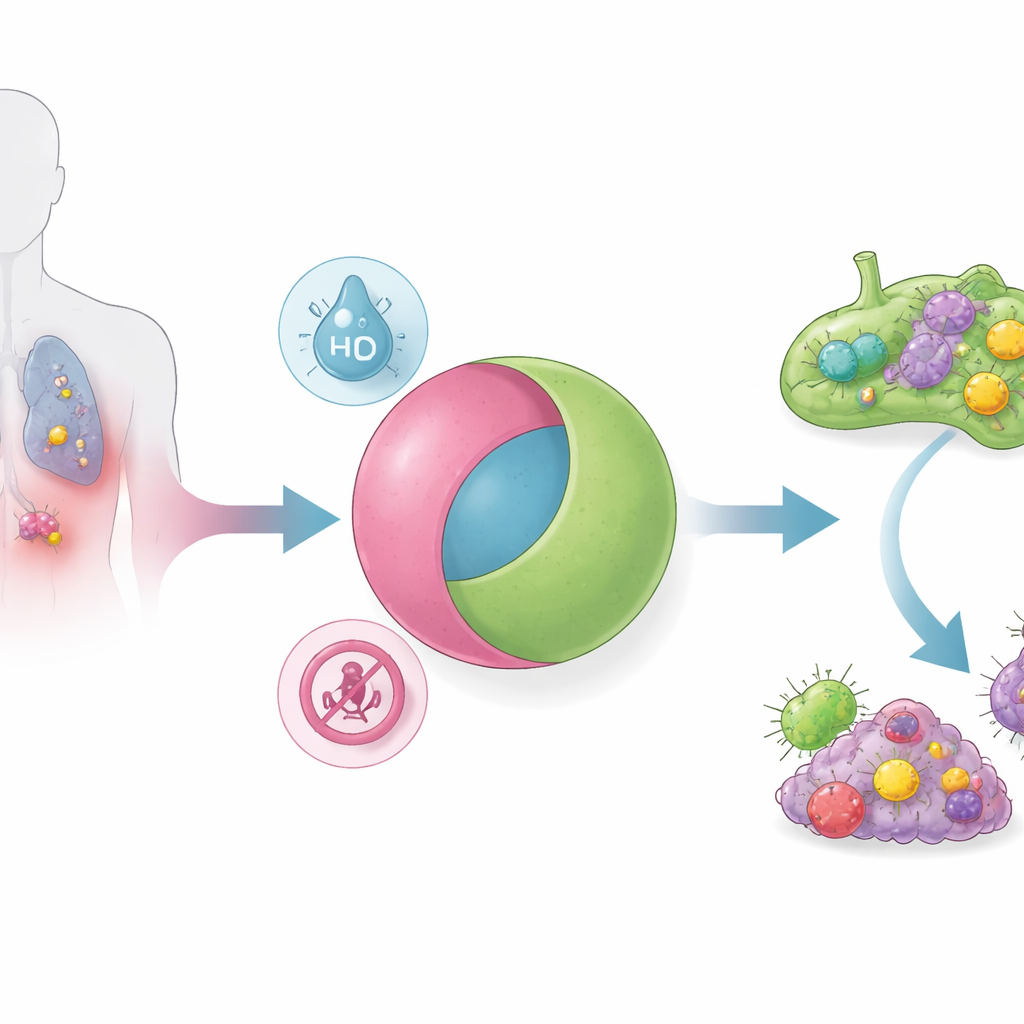
Den Funken an die richtigen Immunzellen richten
In Mäusen zirkulierten diese AND‑geschalteten Partikel stundenlang ohne Aggregate zu bilden und reichern sich bevorzugt in Milz, Lymphknoten und Lungenmetastasen an. Durchflusszytometrie zeigte, dass sie hauptsächlich von wichtigen Immunwächtern – dendritischen Zellen und Makrophagen – aufgenommen wurden, nicht primär von T‑Zellen oder den Krebszellen selbst. Unter hypoxischen Bedingungen erhöhten dendritische Zellen natürlicherweise die Menge eines Enzyms, das die sauerstoffempfindliche Bindung zerschneidet und so die tumorselektive Reaktion weiter schärft. Einmal in diesen Zellen aktiviert, lösten die Partikel eine starke Produktion von Interferon‑β und anderen Alarmsignalen aus, jedoch nur wenn die lokale Umgebung sowohl sauer als auch sauerstoffarm war, was dazu beitrug, die STING‑Aktivierung auf erkrankte Gewebe zu begrenzen.
Von der Logikschaltung zur Tumorkontrolle in Mäusen
Die Autoren testeten anschließend ihre führende Formulierung, genannt PHM‑Nanopartikel, in mehreren aggressiven Mauskrebsmodellen, darunter Lungenmetastasen eines Lewis‑Lungenkarzinoms, dreifach negativer Brustkrebs und Melanom. Eine einzelne intravenöse Dosis verringerte die Zahl sichtbarer Lungentumorknoten deutlich im Vergleich zu freiem Wirkstoff oder zu Partikeln, die nur auf einen Stimulus reagierten. In direkten Vergleichen, bei denen auch Leber‑ und Nieren‑Schädigungsmarker sowie entzündliche Zytokine verfolgt wurden, bot das AND‑geschaltete Design die beste Balance aus starker Tumorkontrolle und geringer systemischer Toxizität. Detaillierte Immununtersuchungen erklärten warum: Die Wirkung beruhte auf einem intakten STING‑Signalweg, einer speziellen Untergruppe dendritischer Zellen (cDC1) und auf zytotoxischen CD8‑T‑Zellen. In behandelten Tumoren zeigten diese dendritischen Zellen hohe Werte aktivierten STING und waren häufig in direktem Kontakt mit Clustern von CD8‑T‑Zellen zu sehen, die potente tumortötende und Gedächtnis‑Eigenschaften erworben hatten. 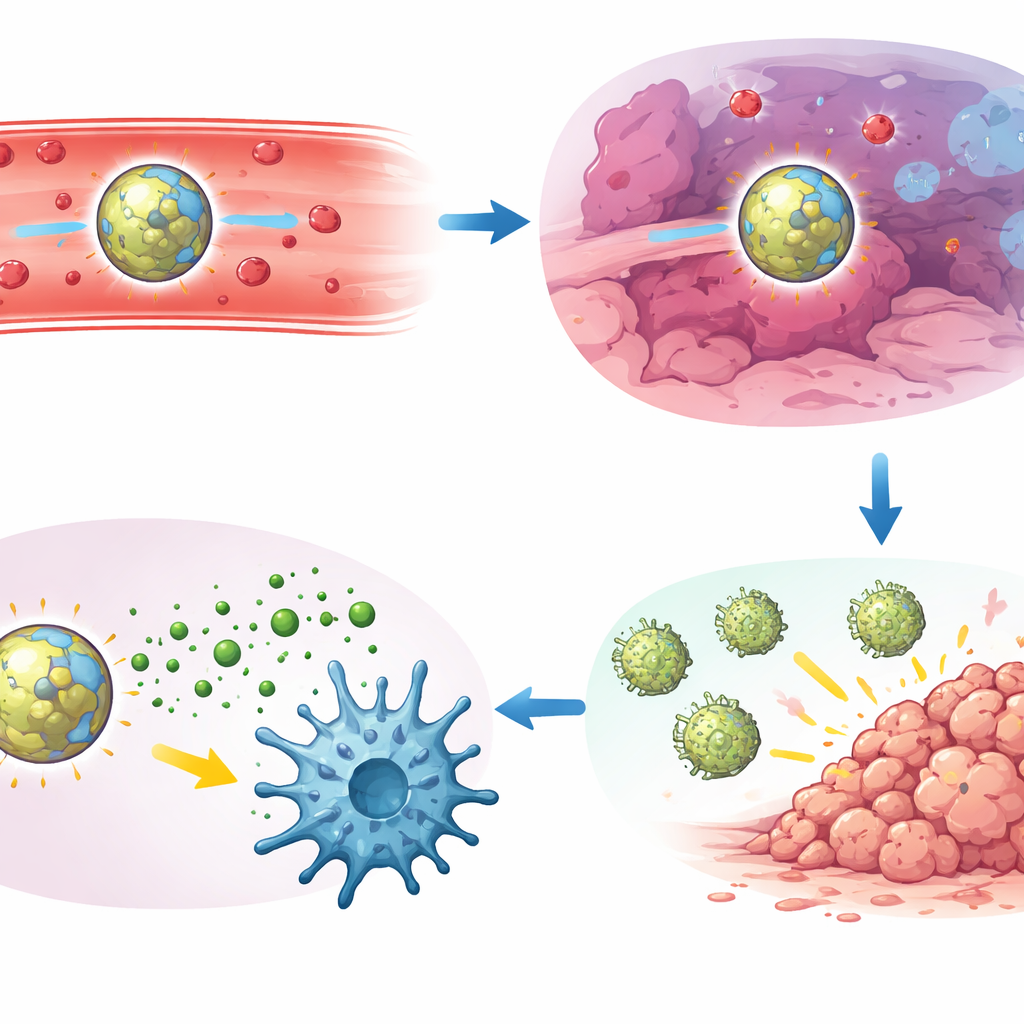
Dauerhafter Schutz und Partnerschaft mit anderen Therapien
Über die Verkleinerung bestehender Metastasen hinaus halfen die Nanopartikel, das Immunsystem langfristig zu schulen. Mäuse, die die Erstbehandlung überlebten, widersetzten sich einer späteren erneuten Herausforderung mit denselben Krebszellen, was auf ein langlebiges immunologisches Gedächtnis hinweist. In Melanommodellen verlängerte die Kombination der Partikel mit einem Checkpoint‑Inhibitor das Überleben weiter, was nahelegt, dass präzise STING‑Aktivierung mit bestehenden Immuntherapien synergieren kann. In einem aggressiven Brustkrebsmodell reduzierten die Partikel allein die Metastasen deutlich und verbesserten das Überleben, obwohl die Kombination mit Checkpoint‑Blockade keinen zusätzlichen Vorteil brachte – ein Hinweis darauf, dass optimale Kombinationen vom Tumortyp abhängen können.
Was das für die zukünftige Krebsversorgung bedeuten könnte
Für den Nicht‑Spezialisten ist die Kernbotschaft: Diese Arbeit verwandelt einen mächtigen, aber unscharfen Immun‑Schalter in etwas Differenzierteres. Indem sie ein molekulares AND‑Gatter bauen, das sowohl auf Säure als auch auf niedrigen Sauerstoffgehalt hört – Bedingungen, die in gefährlichen Tumoren häufig, in den meisten gesunden Geweben jedoch selten sind – erzeugten die Autoren ein Nanopartikel, das den ganzen Körper patrouillieren kann, aber starke Immunaktivität vornehmlich dort entflammt, wo Metastasen lauern. Obwohl sich die Strategie noch im Tiermodellstadium befindet, könnte sie dazu beitragen, künftige Krebsimmuntherapien sicherer und wirkungsvoller zu machen; dieselbe logikbasierte Konstruktion ließe sich auch auf andere Wirkstoffe und Krankheitssignale außerhalb des Krebses anpassen.
Zitation: Ye, S., Chen, S., Basava, V. et al. AND logic nanoparticle for precision immunotherapy of metastatic cancers. Nat. Nanotechnol. 21, 606–616 (2026). https://doi.org/10.1038/s41565-026-02130-3
Schlüsselwörter: Krebsimmuntherapie, Nanopartikel, STING‑Signalweg, tumormikroumgebung, Metastase