Clear Sky Science · ja
転移がんの精密免疫療法のためのAND論理ナノ粒子
どこで作動するかを知る、より賢いがん治療
今日最も有望ながん治療の多くは、免疫系を動員して腫瘍を認識し除去させることによって働きます。しかし、強力な薬剤は健常な臓器にも炎症を引き起こし、深刻な副作用を招くことがあります。本研究は「スマート」なナノ粒子を記述しており、単なる薬物カプセルというよりは小さな論理回路のように振る舞います。攻撃的な腫瘍の特徴が二つ同時に検出されたときだけ強力な免疫経路を作動させます。目標は単純かつ野心的です――全身に広がり治療困難な転移を攻撃しつつ、体の残りの部分を守ること。
免疫をどこでも起動するのが問題となる理由
肺のような遠隔臓器に腫瘍細胞が播種する転移性がんは、がん死亡の大部分を引き起こします。新規薬剤の有望な標的の一つはSTING経路として知られる細胞の警報システムで、免疫細胞が危険を感知して抗ウイルス・抗腫瘍の防御を開始するのを助けます。適切な場所で作動すればSTINGは休止状態の免疫応答を呼び覚まし、T細胞によるがん攻撃を助けます。しかし、あまりに広範囲または強力に誘導されると免疫細胞を疲弊させたり死に至らせたりし、健常組織に炎症を引き起こす可能性があります。臨床試験に入った初期の低分子STING賦活剤は限定的な利益とかなりの副作用を示しましたが、その一因はどこで、どの細胞で作用するかの精密な制御が欠如していたことにあります。
腫瘍シグナルのための小さなANDゲートの構築
これを解決するため、研究者らは電子的なAND論理ゲートのように動作するナノ粒子を設計しました。これらは二つの別個の腫瘍条件が同時に存在する場合にのみSTING賦活化物質を放出します。粒子はpH感受性ポリマーから作られ、血流の中性環境で安定するミセル(ナノサイズの球)として組み立てられます。小分子のSTINGアゴニストは、低酸素条件下で分解されるリンカーを介してこのポリマーに化学的に連結されています。多くの固形腫瘍、特に転移性の「免疫寒冷」腫瘍は、正常組織より同時に酸性で低酸素です。この組み合わせの環境でのみ粒子は分解し薬剤を放出します。試験管内実験はANDゲートの完全な真理値表を確認しました:酸性がなければ、低酸素がなければ、または二つのうち一方しかない場合はほとんど薬剤は放出されず、両方が揃うと放出は迅速かつほぼ完全になりました。 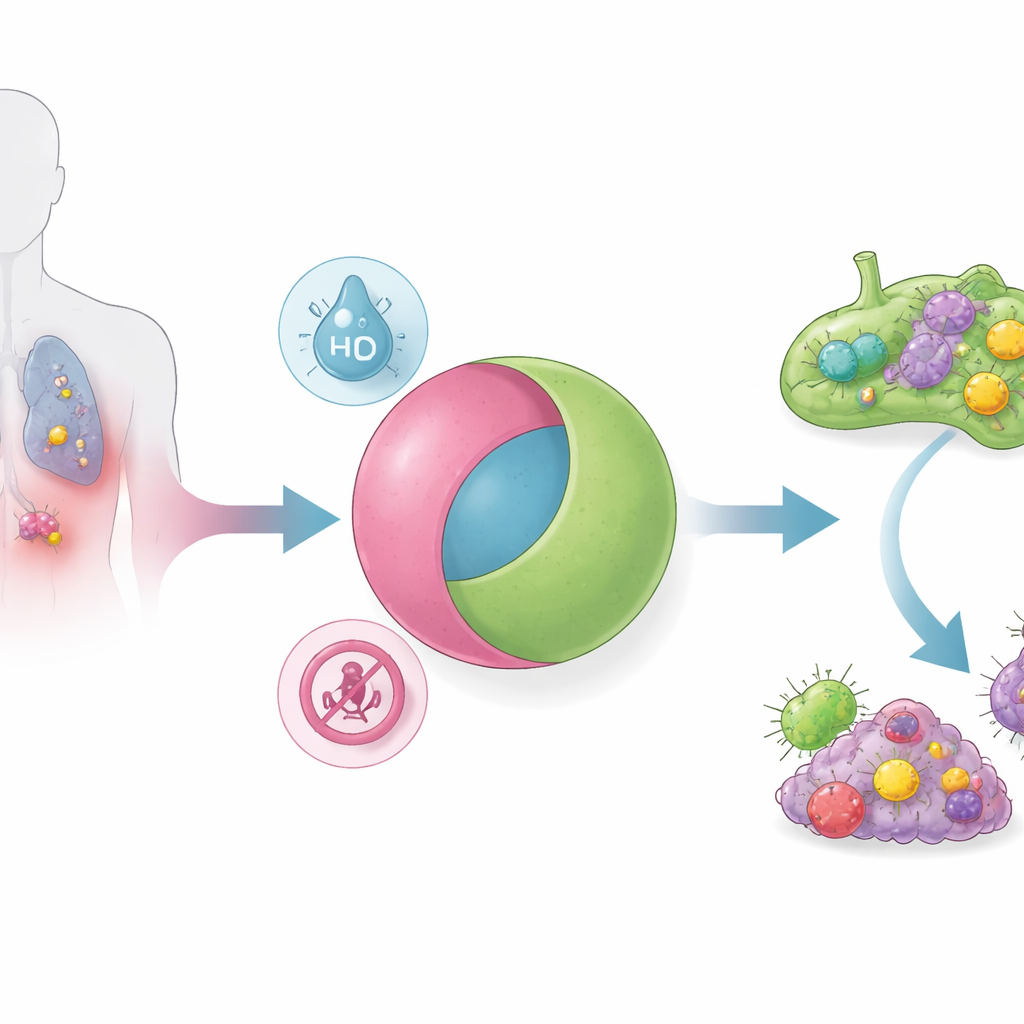
発火を正しい免疫細胞へ導く
マウスでは、これらのANDゲート粒子は数時間にわたり凝集せず循環し、脾臓、リンパ節、肺転移に優先的に蓄積しました。フローサイトメトリー解析は、それらが主に樹状細胞やマクロファージといった重要な免疫の哨戒細胞に取り込まれ、T細胞やがん細胞自身にはあまり取り込まれないことを示しました。低酸素条件下では、樹状細胞は酸素感受性リンカーを切断する酵素の発現を自然に上げ、腫瘍に偏った応答をさらに鋭くしました。これらの細胞内で活性化されると、粒子はインターフェロンβや他の警報シグナルの強力な産生を促しましたが、それは局所環境が酸性かつ低酸素である場合に限られ、STINGの活性化を病変組織に留めるのに役立ちました。
論理ゲートからマウスの腫瘍制御へ
著者らは次に主要な製剤(PHMナノ粒子と命名)をいくつかの攻撃的なマウスがんモデルで試験しました。モデルにはルイス肺がん由来の肺転移、トリプルネガティブ乳がん、メラノーマが含まれます。静脈内単回投与で、可視化できる肺腫瘍結節の数は遊離薬や一つの刺激にのみ応答する粒子と比べて大幅に減少しました。肝臓・腎臓の損傷マーカーや炎症性サイトカインも追跡した直接比較試験では、ANDゲート設計が強い腫瘍制御と低い全身毒性の最良のバランスを示しました。詳細な免疫学的解析はその理由を明らかにしました:治療効果はSTING経路の完全性、特殊な樹状細胞亜群(cDC1)、およびキラーCD8 T細胞に依存していました。治療を受けた腫瘍では、これらの樹状細胞は高レベルの活性化されたSTINGを示し、しばしば強力な腫瘍殺傷能と記憶特性を獲得したCD8 T細胞のクラスターと直接接触しているのが観察されました。 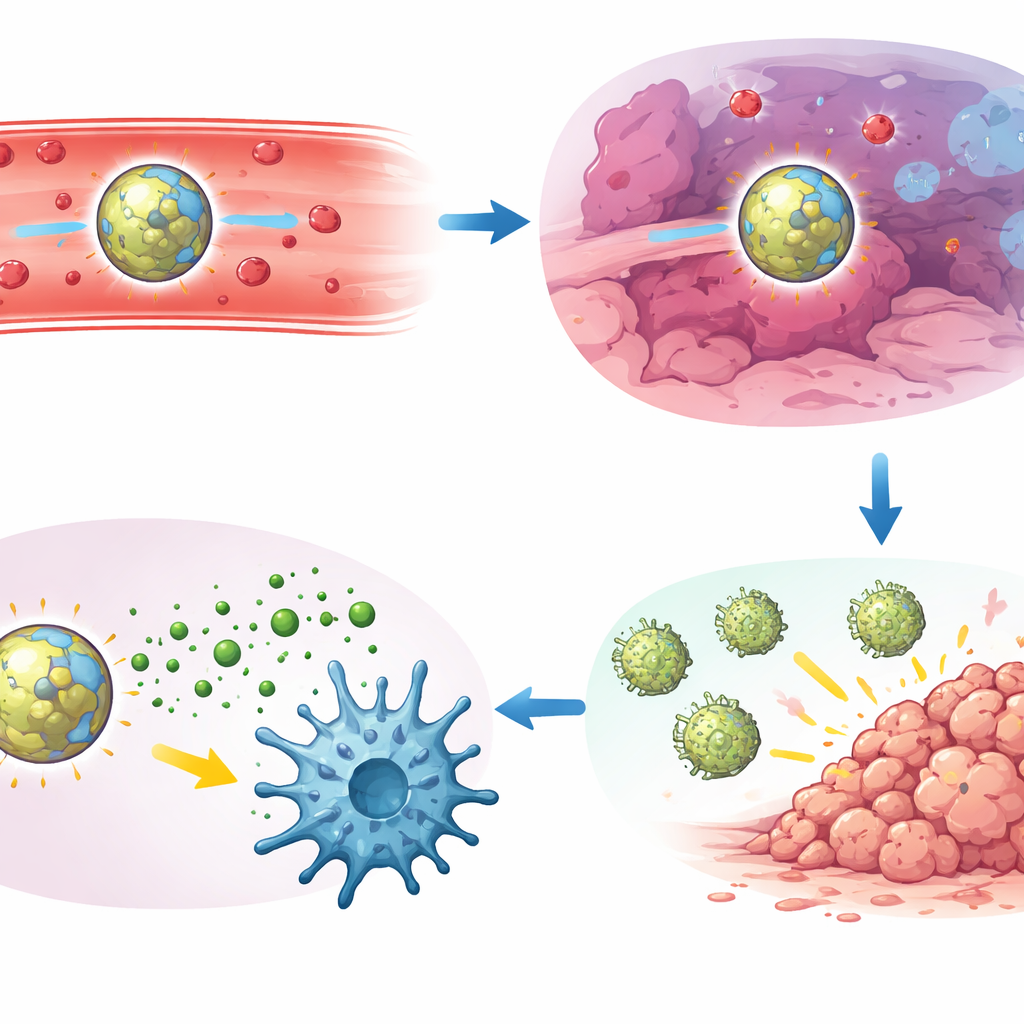
持続的な防御と他療法との連携
既存の転移縮小だけでなく、ナノ粒子は免疫系の長期的な訓練にも寄与しました。初期治療を生存したマウスは同じがん細胞での再チャレンジに抵抗でき、耐久性のある免疫記憶を示しました。メラノーマモデルでは、これらの粒子を免疫チェックポイント阻害剤と併用すると生存期間がさらに延長し、精密なSTING活性化が既存の免疫療法と相乗する可能性が示唆されました。厳しい乳がんモデルでは、粒子単独で転移を著しく減らし生存を改善しましたが、チェックポイント阻害との併用で追加の利得は得られず、最適な組み合わせは腫瘍タイプによって異なることを示しています。
将来のがんケアにとっての意義
専門外の読者にとって主要なメッセージは、この研究が強力だが粗雑な免疫スイッチをより識別力のあるものに変えているという点です。酸性と低酸素の両方を同時に検知する分子ANDゲートを構築することで――これらは危険な腫瘍には一般的だが多くの健常組織には稀な条件です――著者らは全身を巡回しつつも主に転移の潜む場所で強力な免疫活動を点火するナノ粒子を作り出しました。まだ動物実験段階にありますが、この戦略は将来のがん免疫療法をより安全かつ効果的にする助けになり得るとともに、同じ論理に基づく設計はがん以外の薬剤や疾患シグナルにも応用できる可能性があります。
引用: Ye, S., Chen, S., Basava, V. et al. AND logic nanoparticle for precision immunotherapy of metastatic cancers. Nat. Nanotechnol. 21, 606–616 (2026). https://doi.org/10.1038/s41565-026-02130-3
キーワード: がん免疫療法, ナノ粒子, STING経路, 腫瘍微小環境, 転移