Clear Sky Science · tr
Metastatik kanserlerin hassas immünoterapisi için AND mantığı nanopartikülü
Açılmayı Bilececek Daha Akıllı Kanser Tedavileri
Günümüzün en umut verici kanser tedavilerinin çoğu, bağışıklık sistemini tümörleri tanıyıp yok etmeye yönlendirerek çalışıyor. Ancak bu güçlü ilaçlar sağlıklı organlarda da iltihaplanmaya yol açarak ciddi yan etkilere neden olabiliyor. Bu çalışma, basit bir ilaç kapsülünden çok küçük bir mantık devresi gibi davranan “akıllı” bir nanopartikülü anlatıyor: agresif tümörlerin iki ayırt edici özelliğini aynı anda algıladığında güçlü bir bağışıklık yolunu ancak o zaman açıyor. Amaç basit ama iddialı—vücudun geri kalanını koruyarak, yaygın ve tedavisi zor metastazlara saldırmak.
Bağışıklığı Her Yerde Açmanın Neden Sorun Olduğu
Tümör hücrelerinin akciğer gibi uzak organlara yerleştiği metastatik kanser, kanser ölümlerinin büyük çoğunluğuna neden olur. Yeni ilaçlar için cazip hedeflerden biri, hücrelerin tehlikeyi algılayıp antiviral ve antitümör savunmaları başlatmasına yardımcı olan STING adı verilen hücresel alarm sistemidir. Doğru yerde aktive edildiğinde STING, uyuyan bağışıklık yanıtlarını uyandırabilir ve T hücrelerinin kansere saldırmasına yardımcı olabilir. Ancak çok yaygın veya çok güçlü tetiklendiğinde bağışıklık hücrelerini tüketebilir veya öldürebilir ve sağlıklı dokuları iltihaplandırabilir. Klinik denemelerdeki önceki küçük moleküllü STING uyarıcıları sınırlı yarar sağlarken önemli yan etkilere yol açtı; kısmen bunun nedeni hangi yerde ve hangi hücrelerde etki gösterecekleri üzerinde hassas kontrole sahip olmamalarıydı.
Tümör Sinyalleri İçin Küçük Bir AND Kapısı İnşa Etmek
Bunu çözmek için araştırmacılar elektronik bir AND mantık kapısı gibi çalışan nanopartiküller tasarladı: iki ayrı tümör koşulu aynı anda mevcutsa STING aktive edici yüklerini serbest bırakıyorlar. Parçacıklar, kan dolaşımının nötr ortamında kararlı olan misel hâline gelen pH-duyarlı bir polimerden yapılmıştır. Küçük moleküllü bir STING agonisti, oksijenin düşük olduğu koşullarda parçalanan bir bağlayıcı aracılığıyla bu polimere kimyasal olarak bağlanmıştır. Birçok solid tümör, özellikle metastatik “immün‑soğuk” olanlar, normal dokulardan hem daha asidik hem de daha hipoksiktir. Sadece bu birleşik ortamda parçacık çözünür ve ilaç yükünü salar. Deney tüpü çalışmaları bir AND kapısının tam doğruluk tablosunu doğruladı: asidite olmadan, hipoksi olmadan veya yalnızca iki koşuldan biri varsa neredeyse hiç ilaç salımı olmadı; her ikisi birlikteyken salım hızlı ve neredeyse tamamen gerçekleşti. 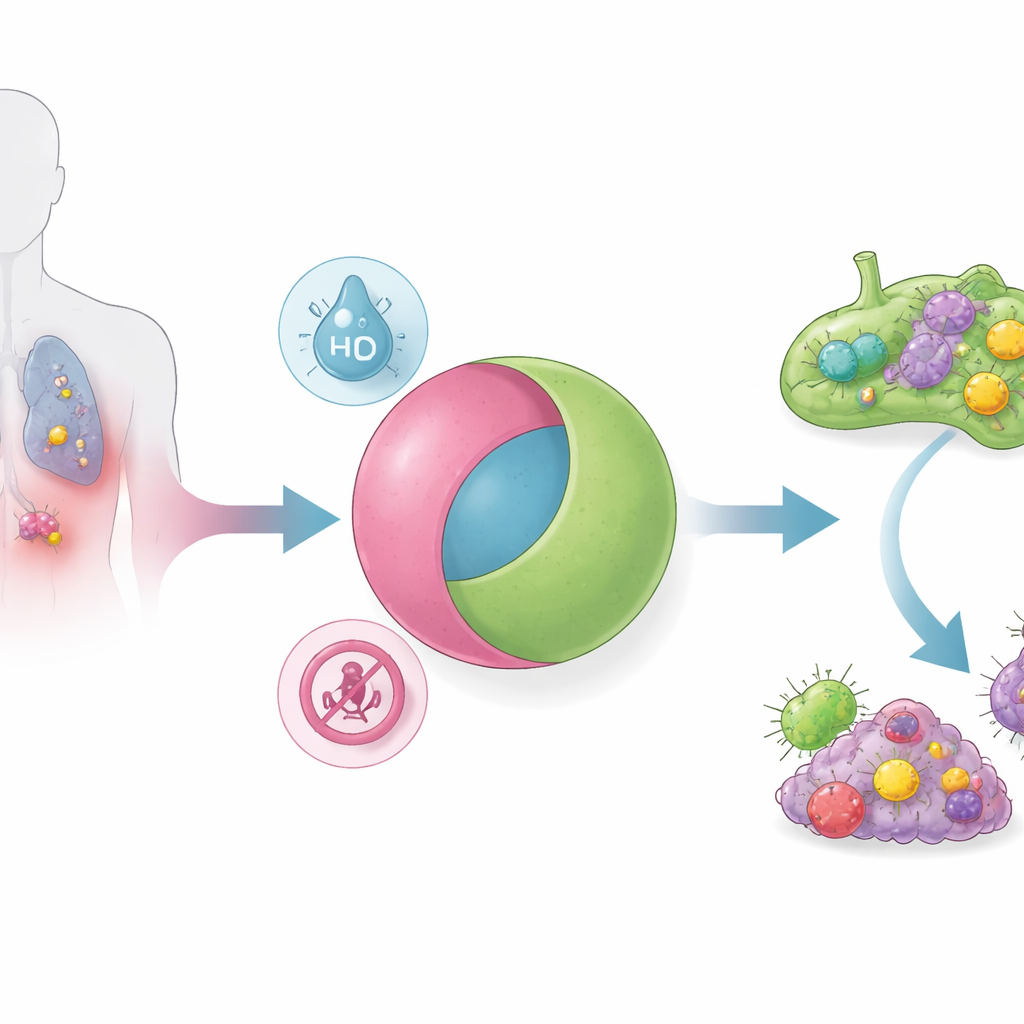
Kıvılcımı Doğru Bağışıklık Hücrelerine Yönlendirmek
Farelerde bu AND kapılı parçacıklar saatlerce kümelenmeden dolaştı ve dalak, lenf düğümleri ile akciğer metastazlarında tercihli olarak birikti. Akım sitometrisi analizleri, parçacıkların esas olarak T hücreleri veya tümör hücreleri yerine dendritik hücreler ve makrofajlar gibi ana bağışıklık nöbetçileri tarafından alındığını gösterdi. Hipoksik koşullar altında dendritik hücreler, oksijene duyarlı bağlayıcıyı kesen bir enzim seviyesini doğal olarak yükseltti ve bu da tümöre yönelimi daha da keskinleştirdi. Bu hücrelerin içinde aktive olduklarında parçacıklar güçlü interferon‑β ve diğer alarm sinyallerinin üretimini tetikledi, ancak sadece yerel ortam hem asidik hem de oksijensiz olduğunda, böylece STING aktivasyonu hastalıklı dokularla sınırlı kaldı.
Mantık Kapısından Farelerde Tümör Kontrolüne
Yazarlar daha sonra PHM nanopartikülleri adını verdikleri öne çıkan formülasyonlarını Lewis akciğer karsinomundan kaynaklanan akciğer metastazları, üçlü negatif meme kanseri ve melanom dahil birkaç agresif fare kanser modelinde test ettiler. Tek bir intravenöz doz, serbest ilaç veya yalnızca tek bir uyaranla yanıt veren partiküllerle karşılaştırıldığında görünür akciğer tümör nodüllerinin sayısını büyük ölçüde azalttı. Karaciğer ve böbrek hasarı belirteçleri ile inflamatuar sitokinleri de izleyen kafa‑kafa karşılaştırmalarda, AND kapılı tasarım güçlü tümör kontrolü ile düşük sistemik toksisite arasındaki en iyi dengeyi sağladı. Detaylı bağışıklık çalışmaları bunun nedenini ortaya koydu: tedavi sağlam bir STING yoluna, özel bir dendritik hücre alt tipine (cDC1) ve öldürücü CD8 T hücrelerine bağlıydı. Tedavi edilen tümörlerde bu dendritik hücreler yüksek seviyelerde aktive STING gösterdi ve genellikle güçlü tümör‑öldürücü ve bellek özellikleri kazanmış CD8 T hücresi kümeleriyle doğrudan temas hâlinde görüldü. 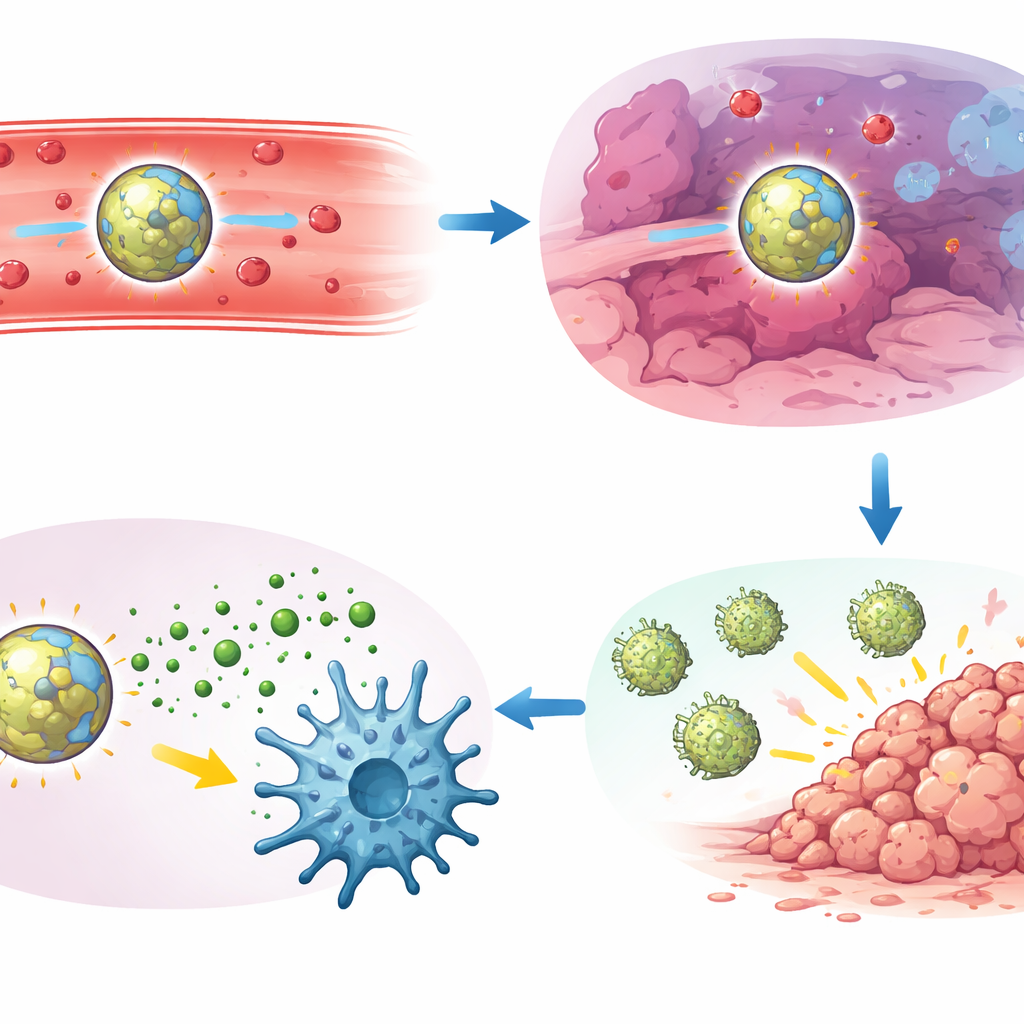
Kalıcı Koruma ve Diğer Tedavilerle Ortaklık
Mevcut metastazları küçültmenin ötesinde nanopartiküller bağışıklık sistemini uzun süre eğitmeye de yardımcı oldu. İlk tedaviden sağ kalan fareler aynı kanser hücreleriyle yapılan sonraki yeniden meydan okumaya direnç gösterdi; bu da dayanıklı bağışıklık belleğini işaret ediyordu. Melanom modellerinde parçacıkların bir immün kontrol noktası inhibitörü ile kombinasyonu hayatta kalmayı daha da uzattı; bu da hassas STING aktivasyonunun mevcut immünoterapilerle sinerji gösterebileceğini düşündürüyor. Zorlu bir meme kanseri modelinde parçacıklar tek başına metastazları belirgin şekilde azalttı ve sağkalımı iyileştirdi; kombinasyonun ek bir fayda sunmaması ise en uygun eşleştirmelerin tümör tipine bağlı olabileceğini vurguluyor.
Gelecekteki Kanser Bakımı İçin Anlamı
Uzman olmayan birine yönelik ana mesaj şudur: bu çalışma güçlü ama kaba bir bağışıklık anahtarını daha seçici bir şeye dönüştürüyor. Hem asiditeyi hem de düşük oksijeni dinleyen moleküler bir AND kapısı kurarak—tehlikeli tümörlerde yaygın, çoğu sağlıklı dokuda nadir olan koşullar—yazarlar tüm vücudu devriye gezebilen ancak güçlü bağışıklık aktivasyonunu esas olarak metastazların saklandığı yerlerde ateşleyebilen bir nanopartikül yarattılar. Henüz hayvan çalışması aşamasında olmakla birlikte, bu strateji geleceğin kanser immünoterapilerini hem daha güvenli hem de daha etkili hale getirmeye yardımcı olabilir ve aynı mantık‑temelli tasarım kanserin ötesinde diğer ilaçlar ve hastalık sinyalleri için de uyarlanabilir.
Atıf: Ye, S., Chen, S., Basava, V. et al. AND logic nanoparticle for precision immunotherapy of metastatic cancers. Nat. Nanotechnol. 21, 606–616 (2026). https://doi.org/10.1038/s41565-026-02130-3
Anahtar kelimeler: kanser immünoterapisi, nanopartiküller, STING yolu, tümör mikroçevresi, metastaz