Clear Sky Science · nl
AND-logica nanodeeltje voor precieze immunotherapie van metastatische kankers
Slimmere kankerbehandelingen die weten wanneer ze moeten inschakelen
Veel van de veelbelovende kankertherapieën van vandaag mobiliseren het immuunsysteem om tumoren te herkennen en te vernietigen. Maar deze krachtige middelen kunnen ook gezonde organen ontsteken en ernstige bijwerkingen veroorzaken. Deze studie beschrijft een "slim" nanodeeltje dat meer op een klein logische schakeling lijkt dan op een eenvoudig geneesmiddelkapsel: het activeert een sterke immuunroute alleen wanneer het gelijktijdig twee kenmerken van agressieve tumoren detecteert. Het doel is eenvoudig maar ambitieus: wijdverspreide, moeilijk te behandelen metastasen aanpakken en tegelijk de rest van het lichaam sparen.
Waarom het overal inschakelen van immuniteit een probleem is
Metastatische kanker, waarbij kankercellen zich in verre organen zoals de longen nestelen, veroorzaakt de grote meerderheid van de kankerdoden. Een aantrekkelijke doelwitroute voor nieuwe geneesmiddelen is een cellaal alarmsysteem dat bekendstaat als de STING-route, die immuuncellen helpt gevaar te detecteren en antivirale en antitumorverdedigingen op te starten. Wanneer STING op de juiste plek wordt geactiveerd, kan het sluimerende immuunreacties wakker maken en T‑cellen helpen tumoren aan te vallen. Maar wanneer het te breed of te sterk wordt geactiveerd, kan het immuuncellen uitputten of zelfs doden en gezonde weefsels ontsteken. Eerdere kleine molecule-STING-stimulatoren in klinische proeven leverden beperkte voordelen maar aanzienlijke bijwerkingen, deels omdat ze geen precieze controle hadden over waar en in welke cellen ze werkzaam waren.
Een klein AND-poortje bouwen voor tumorsignalen
Om dit op te lossen ontwierpen de onderzoekers nanodeeltjes die werken als een elektronische AND-logische poort: ze geven hun STING-activerende lading alleen vrij als twee afzonderlijke tumorcondities gelijktijdig aanwezig zijn. De deeltjes zijn gemaakt van een pH‑gevoelig polymeer dat assembleert tot micellen—nanoschaalbolletjes die stabiel zijn in de neutrale omgeving van het bloed. Een kleine moleculaire STING‑agonist is chemisch aan dit polymeer gekoppeld via een linker die wordt afgebroken onder zuurstofarme omstandigheden. Veel vaste tumoren, vooral metastatische "immuun‑koude" tumoren, zijn zowel zuurder als meer hypoxisch dan normale weefsels. Alleen in deze gecombineerde situatie valt het deeltje uit elkaar en geeft het zijn geneesmiddel vrij. Proefbuisexperimenten bevestigden de volledige waarheidstabel van een AND‑poort: zonder zuurtegraad, zonder hypoxie, of met slechts één van de twee, werd bijna geen medicijn vrijgegeven; met beide werd de afgifte snel en vrijwel volledig. 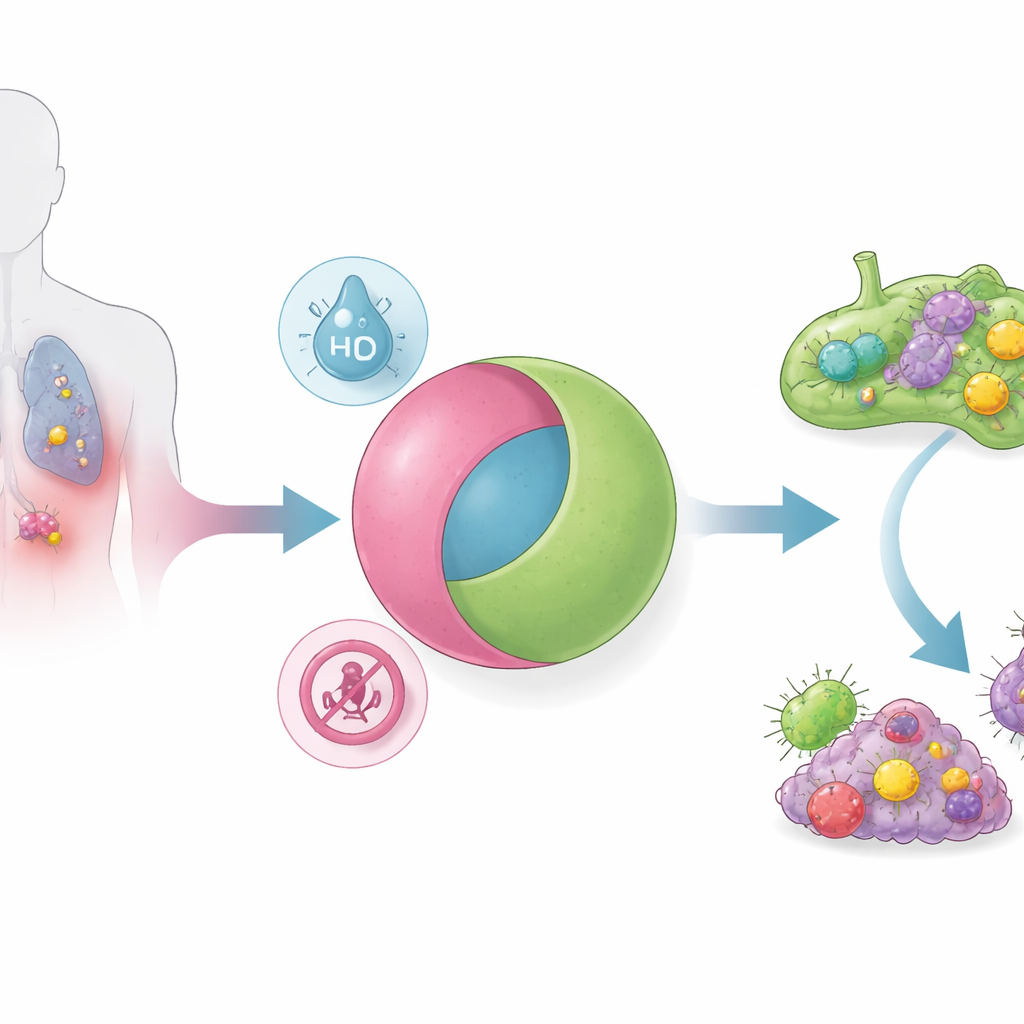
De vonk richten op de juiste immuuncellen
In muizen circuleerden deze AND‑geschakelde deeltjes urenlang zonder samen te klonteren en hoopten ze bij voorkeur op in de milt, lymfeklieren en longmetastasen. Flowcytometrie‑analyses toonden aan dat ze voornamelijk werden opgenomen door belangrijke immuunsentinels—dendritische cellen en macrofagen—en niet zozeer door T‑cellen of de kankercellen zelf. Onder hypoxische omstandigheden verhoogden dendritische cellen van nature het niveau van een enzym dat de zuurstofgevoelige linker knipt, waardoor de tumorgerichte respons verder werd aangescherpt. Eenmaal geactiveerd binnen deze cellen stimuleerden de deeltjes sterke productie van interferon‑β en andere alarmsignalen, maar alleen wanneer de lokale omgeving zowel zuur als zuurstofarm was, wat hielp STING‑activatie tot zieke weefsels te beperken.
Van logische poort naar tumorcontrole in muizen
De auteurs testten vervolgens hun leidende formulering, aangeduid als PHM‑nanodeeltjes, in verschillende agressieve muizen-kankermodellen, waaronder longmetastasen van Lewis longcarcinoom, triple‑negatieve borstkanker en melanoom. Een enkele intraveneuze dosis verminderde het aantal zichtbare longtumorknobbels sterk vergeleken met vrij medicijn of met deeltjes die slechts op één stimulus reageerden. In directe vergelijkingen waarbij ook lever‑ en nierschade‑markers en inflammatoire cytokinen werden gevolgd, leverde het AND‑geschakelde ontwerp de beste balans tussen sterke tumorcontrole en lage systemische toxiciteit. Gedetailleerde immuunstudies onthulden waarom: de behandeling was afhankelijk van een intacte STING‑route, van een gespecialiseerde subset dendritische cellen (cDC1) en van cytotoxische CD8‑T‑cellen. In behandelde tumoren vertoonden deze dendritische cellen hoge niveaus van geactiveerde STING en werden ze vaak gezien in direct contact met clusters van CD8‑T‑cellen, die krachtige tumor‑dodende en geheugenachtige eigenschappen hadden verworven. 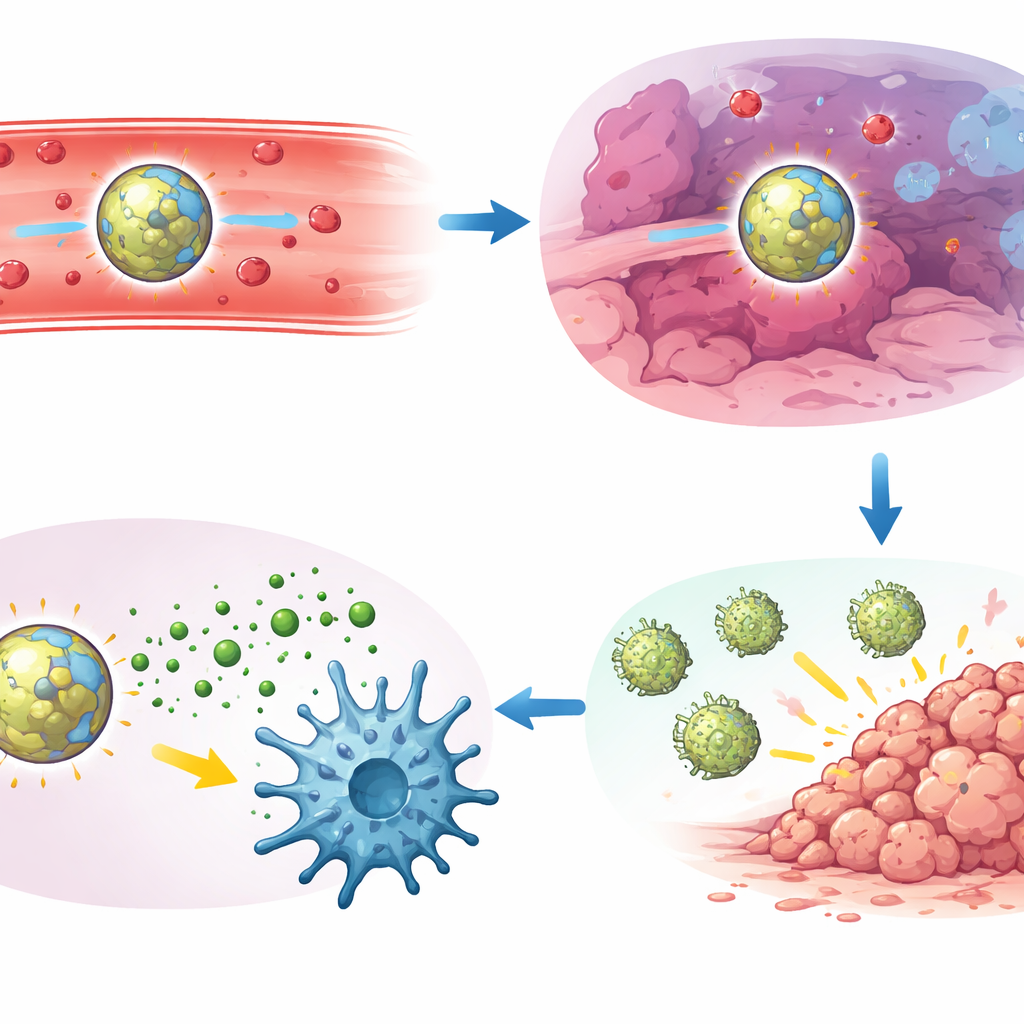
Duurzame bescherming en samenwerking met andere therapieën
Buiten het verkleinen van bestaande metastasen hielpen de nanodeeltjes het immuunsysteem ook langdurig trainen. Muizen die de initiële behandeling overleefden waren bestand tegen een latere heruitdaging met dezelfde kankercellen, wat duidt op duurzaam immuungeheugen. In melanommodellen verlengde de combinatie van de deeltjes met een immuuncheckpointremmer de overleving verder, wat suggereert dat precieze STING‑activatie kan synergeren met bestaande immunotherapieën. In een zwaar borstkankermodel verminderden de deeltjes alleen de metastasen aanzienlijk en verbeterden ze de overleving, hoewel de combinatie met checkpointblokade geen extra voordeel opleverde, wat benadrukt dat optimale combinaties van tumorsoort kunnen afhangen.
Wat dit kan betekenen voor toekomstige kankerzorg
Voor niet‑specialisten is de kernboodschap dat dit werk een krachtige maar botte immuunschakelaar verandert in iets selectievers. Door een moleculaire AND‑poort te bouwen die luistert naar zowel zuurtegraad als lage zuurstof—condities die vaak voorkomen in gevaarlijke tumoren maar zeldzaam zijn in de meeste gezonde weefsels—creëerden de auteurs een nanodeeltje dat het hele lichaam kan patrouilleren maar sterke immuunactiviteit vooral ontsteekt waar metastasen zich verbergen. Hoewel nog in het dieronderzoek‑stadium, kan deze strategie toekomstige kankerimmunotherapieën veiliger en effectiever maken, en hetzelfde logica‑gebaseerde ontwerp kan worden aangepast aan andere geneesmiddelen en ziekte‑signalen buiten kanker.
Bronvermelding: Ye, S., Chen, S., Basava, V. et al. AND logic nanoparticle for precision immunotherapy of metastatic cancers. Nat. Nanotechnol. 21, 606–616 (2026). https://doi.org/10.1038/s41565-026-02130-3
Trefwoorden: kankerimmunotherapie, nanodeeltjes, STING-route, tumormicro-omgeving, metastase