Clear Sky Science · ar
جسيم نانوي بمنطق AND للعلاج المناعي الدقيق للأورام النقيليّة
علاجات سرطانية أذكى تعرف متى تتفعّل
تعمل العديد من العلاجات الواعدة للسرطان اليوم عن طريق تحفيز الجهاز المناعي للتعرف على الأورام وتدميرها. ومع ذلك، يمكن لهذه الأدوية القوية أيضاً أن تهيّج الأعضاء السليمة، مما يسبب آثاراً جانبية خطيرة. تصف هذه الدراسة جسماً نانويّاً «ذكياً» يتصرف أشبه بدائرة منطقية صغيرة أكثر من كونه كبسولة دوائية بسيطة: يتفعّل مسار مناعي قوي فقط عندما يكشف عن علامتين مميزتين للأورام العدوانية معاً. الهدف واضح وطموح — استهداف النقائل المنتشرة والصعبة العلاج مع الحفاظ على بقية الجسم سالماً.
لماذا يمثل تفعيل المناعة في كل مكان مشكلة
يسبب السرطان النقيلي، حيث تزرع خلايا الورم في أعضاء بعيدة مثل الرئتين، الغالبية العظمى من وفيات السرطان. أحد الأهداف الجذّابة للأدوية الجديدة هو نظام إنذار خلوي يعرف باسم مسار STING، الذي يساعد خلايا المناعة على استشعار الخطر وإطلاق دفاعات مضادة للفيروسات والأورام. عندما يتفعّل في المكان المناسب، يمكن لـ STING إيقاظ استجابات مناعية كامنة ومساعدة الخلايا التائية على مهاجمة السرطان. لكن عند تحفيزه بشكل واسع أو قوي للغاية، يمكن أن يستنزف أو يقتل خلايا المناعة ويهيّج الأنسجة السليمة. أظهر المنبهات الجزيئية الصغيرة المبكرة لمسار STING في التجارب السريرية فوائد متواضعة ولكن آثاراً جانبية كبيرة، جزئياً لأنها تفتقر إلى التحكم الدقيق في المكان والخلايا التي تعمل فيها.
بناء بوابة AND صغيرة لإشارات الورم
لحل هذه المشكلة، صمّم الباحثون جسيمات نانوية تعمل مثل بوابة منطقية AND إلكترونية: تُطلق حمولة منشطة لمسار STING فقط إذا وُجدت حالتان ورميّتان منفصلتان في الوقت نفسه. تصنع الجسيمات من بوليمر حساس للحموضة يتجمع إلى ميليس—كرات نانوية مستقرة في بيئة الدم ذات الحموضة المتعادلة. يُربط منشّط STING الجزيئي الصغير كيميائياً بهذا البوليمر عبر واصل يتحلل في ظروف انخفاض الأكسجين. العديد من الأورام الصلبة، خصوصاً النقائليّة «الباردة مناعياً»، تكون أكثر حمضية وأكثر نقصاً في الأكسجين مقارنة بالأنسجة الطبيعية. فقط في هذا الظرف المشترك تتفكك الجسيمات وتطلق حمولة الدواء. أكدت تجارب أنبوب الاختبار جدول الحقيقة الكامل لبوابة AND: بدون الحموضة، أو بدون نقص الأكسجين، أو بوجود أحد العاملين فقط، لم يُطلَق الدواء تقريباً؛ ومع وجودهما معاً، أصبح الإطلاق سريعاً وشبه مكتمل. 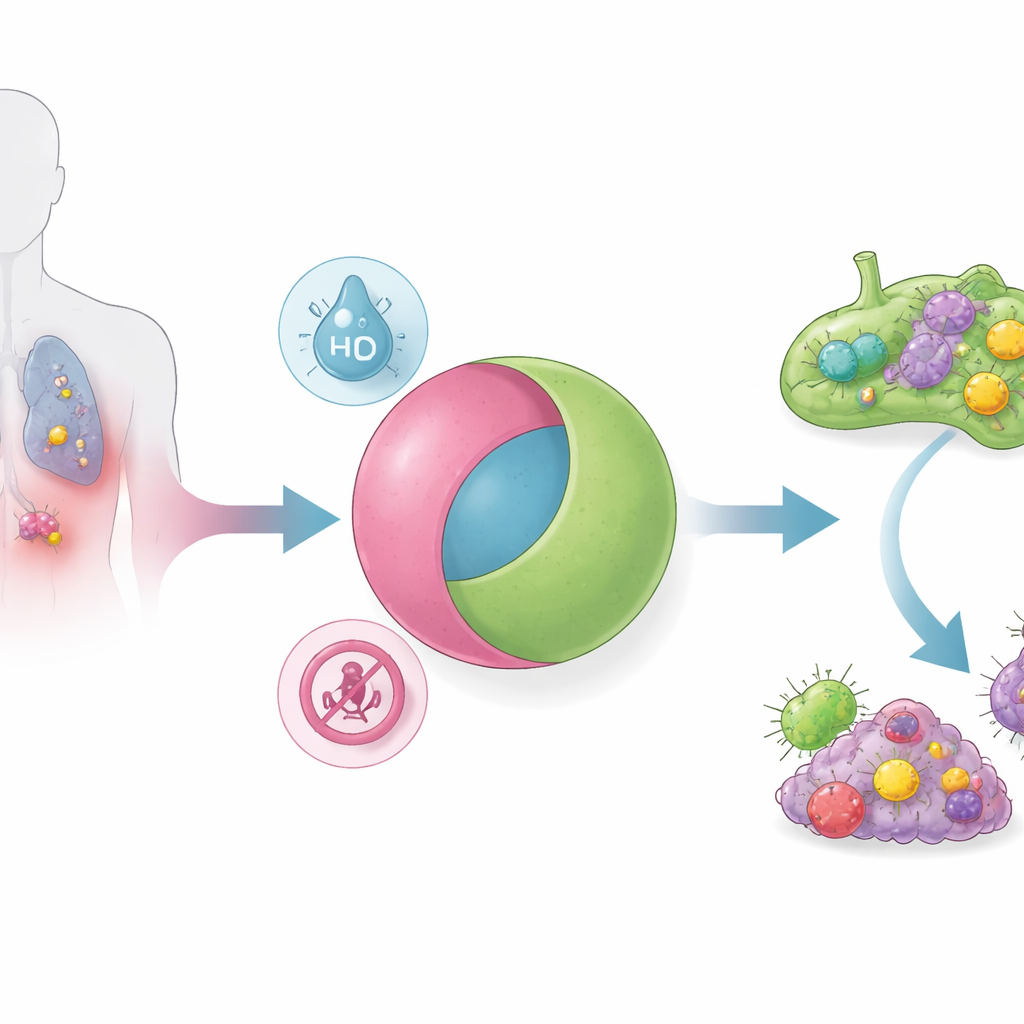
توجيه الشرارة إلى خلايا المناعة المناسبة
في الفئران، دارت هذه الجسيمات ذات بوابة AND لساعات دون تكتل وتراكمت بميول في الطحال والعقد الليمفاوية ونقائل الرئة. أظهرت تحليلات الفلو سيتمتري أنها التُقطت بشكل أساسي بواسطة حراس مناعيين رئيسيين—الخلايا التغصنية والبلعميات—بدلاً من الخلايا التائية أو خلايا السرطان نفسها. تحت ظروف نقص الأكسجين، رفعت الخلايا التغصنية طبيعياً مستويات إنزيم يقطع الوصل الحساس للأكسجين، مما زاد من دقة الاستجابة الميّالة للورم. بمجرد تفعيلها داخل هذه الخلايا، حفّزت الجسيمات إنتاجاً قوياً للإنترفرون-β وإشارات إنذار أخرى، لكن فقط عندما كانت البيئة المحلية حمضية وفقيرة بالأكسجين، مما ساعد على حصر تفعيل STING في الأنسجة المريضة.
من بوابة منطقية إلى السيطرة على الورم في الفئران
اختبر المؤلفون بعد ذلك التركيبة القيادية، المسماة جسيمات PHM، في عدة نماذج سرطانية فئران عدوانيّة، بما في ذلك نقائل رئوية من سرطان رئة لويس، وسرطان ثدي ثلاثي السلبية، والميلانوما. جرعة واحدة وريدية خفّضت بشكل كبير عدد العقيدات الورمية الظاهرة في الرئتين مقارنةً بالمادة الحرة أو بالجسيمات التي استجابت لمؤثر واحد فقط. في مقارنات مباشرة تابعت أيضاً علامات إصابة الكبد والكليتين والسيتوكينات الالتهابية، قدّم تصميم بوابة AND أفضل توازن بين سيطرة قوية على الورم وسمّية جهازية منخفضة. كشفت دراسات مناعية مفصّلة عن السبب: اعتمد العلاج على مسار STING سليم، وعلى فئة متخصصة من الخلايا التغصنية (cDC1)، وعلى خلايا CD8 القاتلة. في الأورام المعالجة، أظهرت هذه الخلايا التغصنية مستويات عالية من STING المفعّل وغالباً ما شوهدت على اتصال مباشر مع مجموعات من خلايا CD8، التي اكتسبت خصائص قتالية ضد الورم وميزات ذاكرة قوية. 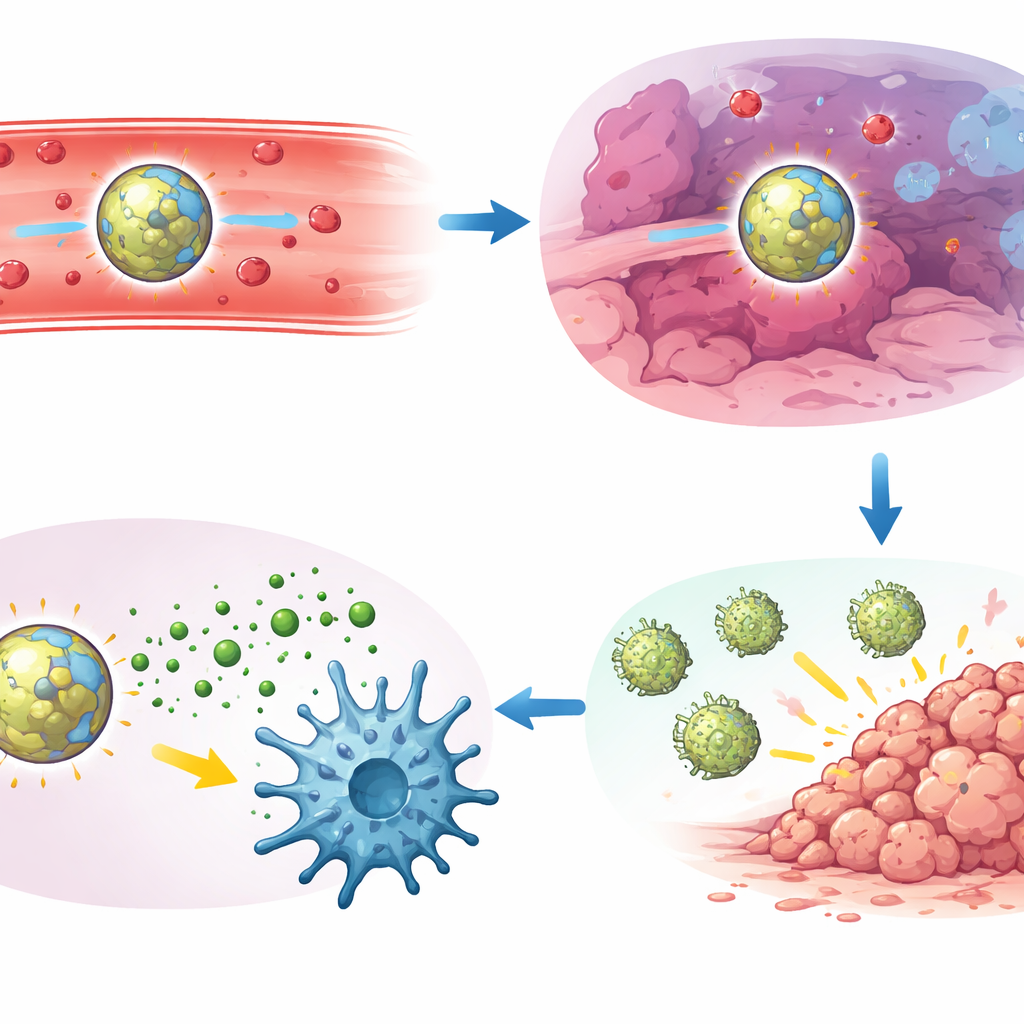
حماية دائمة وتكامل مع علاجات أخرى
بعيداً عن تقليص النقائل الحالية، ساعدت الجسيمات النانوية على تدريب الجهاز المناعي لفترة طويلة. تمكنت الفئران التي نجت من العلاج الأولي من مقاومة إعادة تحدي لاحقة بنفس خلايا السرطان، مما يدل على ذاكرة مناعية دائمة. في نماذج الميلانوما، أدى الجمع بين الجسيمات ومثبط نقاط التفتيش المناعي إلى إطالة البقاء أكثر، مما يشير إلى أن تفعيل STING الدقيق يمكن أن يتآزر مع العلاجات المناعية الحالية. في نموذج قاسٍ لسرطان الثدي، خفّضت الجسيمات وحدها النقائل بشكل ملحوظ وحسّنت البقاء، رغم أن دمجها مع حجب نقاط التفتيش لم يقدّم فائدة إضافية، مما يبرز أن التزاوجات المثلى قد تعتمد على نوع الورم.
ما الذي قد يعنيه هذا لعناية السرطان المستقبلية
لغير المتخصص، الرسالة الأساسية هي أن هذا العمل يحوّل مفتاح مناعي قوي لكنه خشن إلى أداة أكثر تمييزاً. من خلال بناء بوابة جزيئية AND تستمع لكل من الحموضة وقلة الأكسجين—ظروف شائعة في الأورام الخطرة ونادرة في معظم الأنسجة السليمة—أنشأ المؤلفون جسيمات نانوية يمكنها التجوال في الجسم بأكمله ومع ذلك إشعال نشاط مناعي قوي أساساً حيث تكمن النقائل. ومع أنها ما زالت في مرحلة دراسات حيوانية، يمكن أن تساعد هذه الاستراتيجية في جعل العلاجات المناعية للسرطان أكثر أماناً وفعالية، ويمكن تطبيق نفس التصميم القائم على المنطق على أدوية وإشارات مرضية أخرى تتجاوز السرطان.
الاستشهاد: Ye, S., Chen, S., Basava, V. et al. AND logic nanoparticle for precision immunotherapy of metastatic cancers. Nat. Nanotechnol. 21, 606–616 (2026). https://doi.org/10.1038/s41565-026-02130-3
الكلمات المفتاحية: العلاج المناعي للسرطان, الجسيمات النانوية, مسار STING, البيئة الدقيقة للورم, النقائل