Clear Sky Science · sv
AND-logiknanopartikel för precisionsimmunoterapi mot metastaserande cancer
Smartare cancerbehandlingar som vet var de ska slå på sig
Många av dagens mest lovande cancerterapier verkar genom att samla immunsystemet för att känna igen och förstöra tumörer. Dessa kraftfulla läkemedel kan dock också orsaka inflammation i friska organ, med allvarliga biverkningar som följd. I denna studie beskrivs en ”smart” nanopartikel som beter sig mer som en liten logikkrets än som en enkel läkemedelskapsel: den aktiverar en potent immunväg endast när den samtidigt upptäcker två kännetecken för aggressiva tumörer. Målet är enkelt men ambitiöst — att slå mot utbredda, svårbehandlade metastaser samtidigt som resten av kroppen skonas.
Varför det är problematiskt att slå på immuniteten överallt
Metastaserande cancer, där tumörceller sprider sig till avlägsna organ som lungorna, orsakar majoriteten av cancerrelaterade dödsfall. Ett attraktivt mål för nya läkemedel är ett cellulärt alarmsystem känt som STING‑vägen, som hjälper immunceller att uppfatta fara och initiera antivirala och antitumörförsvar. När STING slås på på rätt plats kan det väcka tysta immunsvar och hjälpa T‑celler att angripa cancer. Men om det triggas alltför brett eller kraftfullt kan det trötta ut eller till och med döda immunceller och orsaka inflammation i friska vävnader. Tidigare småmolekylära STING‑stimulatorer i kliniska prövningar gav måttliga fördelar men betydande biverkningar, delvis därför att de saknade precis kontroll över var och i vilka celler de verkade.
Bygga en liten AND-grind för tumörsignaler
För att lösa detta designade forskarna nanopartiklar som fungerar som en elektronisk AND‑logikgrind: de frigör sitt STING‑aktiverande innehåll endast om två separata tumörvillkor är närvarande samtidigt. Partiklarna är gjorda av en pH‑känslig polymer som monterar sig till miceller — nanoskaliga sfärer som är stabila i blodomloppets neutrala miljö. En småmolekylär STING‑agonist är kemiskt fäst till denna polymer genom en länk som bryts ner under låg‑syreförhållanden. Många solida tumörer, särskilt metastaserande ”immun‑kalla” sådana, är samtidigt mer sura och mer hypoxiska än normala vävnader. Endast i denna kombinerade miljö lossnar partikeln och avger sin läkemedelslast. Rörprovsförsök bekräftade sannolikhetstabellen för en AND‑grind: utan surhet, utan hypoxi eller med bara en av de två, frigjordes nästan inget läkemedel; med båda blev frisättningen snabb och nära nog fullständig. 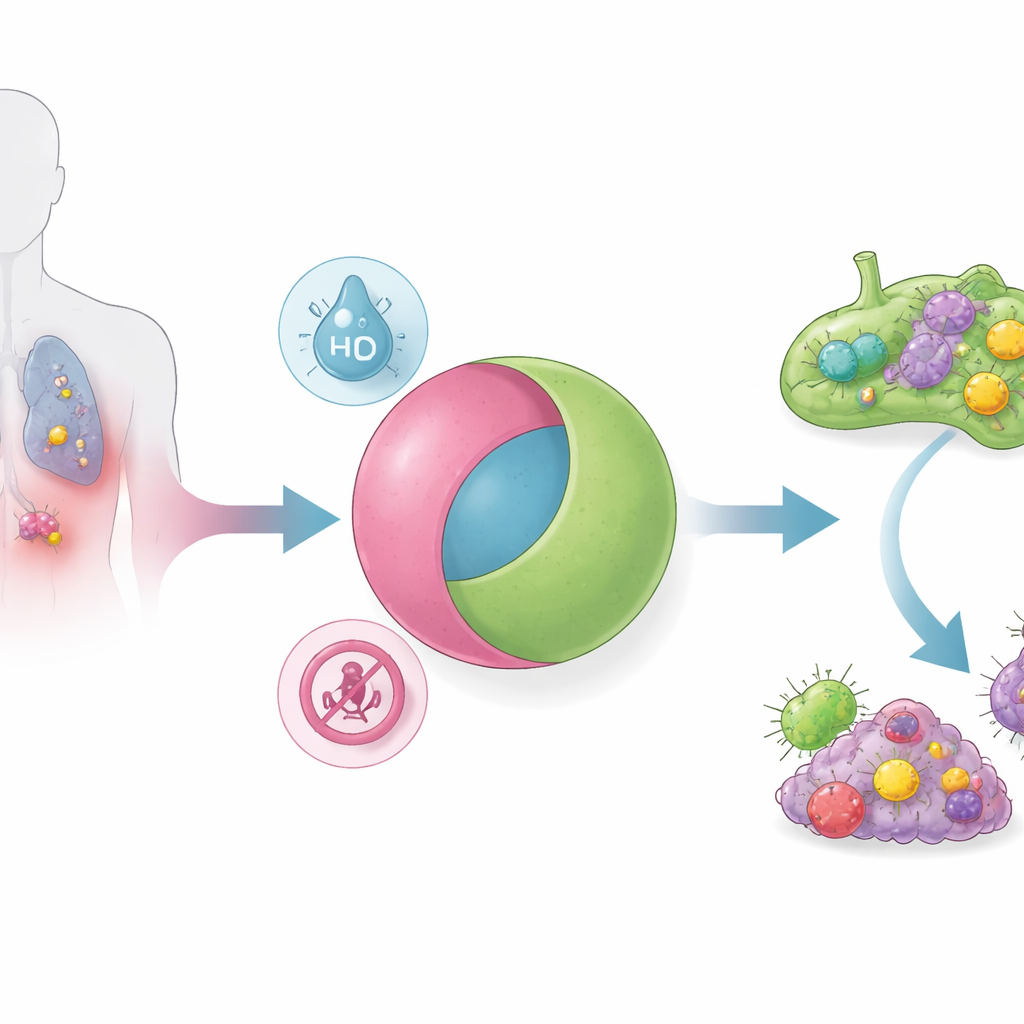
Rikta gnistan mot rätt immunceller
I möss cirkulerade dessa AND‑grindade partiklar i timmar utan att klumpa sig och ackumulerades föredömligt i mjälten, lymfknutor och lungmetastaser. Flödescytometrianalyser visade att de togs upp huvudsakligen av nyckelimmunsentineler — dendritiska celler och makrofager — snarare än av T‑celler eller av cancercellerna själva. Under hypoxiska förhållanden ökade dendritiska celler naturligt nivåerna av ett enzym som klipper den syrekänsliga länken, vilket ytterligare skärpte det tumörbiaserade svaret. När partiklarna väl aktiverades inne i dessa celler drev de stark produktion av interferon‑β och andra alarmsignaler, men endast när den lokala miljön var både sur och syrefattig, vilket hjälpte till att begränsa STING‑aktiveringen till sjuk vävnad.
Från logikkrets till tumörkontroll i möss
Författarna testade sedan sin ledande formulering, kallad PHM‑nanopartiklar, i flera aggressiva muscancermodeller, inklusive lungmetastaser från Lewis lungkarcinom, trippelnegativ bröstcancer och melanom. En enda intravenös dos reducerade kraftigt antalet synliga lungtumörnoder jämfört med fritt läkemedel eller partiklar som reagerade på endast ett stimuli. I huvud‑mot‑huvud‑jämförelser som också följde lever‑ och njurmarkörer för skada och inflammatoriska cytokiner levererade den AND‑styrda designen den bästa balansen mellan stark tumörkontroll och låg systemisk toxicitet. Detaljerade immunstudier visade varför: behandlingen var beroende av en intakt STING‑väg, av en specialiserad dendritisk cellsubtyp (cDC1) och av mördande CD8‑T‑celler. I behandlade tumörer visade dessa dendritiska celler höga nivåer av aktiverad STING och sågs ofta i direkt kontakt med kluster av CD8‑T‑celler, som hade förvärvat kraftfulla tumördödande och minnesegenskaper. 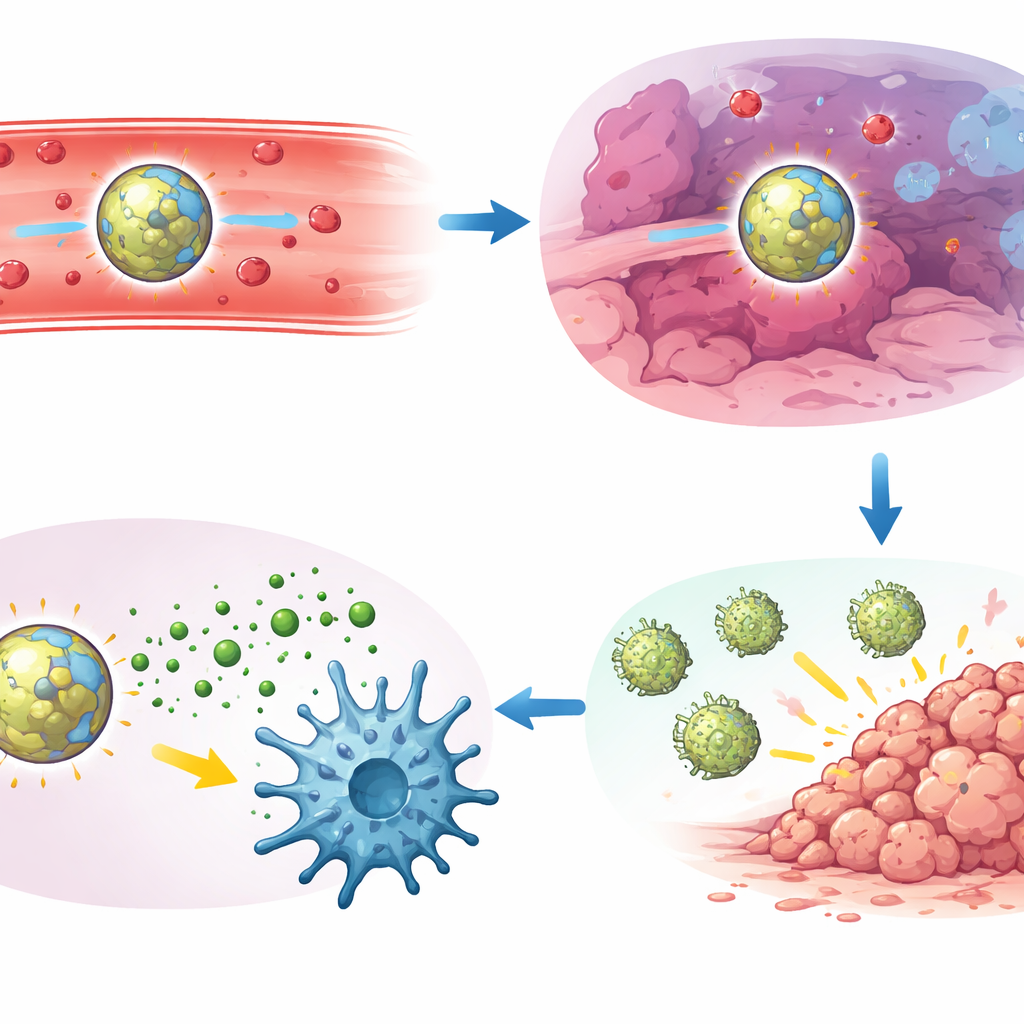
Varaktigt skydd och samarbete med andra terapier
Förutom att krympa befintliga metastaser hjälpte nanopartiklarna immunsystemet att lära för lång sikt. Möss som överlevde den initiala behandlingen kunde motstå en senare återutmaning med samma cancerceller, vilket indikerar hållbart immunminne. I melanommodeller förlängde kombinationen av partiklarna med en immuncheckpoint‑hämmare överlevnaden ytterligare, vilket tyder på att precis STING‑aktivering kan synergisera med befintliga immunoterapier. I en svår bröstcancermodell minskade partiklarna ensamma metastaser markant och förbättrade överlevnaden, även om deras kombination med checkpoint‑blockad inte gav ytterligare fördel, vilket framhäver att optimala kombinationer kan bero på tumörtyp.
Vad detta kan betyda för framtidens cancervård
För icke‑specialisten är huvudbudskapet att detta arbete omvandlar en kraftfull men trubbig immunbrytare till något mer diskriminerande. Genom att bygga en molekylär AND‑grind som lyssnar efter både surhet och låg syrehalt — förhållanden vanliga i farliga tumörer men ovanliga i de flesta friska vävnader — skapade författarna en nanopartikel som kan patrullera hela kroppen men tända kraftfulla immunsvar främst där metastaser gömmer sig. Trots att det fortfarande är i djurstudie‑stadiet kan denna strategi göra framtida cancerimmunoterapier både säkrare och mer effektiva, och samma logikbaserade design kan anpassas till andra läkemedel och signalsystem bortom cancer.
Citering: Ye, S., Chen, S., Basava, V. et al. AND logic nanoparticle for precision immunotherapy of metastatic cancers. Nat. Nanotechnol. 21, 606–616 (2026). https://doi.org/10.1038/s41565-026-02130-3
Nyckelord: cancerimmunoterapi, nanopartiklar, STING‑vägen, tumörmikromiljö, metastas