Clear Sky Science · zh
跨哺乳动物大脑的信息整合及其在麻醉下崩溃的转录组与连通组控制器的趋同
这对日常大脑意味着什么
当你在全身麻醉下昏睡过去时,即便大脑在解剖上仍然完好,你对外界的觉察会消失。该研究提出了一个简单却深刻的问题:在那一刻大脑内部究竟发生了什么变化,这种变化是否在非常不同的哺乳动物和不同药物之间共有?通过结合脑成像、基因学与计算模型在人类、猕猴、绒头猴和小鼠中的应用,作者发现了一些共同的“控制旋钮”,它们似乎决定了大脑将信息缝合成连贯意识体验的能力。
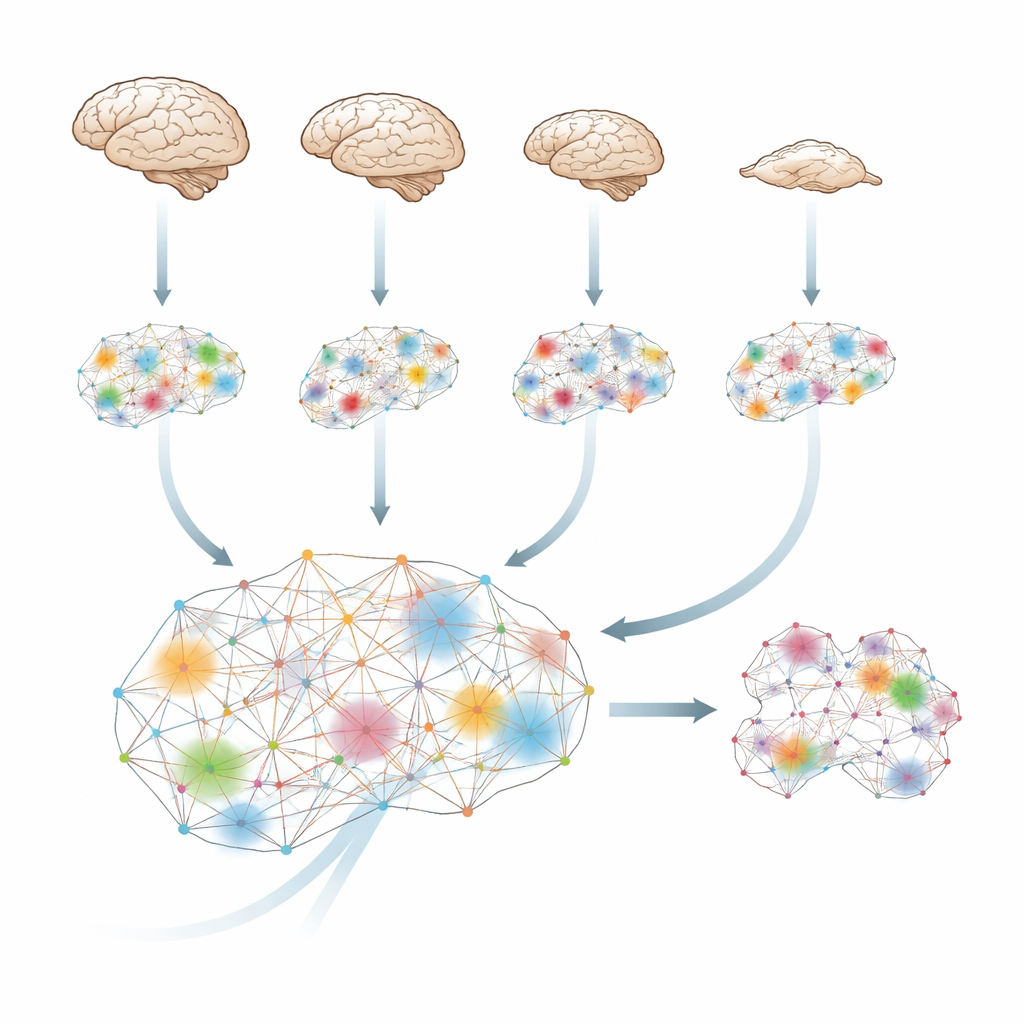
大脑如何将信息编织为整体
大脑不断进行预测与更新,因此下一刻会发生什么部分依赖于之前发生的事情。研究者使用信息论工具,量化了当脑区协同工作时所涌现出的“额外”信息,超出各自单独携带的信息量。他们将此称为整合信息:衡量不同大脑部分作为单一协调系统而非孤立岛屿或彼此简单回声地行动的强度的指标。
麻醉在物种间的共同效应
研究团队分析了四种物种——人类、猕猴、绒头猴和小鼠——在清醒与使用多种麻醉药物时的功能性磁共振成像。尽管大脑结构与药物差异巨大,结果却出人意料地相似。每当动物失去行为响应时,整个大脑的整合信息水平都会下降。在人类中,这一度量在自发从七氟烷(sevoflurane)中醒来时又回升。在猕猴中,对中央丘脑区域——位于大脑深处——的电刺激在仍在输注药物的情况下,既恢复了行为也恢复了整合信息。这表明麻醉的核心作用并非仅仅是压制大脑活动,而是扰乱其将信息融合为统一整体的能力,而且通过定向刺激可以逆转这种丧失。
为何大脑动力学变得更难以操控
为理解这种崩溃背后的力学机制,作者采用了网络控制理论,该理论将大脑视为一个可在多种活动模式间切换的复杂系统。利用各物种特有的区域物理连线图,他们计算了将大脑从一个瞬时活动模式推到下一个需要多少“能量”。在麻醉下,这种控制能量一致地增加:可能的大脑状态景观变得更陡峭、更难以穿越。重要的是,当受试者醒来或丘脑刺激恢复响应时,这种动力学的僵化会松弛,并且与整合信息的下降紧密相关。简而言之,当大脑更难被引导时,它也更难以整合信息。
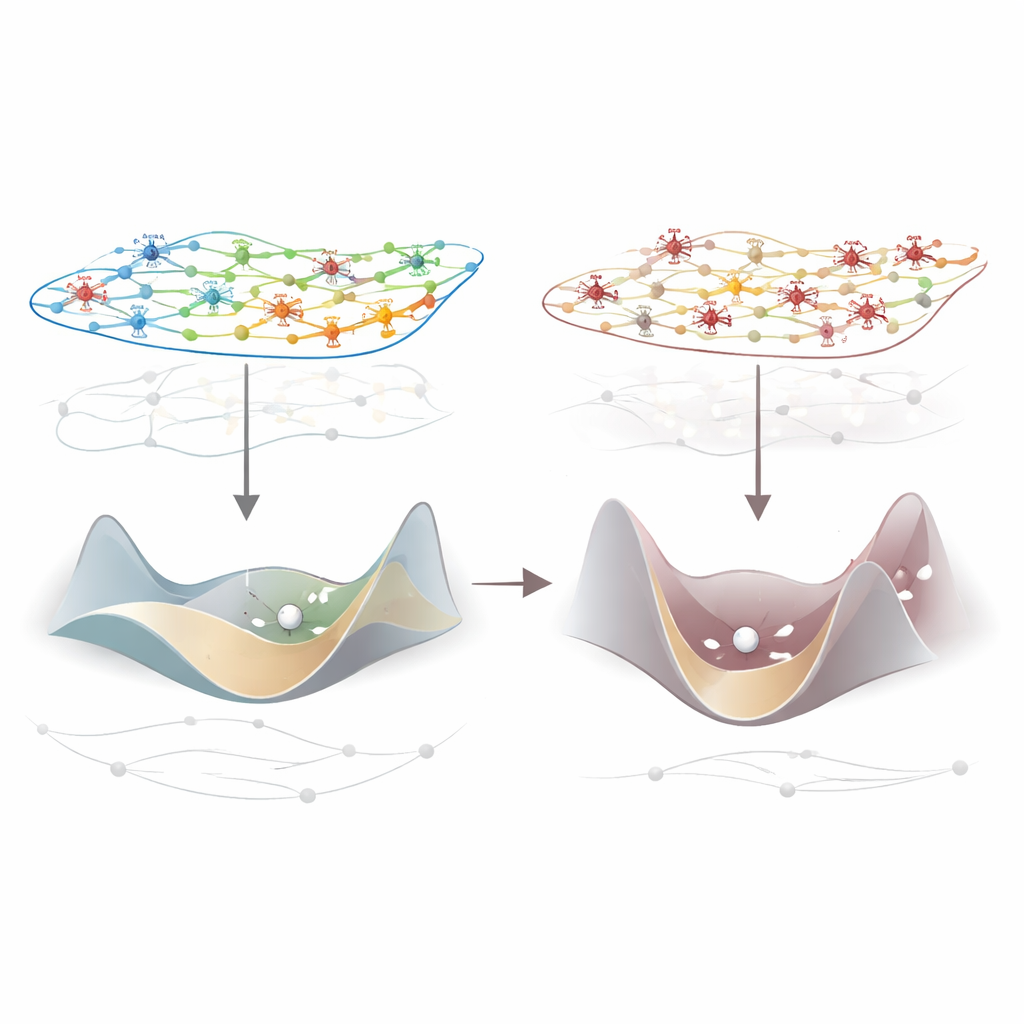
调节局部活动刹车的基因
并非所有脑区受影响的程度相同。整合信息损失最大的是初级感觉与运动区,但变化是广泛存在的。为探究原因,研究者将这些模式与人类、猕猴和小鼠皮层的基因表达详图叠加。一个基因在各物种中尤为显著:PVALB,它标记一类快速抑制性中间神经元,这些神经元对局部电路起“刹车”作用。PVALB表达较强的区域往往在麻醉下显示出更大的整合信息下降。在小鼠中,这些区域在使用较轻麻醉时也表现出最强的变化——无论是上升还是下降——表明富含PVALB的区域是重塑信息流的特别有力的杠杆点。
在虚拟大脑中检验机制
为了超越相关性,团队构建了生物物理启发的全脑计算模型,分别针对人类、猕猴和小鼠,并以各物种真实的解剖连接为连线。随后他们根据各区域的PVALB水平提高模型中该区域的抑制强度。在三种物种中,这一操作比任意随机的抑制模式更能降低模拟脑活动中的整合信息,并增加在状态间移动所需的控制能量,正如真实麻醉所表现的那样。在一个单独的猕猴模型中,他们加入了丘脑区域并模拟刺激:兴奋中央丘脑相比刺激邻近的控制核,能更大幅度地恢复整合信息,这与动物实验相呼应。
这对意识与恢复意味着什么
这些汇聚的证据指向一个共同的结论:在哺乳动物大脑中,各种麻醉药物通过直接或间接作用于由PVALB标记的抑制回路,使大尺度活动更难以控制并且整合性降低。当这种整合失败时,大脑无法将输入信号编织成统一的、可响应的状态,意识便消退。对中央丘脑的精确刺激可以部分逆转这一过程。除了阐明麻醉的作用机制外,这些发现还为恢复重度脑损伤患者的意识提供了新策略:通过使用大脑连线和基因表达图谱来预测最佳刺激区域,以重新唤起支持意识体验的整合动力学。
引用: Luppi, A.I., Uhrig, L., Tasserie, J. et al. Convergent transcriptomic and connectomic controllers of information integration and its anaesthetic breakdown across mammalian brains. Nat Hum Behav 10, 777–802 (2026). https://doi.org/10.1038/s41562-025-02381-5
关键词: 意识, 麻醉, 大脑网络, 信息整合, 丘脑刺激