Clear Sky Science · ar
المتحكمات المتقاربة عبر النسخ الجيني والاتصالي لدمج المعلومات وانهيارها بسبب التخدير عبر أدمغة الثدييات
لماذا يهم هذا لأدمغة الحياة اليومية
عندما تفقد وعيك تحت التخدير العام، يتلاشى إدراكك للعالم رغم بقاء دماغك سليمًا من الناحية الفيزيائية. تطرح هذه الدراسة سؤالاً بسيطًا لكنه عميق: ماذا يتغير فعلاً داخل الدماغ في تلك اللحظة، وهل يتشارك هذا التغير عبر ثدييات وأدوية مختلفة؟ بدمج تصوير الدماغ، والوراثة، والنماذج الحاسوبية لدى البشر والقرود والفئران، يكشف الباحثون عن مقاييس تحكم مشتركة تبدو وكأنها تحكم مدى قدرة الدماغ على نسج المعلومات معًا لتشكيل تجربة واعية متماسكة.
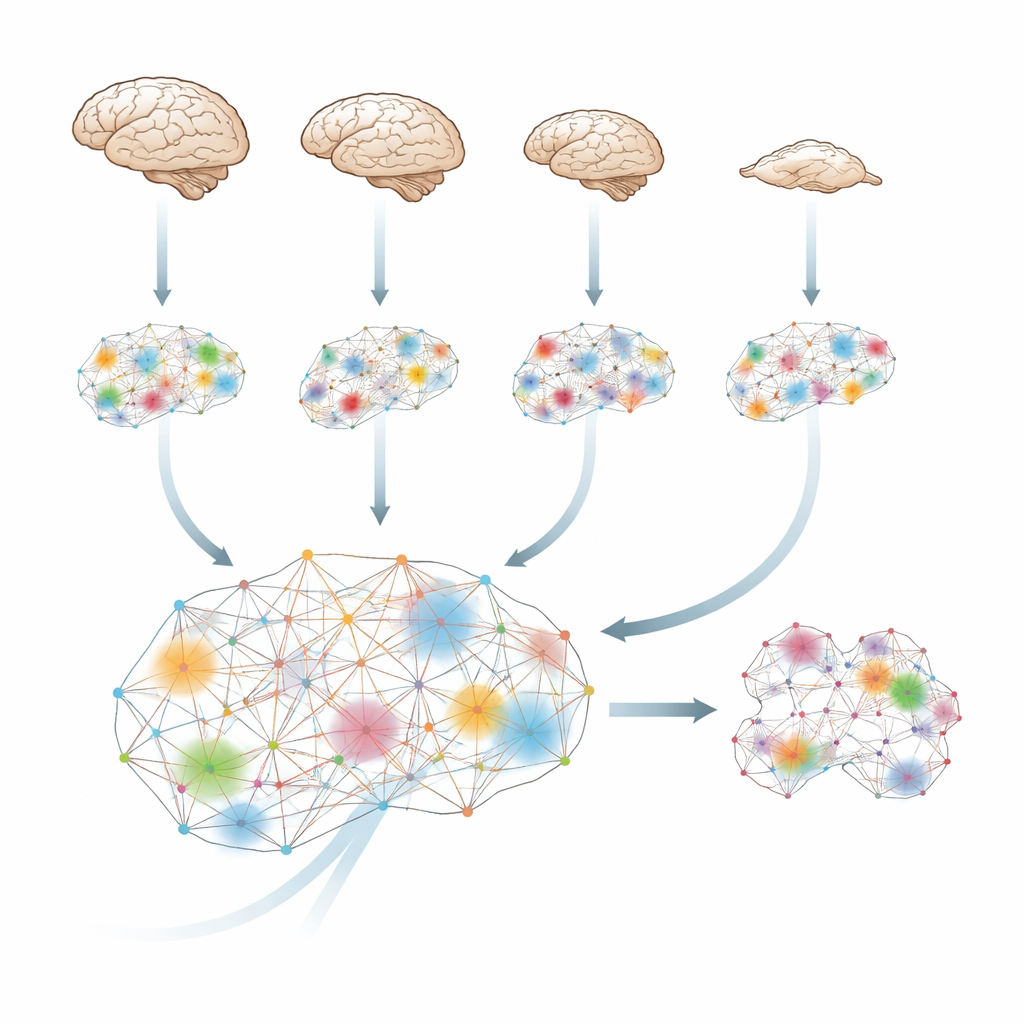
كيف ينسج الدماغ المعلومات إلى كُل
الدماغ يتنبأ ويحدّث باستمرار، لذلك ما سيحدث في اللحظة التالية يعتمد جزئياً على ما حدث للتو. باستخدام أدوات من نظرية المعلومات، يقيس الباحثون مقدار "المعلومات الإضافية" التي تظهر عندما تعمل مناطق الدماغ معًا، فوق ما تحمله كل منطقة بمفردها. يسميون هذا المعلومات المتكاملة: مقياس لمدى قوة عمل أجزاء مختلفة من الدماغ كنظام موحد ومنسق بدلاً من أن تكون جزرًا معزولة أو صدى بسيط لبعضها البعض.
ماذا يفعل التخدير عبر الأنواع
حلل الفريق صور الرنين الوظيفي من أربع أنواع—البشر، والقرود المكاك، والمارموسيت، والفئران—حين كانوا مستيقظين وتحت مجموعة من أدوية التخدير. رغم الفوارق الكبيرة في الأدمغة والأدوية، كان النمط متشابهًا إلى حد لافت. كلما فقدت الحيوانات الاستجابة السلوكية، انخفض مستوى المعلومات المتكاملة عبر الدماغ. لدى البشر، ارتفع هذا المقياس مجددًا عندما استيقظ الأشخاص تلقائيًا من سيفوفلوران. في المكاك، أعاد التحفيز الكهربائي لمنطقة مركزية في المهاد—عميق داخل الدماغ—كلًا من السلوك والمعلومات المتكاملة حتى مع استمرار تسريب الدواء. يشير ذلك إلى أن التأثير الجوهري للتخدير ليس مجرد إسكات الدماغ، بل تعطيل قدرته على مزج المعلومات إلى كُل موحد، وأن هذا الفقدان يمكن عكسه بتحفيز مستهدف.
لماذا تصبح ديناميكيات الدماغ أصعب في التوجيه
لفهم آلية هذا الانهيار، لجأ المؤلفون إلى نظرية التحكم الشبكي، التي تعامل الدماغ كنظام معقد يمكنه الانتقال بين أنماط نشاط متعددة. باستخدام خرائط توصيل نوعية توضح كيف ترتبط المناطق ماديًا، حسبوا كمية "الطاقة" اللازمة لتحريك الدماغ من نمط نشاط لحظي إلى آخر. تحت التخدير، زادت هذه طاقة التحكم باستمرار: أصبح منظر الحالات الدماغية الممكنة أكثر انحدارًا وأصعب عبورًا. وبأهمية كبيرة، ارتخى هذا التصلب في الديناميكيات مجددًا عندما استيقظت العينات أو عندما أعاد تحفيز المهاد الاستجابة، وكان مرتبطًا ارتباطًا وثيقًا بالانخفاض في المعلومات المتكاملة. ببساطة، عندما يصبح الدماغ أقل قابلية للتوجيه، يصبح أيضًا أقل قدرة على دمج المعلومات.
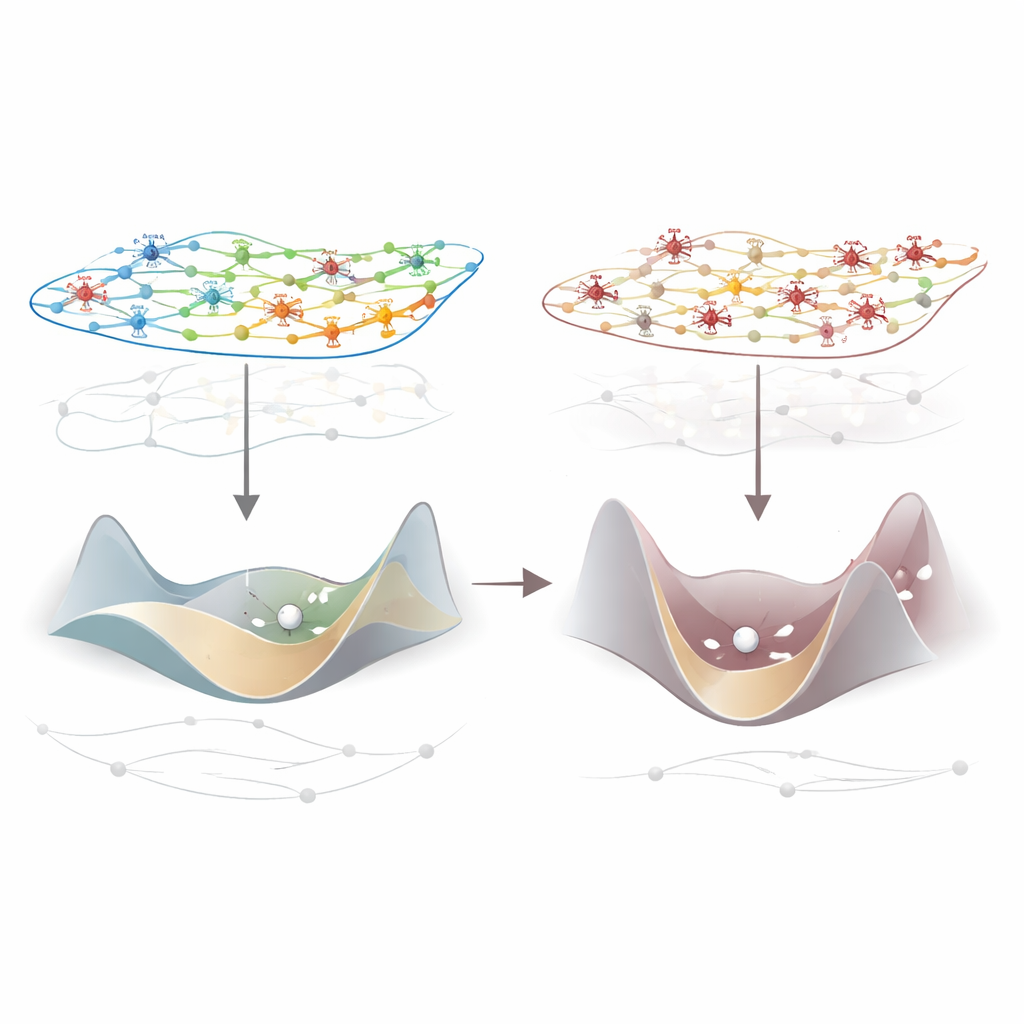
جينات تضبط المكابح المحلية على نشاط الدماغ
لم تتأثر كل المناطق على نحو متساوٍ. بدا أن أكبر خسائر التكامل تحدث في مناطق الحواس والحركة الأولية، لكن التغيرات كانت واسعة الانتشار. لسؤال السبب، وضع الباحثون هذه الأنماط فوق خرائط مفصلة لنشاط الجينات في قشرة البشر والماك والفئران. برز جين واحد عبر الأنواع: PVALB، الذي يميز فئة من الخلايا الداخلية المثبطة سريعة الأداء التي تضع مكابح على الدوائر المحلية. المناطق ذات تعبير أقوى لجين PVALB كانت تميل إلى إظهار انخفاضات أكبر في المعلومات المتكاملة الناجمة عن التخدير. في الفئران، أظهرت هذه المناطق أيضًا أقوى التغيرات—سواء زيادات أو انخفاضات—عند استخدام تخدير أخف، مما يوحي أن المناطق الغنية بـPVALB هي رافعات فعّالة لإعادة تشكيل تدفق المعلومات.
اختبار الآلية في أدمغة افتراضية
للخروج من إطار الارتباط، بنى الفريق نماذج حاسوبية شاملة ذات أساس فيزيائي حيوي لأدمغة البشر والماك والفئران، موصولة بخريطة الاتصالات التشريحية الفعلية لكل نوع. ثم رفعوا نسبة التثبيط في كل منطقة نموذجية وفقًا لمستوى PVALB فيها. عبر الأنواع الثلاثة، أدى هذا التلاعب إلى خفض المعلومات المتكاملة في نشاط الدماغ المحاكى أكثر من أي نمط عشوائي من التثبيط، وزاد طاقة التحكم المطلوبة للتنقل بين الحالات، تمامًا كما تفعل المخدرات الحقيقية. في نموذج مكاك منفصل، أضافوا مناطق مهادية ومحاكوا التحفيز: أدى إثارة المهاد المركزي إلى استعادة أكبر للمعلومات المتكاملة مقارنة بإثارة نواة مجاورة ضابطة، مما يعكس تجارب الحيوانات.
ماذا يعني ذلك للوعي والانتعاش
تشير هذه الخطوط المتقاربة من الأدلة إلى قصة مشتركة: في أدمغة الثدييات، تعمل أدوية التخدير المتنوعة، بشكل مباشر أو غير مباشر، على الدوائر المثبطة المعلمة بجين PVALB لتجعل النشاط واسع النطاق أصعب في التحكم وأقل تكاملًا. عندما يفشل هذا التكامل، يعجز الدماغ عن خياطة الإشارات الواردة إلى حالة موحدة ومستجيبة، فيتلاشى الوعي. يمكن لتحفيز المهاد المركزي المستهدف بعناية أن يعكس هذه العملية جزئيًا. بخلاف توضيح كيفية عمل التخدير، تقترح هذه النتائج استراتيجيات جديدة لاستعادة الوعي لدى مرضى إصابات الدماغ الشديدة، باستخدام خرائط توصيل الدماغ وتعبير الجينات للتنبؤ بالمناطق الأفضل لتحفيزها لإعادة إحياء الديناميكيات المتكاملة التي تدعم التجربة الواعية.
الاستشهاد: Luppi, A.I., Uhrig, L., Tasserie, J. et al. Convergent transcriptomic and connectomic controllers of information integration and its anaesthetic breakdown across mammalian brains. Nat Hum Behav 10, 777–802 (2026). https://doi.org/10.1038/s41562-025-02381-5
الكلمات المفتاحية: الوعي, التخدير, شبكات الدماغ, دمج المعلومات, تحفيز المهاد