Clear Sky Science · es
Controladores transcriptómicos y conectómicos convergentes de la integración de la información y su colapso por anestesia en cerebros de mamíferos
Por qué importa para cerebros cotidianos
Cuando te adormeces bajo anestesia general, tu conciencia del mundo desaparece aunque el cerebro siga físicamente intacto. Este estudio plantea una pregunta simple pero profunda: ¿qué cambia realmente dentro del cerebro en ese momento, y ese cambio es común entre mamíferos y fármacos muy distintos? Al combinar neuroimagen, genética y modelos computacionales en humanos, macacos y ratones, los autores identifican mandos comunes que parecen gobernar qué tan bien el cerebro entreteje la información en una experiencia consciente coherente.
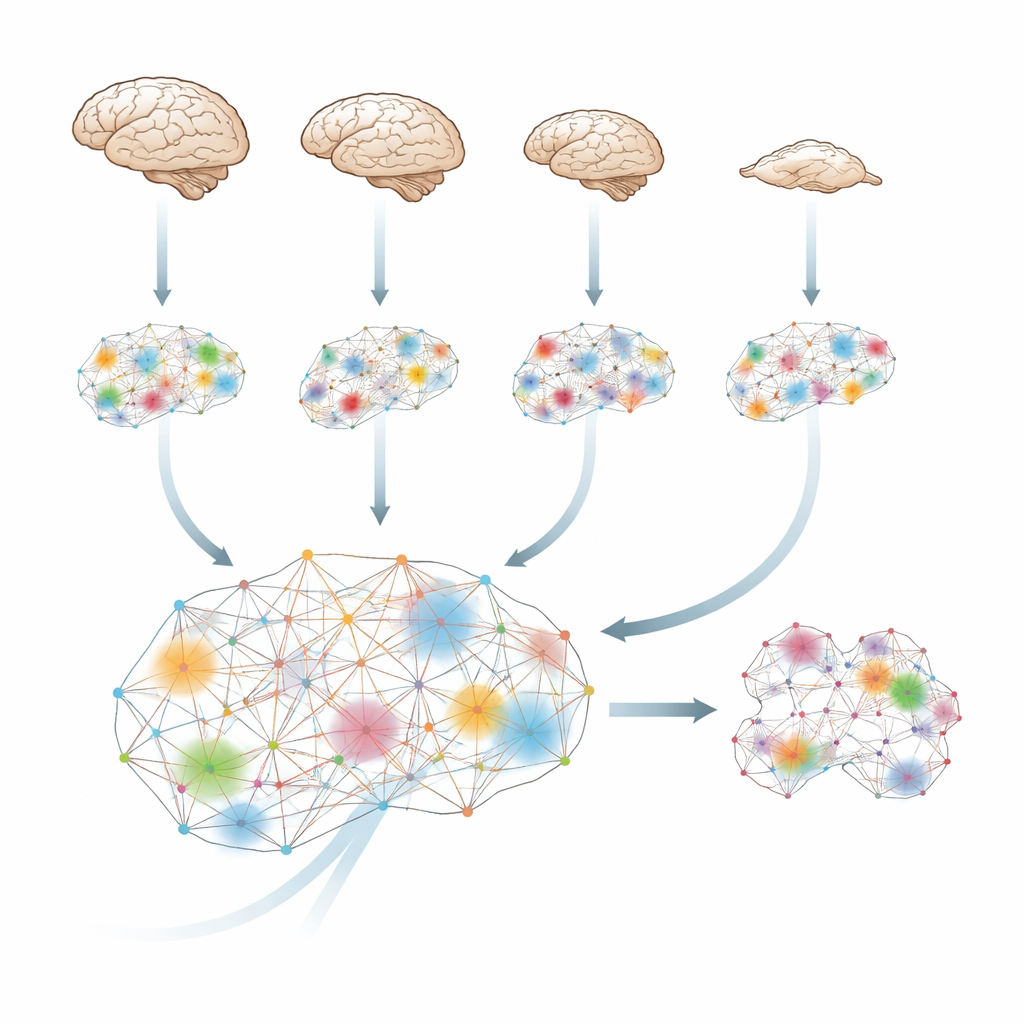
Cómo el cerebro teje la información en un todo
El cerebro predice y actualiza constantemente, de modo que lo que ocurre en el momento siguiente depende en parte de lo que ocurrió antes. Usando herramientas de la teoría de la información, los investigadores cuantifican cuánta «información extra» emerge cuando las regiones cerebrales cooperan, más allá de lo que cada región aporta por sí sola. Lo llaman información integrada: una medida de cuánto las distintas partes del cerebro actúan como un sistema único y coordinado en lugar de islas aisladas o simples ecos unas de otras.
Qué hace la anestesia a través de las especies
El equipo analizó escáneres de resonancia funcional de cuatro especies —humanos, macacos, marmosets y ratones— mientras estaban despiertos y bajo distintos fármacos anestésicos. A pesar de las grandes diferencias en cerebros y fármacos, el patrón fue notablemente similar. Siempre que los animales perdían la capacidad de respuesta conductual, el nivel de información integrada a través del cerebro disminuía. En humanos, esta medida aumentó de nuevo cuando las personas despertaron espontáneamente tras sevoflurano. En macacos, la estimulación eléctrica de una región talámica central —en lo profundo del cerebro— restauró tanto el comportamiento como la información integrada aun cuando el fármaco seguía siendo administrado. Esto sugiere que el efecto central de la anestesia no es solo silenciar el cerebro, sino alterar su capacidad de combinar la información en un todo unificado, y que esta pérdida puede revertirse mediante estimulación dirigida.
Por qué la dinámica cerebral se vuelve más difícil de dirigir
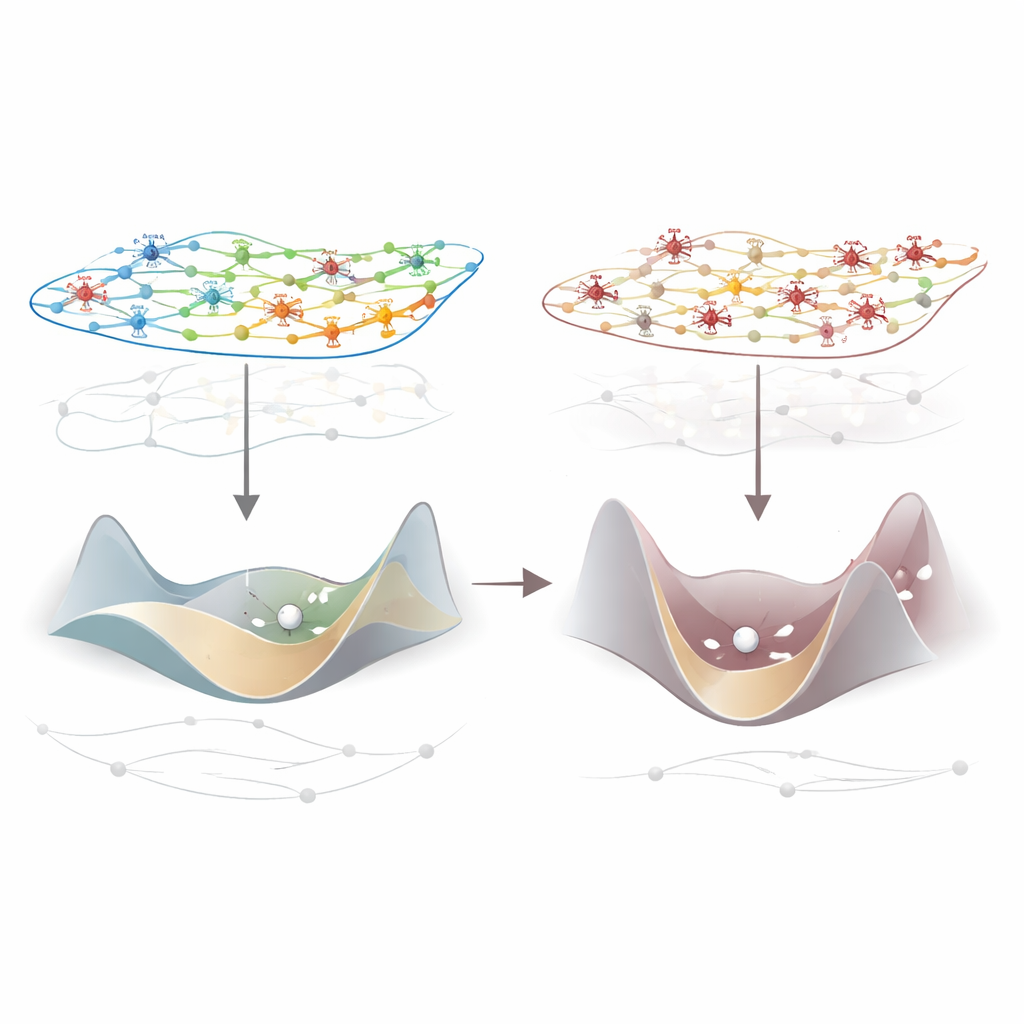
Para entender la mecánica detrás de este colapso, los autores recurrieron a la teoría del control de redes, que trata al cerebro como un sistema complejo que puede cambiar entre muchos patrones de actividad. Usando mapas de conexión específicos de cada especie sobre cómo están físicamente conectadas las regiones, calcularon cuánta «energía» haría falta para mover el cerebro de un patrón de actividad momentáneo al siguiente. Bajo anestesia, esta energía de control aumentó de forma consistente: el paisaje de estados cerebrales posibles se volvió más empinado y difícil de recorrer. Es importante que este endurecimiento de la dinámica se relajó cuando los sujetos despertaron o cuando la estimulación talámica restauró la capacidad de respuesta, y estuvo estrechamente ligado a la caída de la información integrada. En términos sencillos, cuando el cerebro es menos maniobrable, también pierde capacidad para integrar información.
Genes que ajustan los frenos locales de la actividad cerebral
No todas las regiones se vieron afectadas por igual. Las mayores pérdidas de integración aparecieron en áreas sensoriales y motoras primarias, aunque los cambios fueron generalizados. Para investigar por qué, los investigadores superpusieron estos patrones con mapas detallados de actividad génica en la corteza de humanos, macacos y ratones. Un gen destacó a través de las especies: PVALB, que marca una clase de interneuronas inhibitorias de acción rápida que actúan como frenos en los circuitos locales. Las regiones con mayor expresión de PVALB tendieron a mostrar caídas mayores de información integrada inducidas por la anestesia. En ratones, esas regiones también exhibieron los cambios más fuertes —ya fuesen aumentos o disminuciones— cuando se usaron anestesias más ligeras, lo que sugiere que las áreas ricas en PVALB son palancas especialmente potentes para remodelar el flujo de información.
Probar el mecanismo en cerebros virtuales
Para ir más allá de la correlación, el equipo construyó modelos computacionales de todo el cerebro inspirados en la biofísica para humanos, macacos y ratones, conectándolos con las conexiones anatómicas reales de cada especie. Luego aumentaron la inhibición en cada región del modelo según su nivel de PVALB. En las tres especies, esta manipulación redujo la información integrada en la actividad simulada más que cualquier patrón aleatorio de inhibición, y elevó la energía de control necesaria para moverse entre estados, tal como hacen las anestesias reales. En un modelo separado de macaco añadieron regiones talámicas y simularon la estimulación: excitar el tálamo central produjo una recuperación de la información integrada mucho mayor que la excitación de un núcleo de control cercano, reflejando los experimentos en animales.
Qué significa para la conciencia y la recuperación
En conjunto, estas líneas convergentes de evidencia apuntan a una historia común: en cerebros de mamíferos, fármacos anestésicos diversos actúan, directa o indirectamente, sobre circuitos inhibitorios marcados por el gen PVALB para hacer que la actividad a gran escala sea más difícil de controlar y menos integrada. Cuando esa integración falla, el cerebro ya no puede ensamblar las señales entrantes en un estado unificado y receptivo, y la conciencia se desvanece. La estimulación cuidadosamente dirigida del tálamo central puede revertir parcialmente este proceso. Más allá de explicar cómo funciona la anestesia, estos hallazgos sugieren nuevas estrategias para restaurar la conciencia en pacientes con lesiones cerebrales graves, usando mapas de conectividad y expresión génica para predecir las mejores regiones a estimular y reavivar las dinámicas integradas que sustentan la experiencia consciente.
Cita: Luppi, A.I., Uhrig, L., Tasserie, J. et al. Convergent transcriptomic and connectomic controllers of information integration and its anaesthetic breakdown across mammalian brains. Nat Hum Behav 10, 777–802 (2026). https://doi.org/10.1038/s41562-025-02381-5
Palabras clave: conciencia, anestesia, redes cerebrales, integración de la información, estimulación talámica