Clear Sky Science · ru
Конвергентные транскриптомные и коннектомные регуляторы интеграции информации и её анастетическая дезинтеграция в мозгах млекопитающих
Почему это важно для обычных мозгов
Когда вы погружаетесь в общую анестезию, ваше восприятие мира исчезает, хотя мозг остаётся физически целым. В этом исследовании поставлен простой, но глубинный вопрос: что именно меняется в мозге в этот момент, и повторяется ли это изменение у очень разных млекопитающих и при разных препаратах? Объединив данные МРТ, генетику и компьютерные модели у людей, макак и мышей, авторы выявляют общие «ручки управления», которые, по-видимому, определяют, насколько мозг умеет связывать информацию в связный опыт сознания.
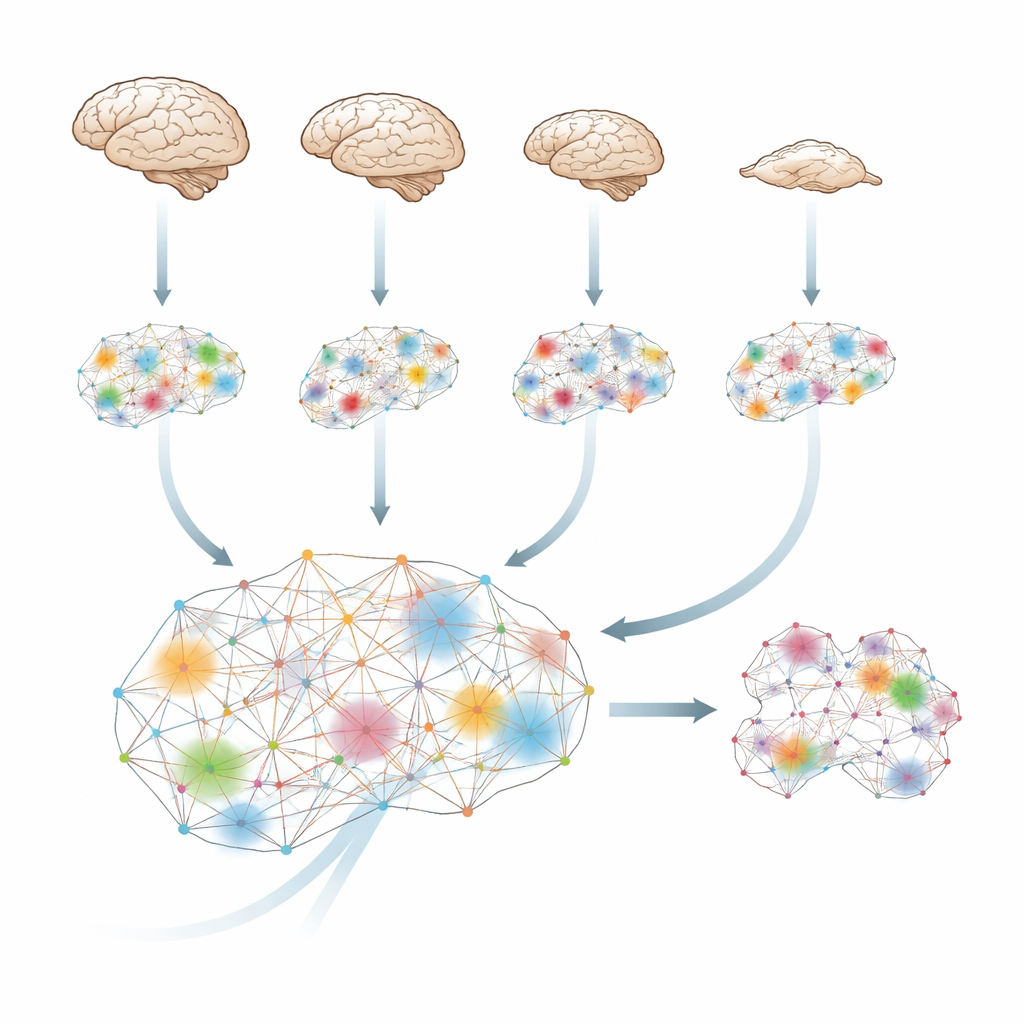
Как мозг сплетает информацию в целое
Мозг постоянно предсказывает и обновляет состояние, поэтому то, что произойдёт в следующий момент, частично зависит от предшествующего. С помощью инструментов теории информации исследователи количественно оценили, сколько «дополнительной» информации возникает, когда области мозга работают вместе, сверх того, что содержит каждая отдельная область. Они называют это интегрированной информацией: мерой того, насколько разные части мозга действуют как единая, скоординированная система, а не как изолированные острова или простые эхо друг друга.
Что делает анестезия у разных видов
Команда проанализировала функциональные снимки МРТ у четырёх видов — людей, макак, мармозеток и мышей — в состоянии бодрствования и под действием разных анестетиков. Несмотря на большие различия в мозгах и в препаратах, паттерн оказался поразительно схожим. Каждый раз, когда животные теряли поведенческую отзывчивость, уровень интегрированной информации в мозге падал. У людей эта величина поднималась обратно по мере самопроизвольного пробуждения от севофлурана. У макак электрическая стимуляция центральной таламической области — глубоко в мозге — восстанавливала и поведение, и интегрированную информацию, даже пока препарат продолжал вводиться. Это указывает на то, что основное действие анестезии — не просто глушение мозга, а нарушение его способности объединять информацию в единое целое, и эту утрату можно частично обратить с помощью целенаправленной стимуляции.
Почему динамику мозга становится труднее управлять
Чтобы понять механику этого срыва, авторы обратились к теории управления сетями, которая рассматривает мозг как сложную систему, способную переходить между множеством паттернов активности. Используя видоспецифические карты анатомических связей между областями, они рассчитали, сколько «энергии» потребовалось бы, чтобы переместить мозг из одного текущего паттерна активности в другой. Под анестезией эта управляющая энергия систематически возрастала: ландшафт возможных состояний мозга становился круче и труднее для обхода. Важно, что это «ужесточение» динамики ослабевало при пробуждении субъектов или при восстановлении отзывчивости после стимуляции таламуса и было тесно связано с падением интегрированной информации. Проще говоря, когда мозг становится менее управляемым, он также хуже интегрирует информацию.
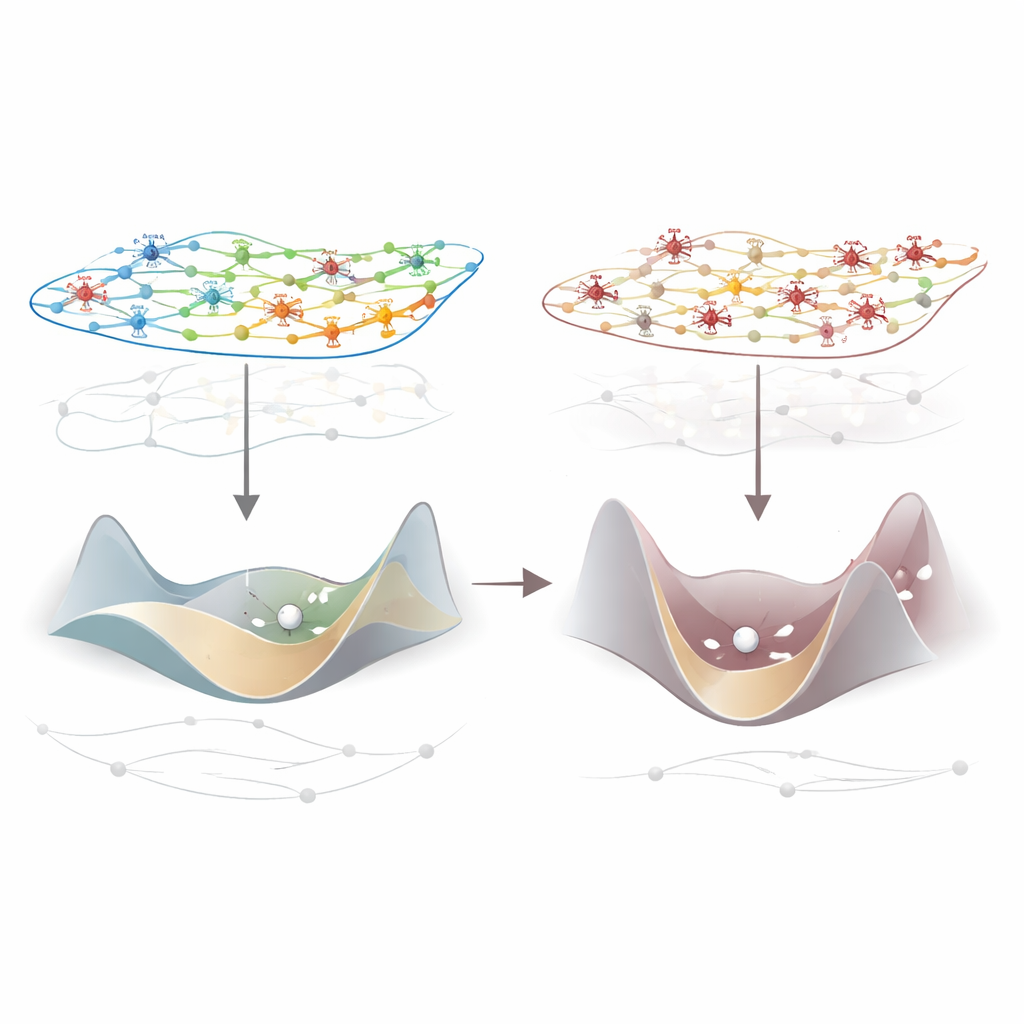
Гены, регулирующие местные «тормоза» активности мозга
Не все области страдали одинаково. Наибольшие потери интеграции наблюдались в первичных сенсорных и моторных зонах, но изменения были широко распространены. Чтобы понять причину, исследователи сопоставили эти паттерны с картами экспрессии генов в коре человека, макаки и мыши. Один ген выделялся во всех видах: PVALB, метка класса быстро действующих тормозных интернейронов, которые «подводят тормоза» к локальным цепям. Области с более высокой экспрессией PVALB, как правило, демонстрировали более сильные падения интеграции под действием анестезии. У мышей эти же области показывали наибольшие изменения — как в сторону увеличения, так и уменьшения — при более лёгкой анестезии, что указывает на то, что регионы, богатые PVALB, особенно эффективно перекраивают потоки информации.
Проверка механизма в виртуальных мозгах
Чтобы выйти за рамки корреляции, команда построила биофизически обоснованные модели целого мозга для людей, макак и мышей, подключив их по реальным анатомическим связям каждого вида. Затем они усиливали торможение в каждой области модели в соответствии с уровнем PVALB. Во всех трёх видах такая манипуляция снижала интегрированную информацию в смоделированной активности больше, чем любой случайный профиль торможения, и повышала энергию управления, необходимую для перехода между состояниями — точно так же, как это делают реальные анестетики. В отдельной модели макаки добавление таламических областей и моделирование стимуляции показало: возбуждение центрального таламуса восстанавливало интегрированную информацию гораздо сильнее, чем возбуждение близкого контрольного ядра, что повторяет результаты эксперимента на животных.
Что это значит для сознания и восстановления
В совокупности эти сходящиеся доказательства указывают на общую картину: в мозгах млекопитающих разнообразные анестетики действуют прямо или косвенно на тормозные цепи, помеченные геном PVALB, делая крупномасштабную активность труднее контролировать и менее интегрированной. Когда интеграция нарушается, мозг теряет способность сшивать входящие сигналы в единое отзывчивое состояние, и сознание угасает. Тщательно направленная стимуляция центрального таламуса может частично обратить этот процесс. Помимо объяснения механизмов анестезии, эти выводы предлагают новые стратегии восстановления сознания у пациентов с тяжёлыми повреждениями мозга: используя карты проводимости и экспрессии генов, можно прогнозировать лучшие области для стимуляции, чтобы вернуть интегрированную динамику, поддерживающую сознательный опыт.
Цитирование: Luppi, A.I., Uhrig, L., Tasserie, J. et al. Convergent transcriptomic and connectomic controllers of information integration and its anaesthetic breakdown across mammalian brains. Nat Hum Behav 10, 777–802 (2026). https://doi.org/10.1038/s41562-025-02381-5
Ключевые слова: сознание, анестезия, сетевые структуры мозга, интеграция информации, стимуляция таламуса