Clear Sky Science · de
Konvergente transkriptomische und konnektomische Steuerungen der Informationsintegration und ihres anästhetischen Zusammenbruchs über Säugetiergehirne hinweg
Warum das für alltägliche Gehirne wichtig ist
Wenn Sie unter einer Allgemeinanästhesie einschlafen, verschwindet Ihre Wahrnehmung der Welt, obwohl Ihr Gehirn physisch weiterhin intakt ist. Diese Studie stellt eine einfache, aber tiefgehende Frage: Was ändert sich in diesem Moment tatsächlich im Gehirn, und ist diese Veränderung bei sehr unterschiedlichen Säugetieren und Wirkstoffen ähnlich? Indem die Autoren Hirnscans, Genetik und Computermodelle bei Menschen, Makaken und Mäusen kombinieren, identifizieren sie gemeinsame Stellschrauben, die offenbar steuern, wie gut das Gehirn Informationen zu einer kohärenten bewussten Erfahrung zusammenfügt.
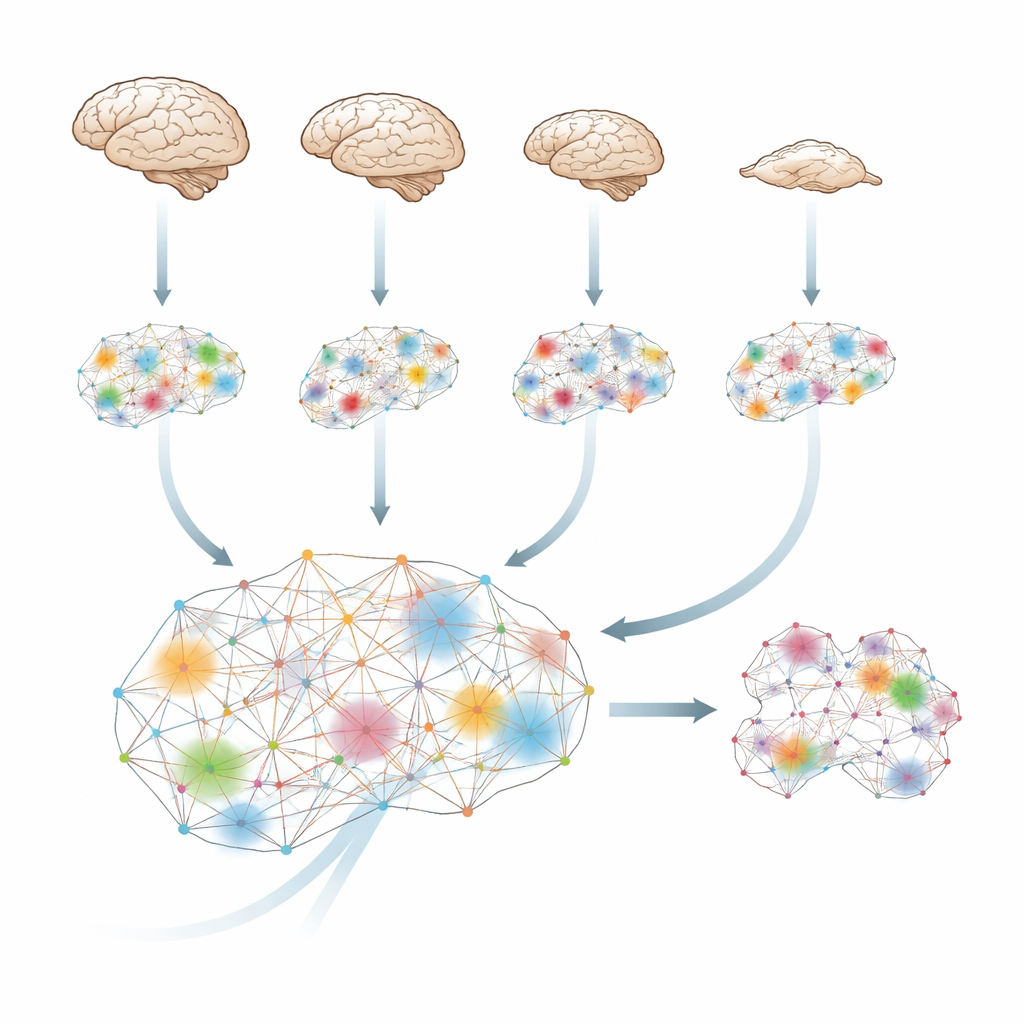
Wie das Gehirn Informationen zu einem Ganzen verwebt
Das Gehirn sagt ständig voraus und aktualisiert sich, sodass das, was im nächsten Moment passiert, teilweise von dem abhängt, was kurz zuvor geschah. Mit Werkzeugen aus der Informationstheorie quantifizieren die Forschenden, wie viel „zusätzliche“ Information entsteht, wenn Hirnregionen zusammenarbeiten, über das hinaus, was jede Region für sich allein liefert. Sie nennen dies integrierte Information: ein Maß dafür, wie stark verschiedene Teile des Gehirns als ein einziges, koordiniertes System wirken, statt als isolierte Inseln oder einfache Echos voneinander.
Was Anästhesie über Arten hinweg bewirkt
Das Team analysierte funktionelle MRT-Aufnahmen von vier Arten — Menschen, Makaken, Marmosetten und Mäusen — im wachen Zustand und unter verschiedenen anästhetischen Wirkstoffen. Trotz großer Unterschiede in Gehirnen und Wirkstoffen war das Muster auffallend ähnlich. Immer wenn die Tiere ihr Verhaltensansprechen verloren, sank das Niveau der integrierten Information im Gehirn. Beim Menschen stieg dieses Maß wieder an, als Personen spontan von Sevofluran aufwachten. Bei Makaken stellte elektrische Stimulation einer zentralen thalamischen Region — tief im Inneren des Gehirns — sowohl das Verhalten als auch die integrierte Information wieder her, obwohl das Medikament weiterhin verabreicht wurde. Das deutet darauf hin, dass die Kernauswirkung der Anästhesie nicht nur darin besteht, das Gehirn stumm zu schalten, sondern seine Fähigkeit zu stören, Informationen zu einem einheitlichen Ganzen zu verschmelzen, und dass dieser Verlust durch gezielte Stimulation umkehrbar ist.
Warum sich die Gehirndynamik schlechter steuern lässt
Um die Mechanik hinter diesem Zusammenbruch zu verstehen, griffen die Autorinnen und Autoren auf die Netzwerktontrolle zurück, die das Gehirn als komplexes System betrachtet, das zwischen vielen Aktivitätsmustern wechseln kann. Anhand artspezifischer Leitungsnetze der physischen Verbindungen zwischen Regionen berechneten sie, wie viel „Energie“ nötig wäre, um das Gehirn von einem momentanen Aktivitätsmuster zum nächsten zu bewegen. Unter Anästhesie stieg diese Kontrollenergie konsequent an: die Landschaft möglicher Gehirnzustände wurde steiler und schwerer zu durchqueren. Wichtig ist, dass diese Versteifung der Dynamik sich wieder löste, als Probanden aufwachten oder thalamische Stimulation das Reagieren wiederherstellte, und dass sie eng mit dem Rückgang der integrierten Information verknüpft war. Einfach gesagt: Wenn das Gehirn weniger steuerbar ist, wird es auch weniger fähig, Information zu integrieren.
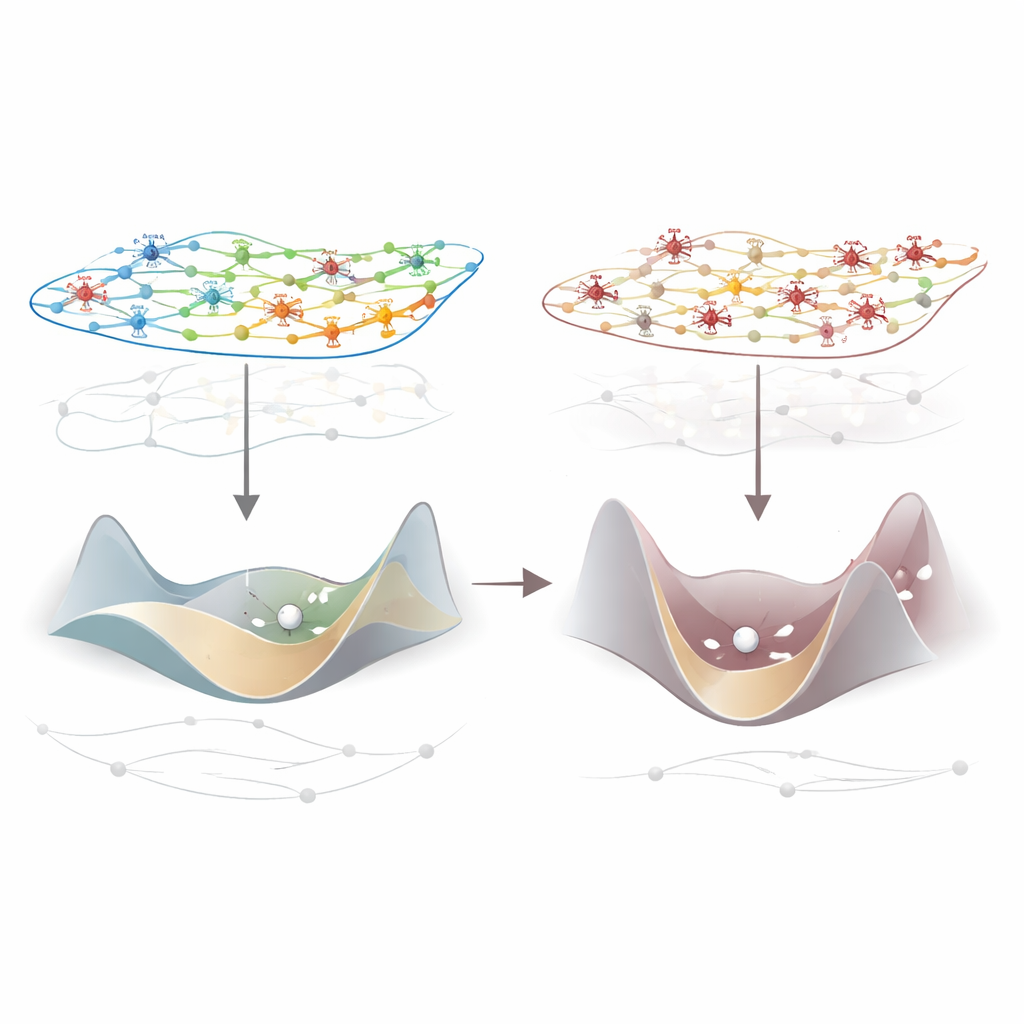
Gene, die lokale Bremsen der Hirnaktivität einstellen
Nicht alle Regionen waren gleichermaßen betroffen. Die größten Verluste an Integration zeigten sich in primären sensorischen und motorischen Arealen, doch waren die Veränderungen weit verbreitet. Um der Ursache nachzugehen, überlagerten die Forschenden diese Muster mit detaillierten Karten der Genaktivität im Kortex von Menschen, Makaken und Mäusen. Ein Gen hob sich über die Arten hinweg hervor: PVALB, das eine Klasse schnell wirkender inhibitorischer Interneurone kennzeichnet, die lokale Schaltkreise abbremsen. Regionen mit stärkerer PVALB-Expression zeigten tendenziell größere anästhesiebedingte Einbrüche der integrierten Information. Bei Mäusen zeigten diese Regionen außerdem die stärksten Änderungen — ob Zunahmen oder Abnahmen — bei leichterer Anästhesie, was nahelegt, dass PVALB-reiche Areale besonders wirkungsvolle Hebel sind, um den Informationsfluss umzulenken.
Testen des Mechanismus in virtuellen Gehirnen
Um über Korrelation hinauszukommen, bauten die Forschenden biophysikalisch inspirierte Ganzhirn-Computermodelle für Menschen, Makaken und Mäuse und verdrahteten sie mit den tatsächlichen anatomischen Verbindungen der jeweiligen Art. Sie erhöhten dann die Inhibition in jedem Modellgebiet entsprechend dessen PVALB-Level. In allen drei Arten reduzierte diese Manipulation die integrierte Information in der simulierten Hirnaktivität stärker als jede zufällige Verteilung von Inhibition und erhöhte die Kontrollenergie, die benötigt wird, um zwischen Zuständen zu wechseln — genau wie echte Anästhetika. In einem separaten Makakenmodell fügten sie thalamische Regionen hinzu und simulierten Stimulation: Die Anregung des zentralen Thalamus produzierte eine deutlich größere Wiederherstellung der integrierten Information als die Anregung eines nahegelegenen Kontrollkernes, was die Tierexperimente widerspiegelt.
Was das für Bewusstsein und Wiedererlangung bedeutet
Zusammen deuten diese konvergenten Befunde auf eine gemeinsame Geschichte hin: In Säugetiergehirnen wirken verschiedene anästhetische Wirkstoffe, direkt oder indirekt, auf inhibitorische Schaltkreise, die durch das PVALB-Gen markiert sind, und machen großräumige Aktivität schwerer kontrollierbar und weniger integriert. Wenn diese Integration versagt, kann das Gehirn eingehende Signale nicht mehr zu einem einheitlichen, reaktionsfähigen Zustand verweben, und das Bewusstsein schwindet. Gezielt eingesetzte Stimulation des zentralen Thalamus kann diesen Prozess teilweise umkehren. Über die Erklärung der Wirkungsweise von Anästhesie hinaus legen diese Ergebnisse neue Strategien nahe, um Bewusstsein bei Patientinnen und Patienten mit schweren Hirnverletzungen wiederherzustellen: mithilfe von Leitungsnetzen und Genexpressionskarten ließe sich vorhersagen, welche Regionen am besten zu stimulieren sind, um die integrierten Dynamiken zu reaktivieren, die bewusste Erfahrung stützen.
Zitation: Luppi, A.I., Uhrig, L., Tasserie, J. et al. Convergent transcriptomic and connectomic controllers of information integration and its anaesthetic breakdown across mammalian brains. Nat Hum Behav 10, 777–802 (2026). https://doi.org/10.1038/s41562-025-02381-5
Schlüsselwörter: Bewusstsein, Anästhesie, Gehirnnetzwerke, Informationsintegration, thalamische Stimulation