Clear Sky Science · sv
Konvergenta transkriptomiska och konektomiska styrmekanismer för informationsintegration och dess anestetiska kollaps över däggdjurshjärnor
Varför detta är viktigt för vardagliga hjärnor
När du somnar in under generell anestesi försvinner din medvetenhet om omvärlden även om din hjärna fortfarande är fysiskt intakt. Denna studie ställer en enkel men djup fråga: vad förändras egentligen inne i hjärnan i det ögonblicket, och delas den förändringen av mycket olika däggdjur och läkemedel? Genom att kombinera hjärnavbildning, genetik och datormodeller i människor, makaker och möss identifierar författarna gemensamma kontrollreglage som verkar styra hur väl hjärnan väver ihop information till en sammanhållen medveten upplevelse.
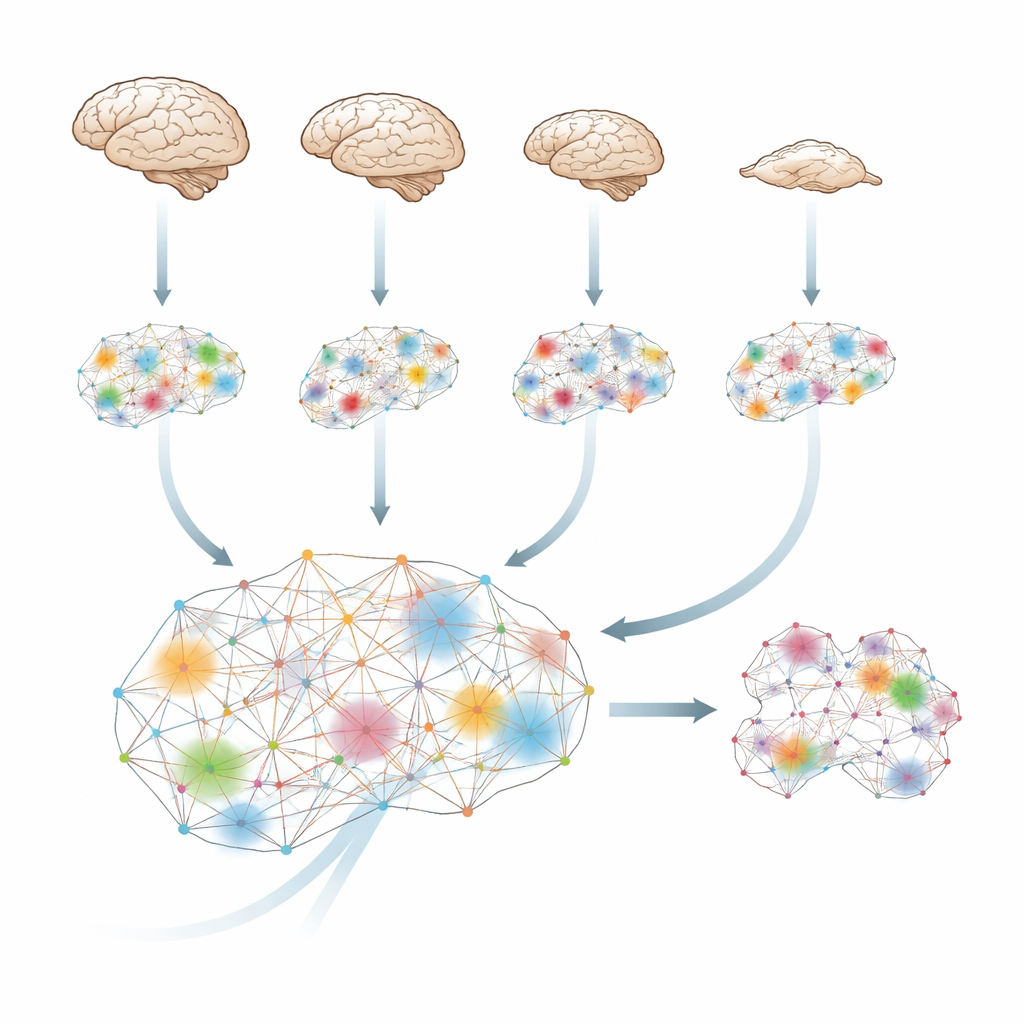
Hur hjärnan väver information till en helhet
Hjärnan förutspår och uppdaterar ständigt, så vad som händer i nästa ögonblick beror delvis på vad som just skedde. Med verktyg från informationsteori kvantifierar forskarna hur mycket "extra" information som uppstår när hjärnregioner samarbetar, utöver vad varje region bär upp ensam. De kallar detta integrerad information: ett mått på hur starkt olika delar av hjärnan agerar som ett enda koordinerat system snarare än som isolerade öar eller enkla eko av varandra.
Vad anestesi gör över arter
Teamet analyserade funktionella magnetröntgenbilder från fyra arter — människor, makaker, marmosetter och möss — medan de var vakna och under en rad anestetiska läkemedel. Trots stora skillnader i hjärnor och i läkemedel var mönstret anmärkningsvärt likt. När djuren förlorade beteendemässig respons sjönk nivån av integrerad information över hjärnan. Hos människor steg detta mått tillbaka när personer spontant vaknade upp från sevofluran. Hos makaker återställde elektrisk stimulering av en central thalamisk region — djupt inne i hjärnan — både beteende och integrerad information även medan läkemedlet fortfarande tillfördes. Detta tyder på att anestesins kärneffekt inte bara är att tysta hjärnan, utan att rubba dess förmåga att sammanfoga information till en enhetlig helhet, och att denna förlust kan återvändas genom riktad stimulering.
Varför hjärndynamik blir svårare att styra
För att förstå mekaniken bakom denna kollaps vände sig författarna till nätverkskontrollteori, som behandlar hjärnan som ett komplext system som kan växla mellan många aktivitetsmönster. Med art-specifika kopplingskartor över hur regioner är fysiskt förbundna beräknade de hur mycket "energi" som skulle krävas för att föra hjärnan från ett momentan aktivitetsmönster till nästa. Under anestesi ökade denna styrenergi konsekvent: landskapet av möjliga hjärntillstånd blev brantare och svårare att korsa. Viktigt nog släppte denna förhårdnad i dynamiken igen när försökspersonerna vaknade eller när thalamisk stimulering återställde responsen, och det var starkt kopplat till fallet i integrerad information. Enkelt uttryckt: när hjärnan är mindre styrbar blir den också mindre kapabel att integrera information.
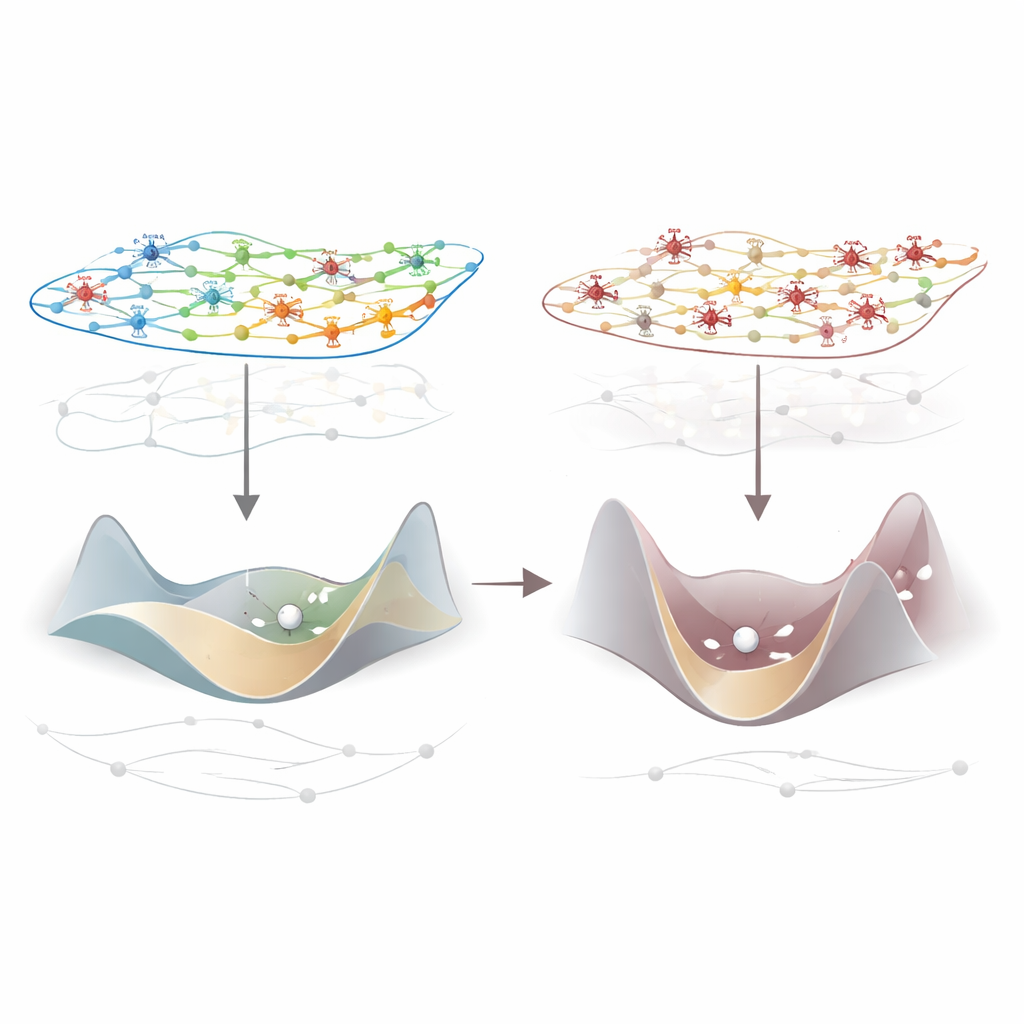
Gener som justerar lokala bromsar på hjärnaktivitet
Alla regioner påverkades inte lika mycket. De största förlusterna av integration syntes i primära sensoriska och motoriska områden, men förändringar förekom vida. För att ta reda på varför lade forskarna dessa mönster ovanpå detaljerade kartor över genaktivitet i människans, makakens och musens cortex. En gen stack ut över arterna: PVALB, som markerar en klass av snabbt verkande hämmande interneuroner som sätter bromsen på lokala kretsar. Regioner med starkare PVALB-uttryck tenderade att visa större anestesiinducerade fall i integrerad information. Hos möss visade dessa regioner också de starkaste förändringarna — vare sig ökningar eller minskningar — när lättare anestesi användes, vilket tyder på att PVALB-rika områden är särskilt effektfulla reglage för att omforma informationsflödet.
Testa mekanismen i virtuella hjärnor
För att gå bortom korrelation byggde teamet biofysiskt inspirerade helhjärnemodeller för människor, makaker och möss och kopplade dem med varje arts faktiska anatomiska förbindelser. De ökade därefter hämningen i varje modellregion i förhållande till dess PVALB-nivå. I samtliga tre arter minskade denna manipulation integrerad information i de simulerade hjärnaktiviteterna mer än någon slumpmässig fördelning av hämning, och den ökade den styrenergi som krävdes för att växla mellan tillstånd — precis som verkliga anestetika gör. I en separat makakmodell lade de till thalamiska regioner och simulerade stimulering: upphetsning av den centrala thalamus gav en mycket större återhämtning av integrerad information än upphetsning av en närliggande kontrollkärna, vilket speglade djurexperimenten.
Vad detta betyder för medvetande och återhämtning
Tillsammans pekar dessa konvergerande bevislinjer mot en gemensam berättelse: i däggdjurs hjärnor verkar olika anestetiska läkemedel, direkt eller indirekt, verka på hämmande kretsar markerade av PVALB-genen för att göra storskalig aktivitet svårare att kontrollera och mindre integrerad. När den integrationen misslyckas kan hjärnan inte längre sammanfoga inkommande signaler till ett enhetligt, responsivt tillstånd, och medvetandet försvinner. Noggrant riktad stimulering av den centrala thalamus kan delvis vända denna process. Utöver att förklara hur anestesi fungerar antyder dessa fynd nya strategier för att återställa medvetandet hos patienter med svåra hjärnskador, genom att använda kartor över hjärnkopplingar och genuttryck för att förutsäga de bästa regionerna att stimulera för att återväcka de integrerade dynamiker som stöder medvetna upplevelser.
Citering: Luppi, A.I., Uhrig, L., Tasserie, J. et al. Convergent transcriptomic and connectomic controllers of information integration and its anaesthetic breakdown across mammalian brains. Nat Hum Behav 10, 777–802 (2026). https://doi.org/10.1038/s41562-025-02381-5
Nyckelord: medvetande, anestesi, hjärn nätverk, informationsintegration, thalamisk stimulering