Clear Sky Science · fr
Contrôleurs transcriptomiques et connectomiques convergents de l’intégration de l’information et de sa rupture anesthésique à travers les cerveaux mammifères
Pourquoi cela importe pour des cerveaux ordinaires
Lorsque vous vous laissez aller sous anesthésie générale, votre conscience du monde disparaît alors que votre cerveau reste physiquement intact. Cette étude pose une question simple mais profonde : qu’est-ce qui change réellement à l’intérieur du cerveau à ce moment-là, et ce changement est‑il commun à des mammifères et des médicaments très différents ? En combinant imagerie cérébrale, génétique et modèles informatiques chez l’homme, le macaque et la souris, les auteurs découvrent des « boutons de commande » partagés qui semblent gouverner la capacité du cerveau à assembler les informations en une expérience consciente cohérente.
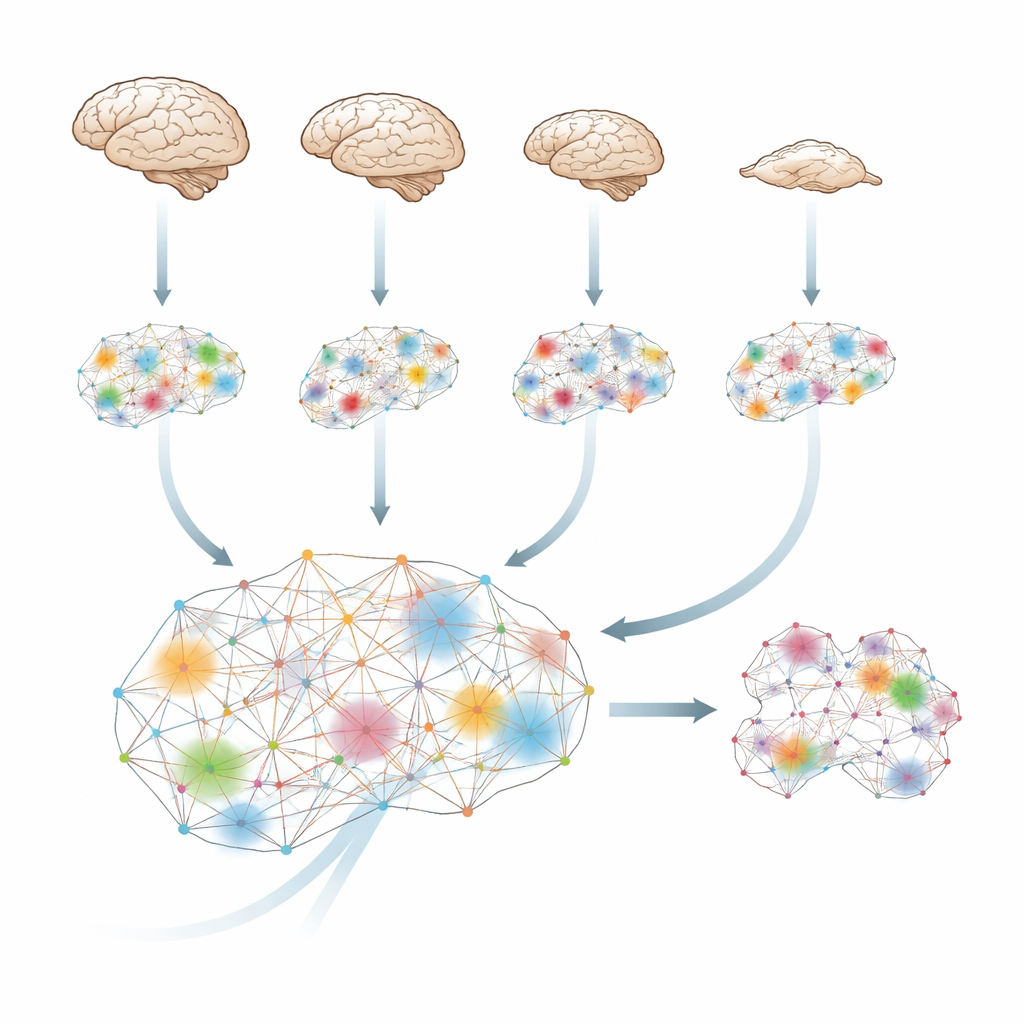
Comment le cerveau tisse l’information en un tout
Le cerveau prédit et met constamment à jour, de sorte que ce qui se passe au moment suivant dépend en partie de ce qui s’est passé juste avant. À l’aide d’outils de la théorie de l’information, les chercheurs quantifient combien d’« information supplémentaire » émerge quand des régions cérébrales travaillent ensemble, au‑delà de ce que chacune porte isolément. Ils appellent cela l’information intégrée : une mesure de la force avec laquelle différentes parties du cerveau fonctionnent comme un système coordonné unique plutôt que comme des îles isolées ou de simples échos les unes des autres.
Ce que fait l’anesthésie à travers les espèces
L’équipe a analysé des scans IRMf fonctionnels de quatre espèces — humains, macaques, marmosets et souris — alors qu’elles étaient éveillées et sous divers agents anesthésiques. Malgré de grandes différences de cerveaux et de médicaments, le schéma était remarquablement similaire. Chaque fois que les animaux perdaient la réactivité comportementale, le niveau d’information intégrée à l’échelle du cerveau diminuait. Chez l’homme, cette mesure remontait spontanément lors du réveil après le sevoflurane. Chez le macaque, une stimulation électrique d’une région thalamique centrale — en profondeur dans le cerveau — restaurait à la fois le comportement et l’information intégrée alors que le produit était encore perfusé. Cela suggère que l’effet fondamental de l’anesthésie n’est pas seulement de réduire l’activité, mais de perturber la capacité du cerveau à fusionner les informations en un tout unifié, et que cette perte peut être inversée par une stimulation ciblée.
Pourquoi la dynamique cérébrale devient plus difficile à piloter
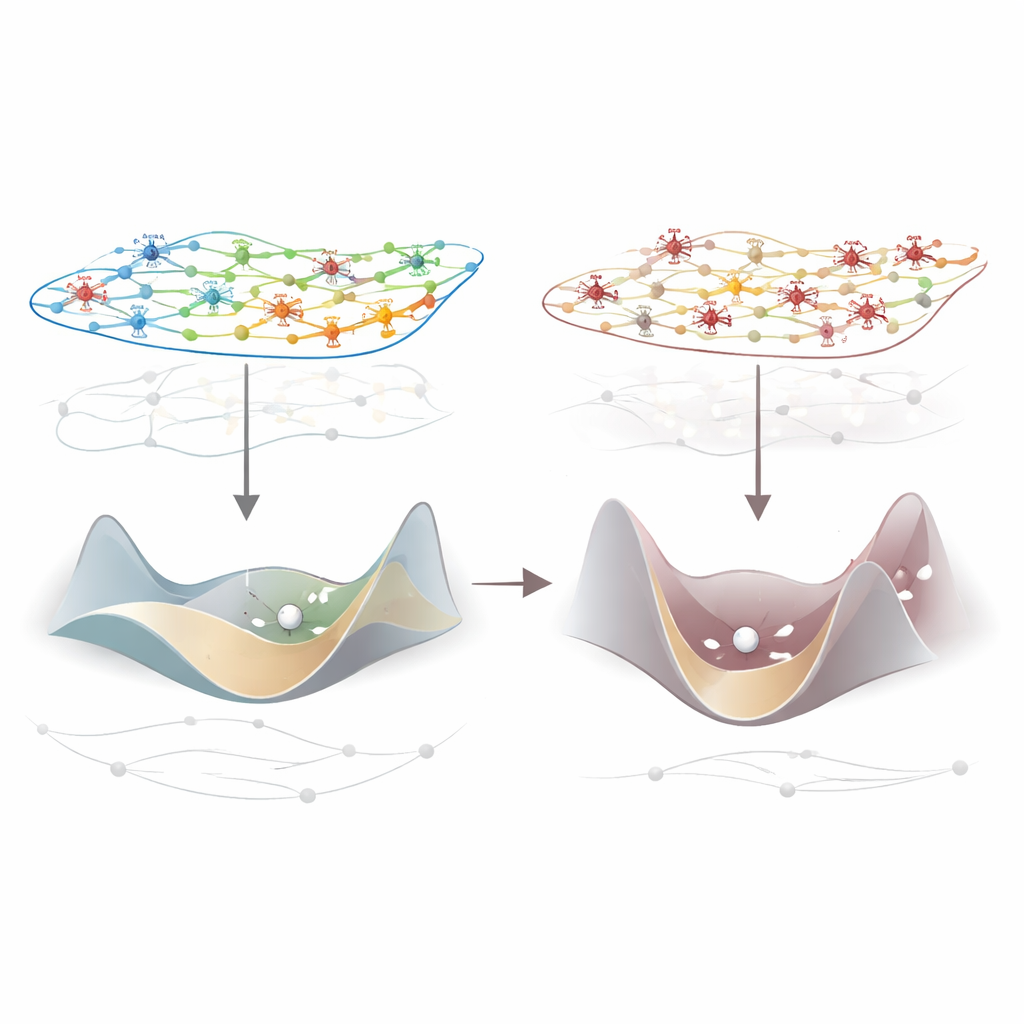
Pour comprendre les mécanismes de cette rupture, les auteurs se sont appuyés sur la théorie du contrôle des réseaux, qui considère le cerveau comme un système complexe capable de basculer entre de nombreux motifs d’activité. En utilisant des cartes de câblage propres à chaque espèce décrivant les connexions physiques entre régions, ils ont calculé quelle « énergie » serait nécessaire pour déplacer le cerveau d’un motif d’activité momentané au suivant. Sous anesthésie, cette énergie de contrôle augmentait systématiquement : le paysage des états cérébraux possibles devenait plus escarpé et plus difficile à parcourir. De manière importante, cet « raideissement » de la dynamique s’assouplissait à nouveau lorsque les sujets se réveillaient ou lorsque la stimulation thalamique rétablissait la réactivité, et il était étroitement lié à la chute de l’information intégrée. En termes simples, quand le cerveau est moins manœuvrable, il devient aussi moins capable d’intégrer l’information.
Gènes qui règlent les freins locaux de l’activité cérébrale
Toutes les régions n’étaient pas également affectées. Les pertes d’intégration les plus marquées apparaissaient dans les aires sensorielles et motrices primaires, mais les changements étaient étendus. Pour comprendre pourquoi, les chercheurs ont superposé ces motifs avec des cartes détaillées d’expression génique dans le cortex humain, macaque et souris. Un gène ressortait à travers les espèces : PVALB, qui marque une classe d’interneurones inhibiteurs à action rapide qui freinent les circuits locaux. Les régions avec une expression plus forte de PVALB avaient tendance à montrer des baisses d’information intégrée plus importantes sous anesthésie. Chez la souris, ces régions montraient aussi les changements les plus prononcés — qu’il s’agisse d’augmentations ou de diminutions — lorsque l’on utilisait une anesthésie plus légère, suggérant que les zones riches en PVALB sont des leviers particulièrement puissants pour remodeler le flux d’information.
Tester le mécanisme dans des cerveaux virtuels
Poursuivant au‑delà de la corrélation, l’équipe a construit des modèles informatiques biophysiquement inspirés du cerveau entier pour l’homme, le macaque et la souris, câblés avec les connexions anatomiques réelles de chaque espèce. Ils ont ensuite augmenté l’inhibition dans chaque région du modèle selon son niveau de PVALB. Dans les trois espèces, cette manipulation réduisait l’information intégrée dans l’activité simulée plus que n’importe quel motif aléatoire d’inhibition, et elle augmentait l’énergie de contrôle nécessaire pour passer d’un état à l’autre, comme le font les anesthésiques réels. Dans un modèle distinct de macaque, ils ont ajouté des régions thalamiques et simulé une stimulation : l’excitation du thalamus central produisait une récupération de l’information intégrée bien plus importante que l’excitation d’un noyau de contrôle voisin, reflétant les expériences animales.
Ce que cela implique pour la conscience et la récupération
Pris ensemble, ces éléments de preuve convergents racontent une histoire commune : chez les mammifères, des agents anesthésiques divers agissent, directement ou indirectement, sur des circuits inhibiteurs marqués par le gène PVALB pour rendre l’activité à grande échelle plus difficile à contrôler et moins intégrée. Lorsque cette intégration échoue, le cerveau ne peut plus tisser les signaux entrants en un état unifié et réactif, et la conscience s’estompe. Une stimulation ciblée du thalamus central peut partiellement inverser ce processus. Au‑delà d’expliquer le fonctionnement de l’anesthésie, ces résultats suggèrent de nouvelles stratégies pour restaurer la conscience chez des patients gravement atteints du cerveau, en utilisant les cartes de câblage et d’expression génique pour prédire les meilleures régions à stimuler afin de rééveiller les dynamiques intégrées qui soutiennent l’expérience consciente.
Citation: Luppi, A.I., Uhrig, L., Tasserie, J. et al. Convergent transcriptomic and connectomic controllers of information integration and its anaesthetic breakdown across mammalian brains. Nat Hum Behav 10, 777–802 (2026). https://doi.org/10.1038/s41562-025-02381-5
Mots-clés: conscience, anesthésie, réseaux cérébraux, intégration de l’information, stimulation thalamique