Clear Sky Science · pl
Zbieżne transkryptomiczne i konektomiczne regulatory integracji informacji oraz jej zanik pod wpływem znieczulenia we wszystkich mózgach ssaków
Dlaczego to ma znaczenie dla codziennych mózgów
Kiedy zapadasz w sen pod wpływem znieczulenia ogólnego, twoja świadomość świata zanika, choć mózg pozostaje fizycznie nienaruszony. To badanie stawia proste, lecz głębokie pytanie: co właściwie zmienia się w mózgu w tym momencie i czy ta zmiana jest podobna u bardzo różnych ssaków oraz przy różnych lekach? Łącząc obrazowanie mózgu, genetykę i modele komputerowe u ludzi, małp i myszy, autorzy odkrywają wspólne „pokrętła sterujące”, które wydają się regulować zdolność mózgu do scalania informacji w spójne świadome doświadczenie.
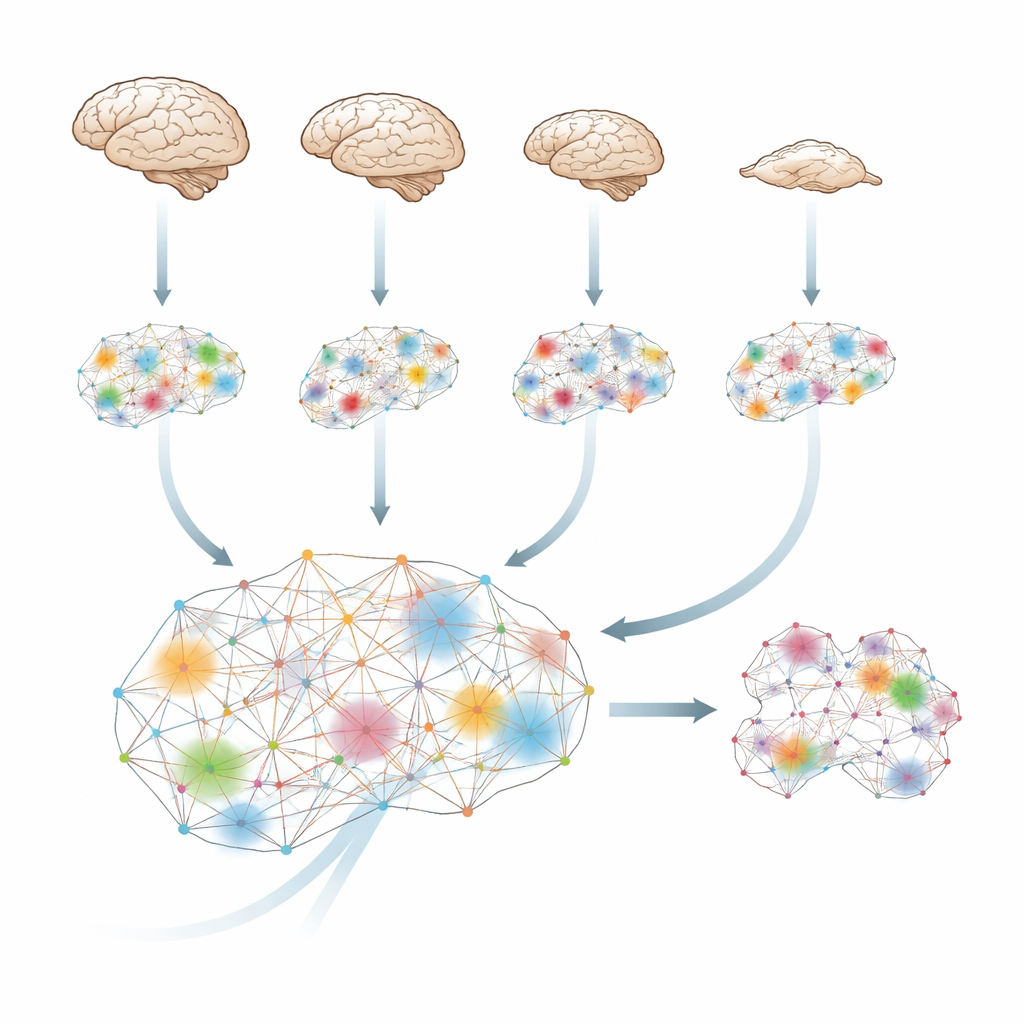
Jak mózg skleja informacje w całość
Mózg nieustannie przewiduje i aktualizuje, więc to, co stanie się w następnym momencie, zależy częściowo od tego, co wydarzyło się wcześniej. Korzystając z narzędzi teorii informacji, badacze mierzą, ile „dodatkowej” informacji pojawia się, gdy regiony mózgu współdziałają — ponad to, co każdy region niesie samodzielnie. Nazywają to zintegrowaną informacją: miarą, jak mocno różne części mózgu działają jako pojedynczy, skoordynowany system, a nie jako izolowane wyspy czy proste echa siebie nawzajem.
Co robi znieczulenie — wspólne cechy u różnych gatunków
Zespół przeanalizował skany fMRI functional od czterech gatunków — ludzi, makaków, marmozet i myszy — w stanie czuwania i pod różnymi lekami znieczulającymi. Pomimo dużych różnic w budowie mózgów i w stosowanych substancjach, wzorzec był uderzająco podobny. Za każdym razem, gdy zwierzęta traciły reakcję behawioralną, poziom zintegrowanej informacji w mózgu spadał. U ludzi ten wskaźnik ponownie rósł, gdy osoby spontanicznie budziły się po sewofluranie. U makaków elektryczna stymulacja centralnego regionu wzgórza — głęboko wewnątrz mózgu — przywracała zarówno zachowanie, jak i zintegrowaną informację, mimo że lek nadal był w infuzji. Sugeruje to, że podstawowy efekt znieczulenia nie polega jedynie na „wyciszeniu” mózgu, lecz na zakłóceniu jego zdolności do scalania informacji w jedną całość, a tę utratę można odwrócić poprzez celowaną stymulację.
Dlaczego dynamika mózgu staje się trudniejsza do sterowania
Aby zrozumieć mechanikę tego załamania, autorzy sięgnęli do teorii sterowania sieciowego, która traktuje mózg jako złożony system mogący przechodzić między wieloma wzorcami aktywności. Korzystając z map połączeń specyficznych dla każdego gatunku, obliczyli, ile „energii” byłoby potrzebne, aby przesunąć mózg z jednego chwilowego wzorca aktywności do następnego. Pod wpływem znieczulenia to zapotrzebowanie na sterowanie konsekwentnie wzrastało: krajobraz możliwych stanów mózgu stawał się bardziej stromy i trudniejszy do przemierzenia. Co ważne, to „usztywnienie” dynamiki ustępowało, gdy badani budzili się lub gdy stymulacja wzgórza przywracała reakcję, i było ściśle powiązane z spadkiem zintegrowanej informacji. Prościej: gdy mózg jest mniej sterowalny, traci też zdolność do integracji informacji.
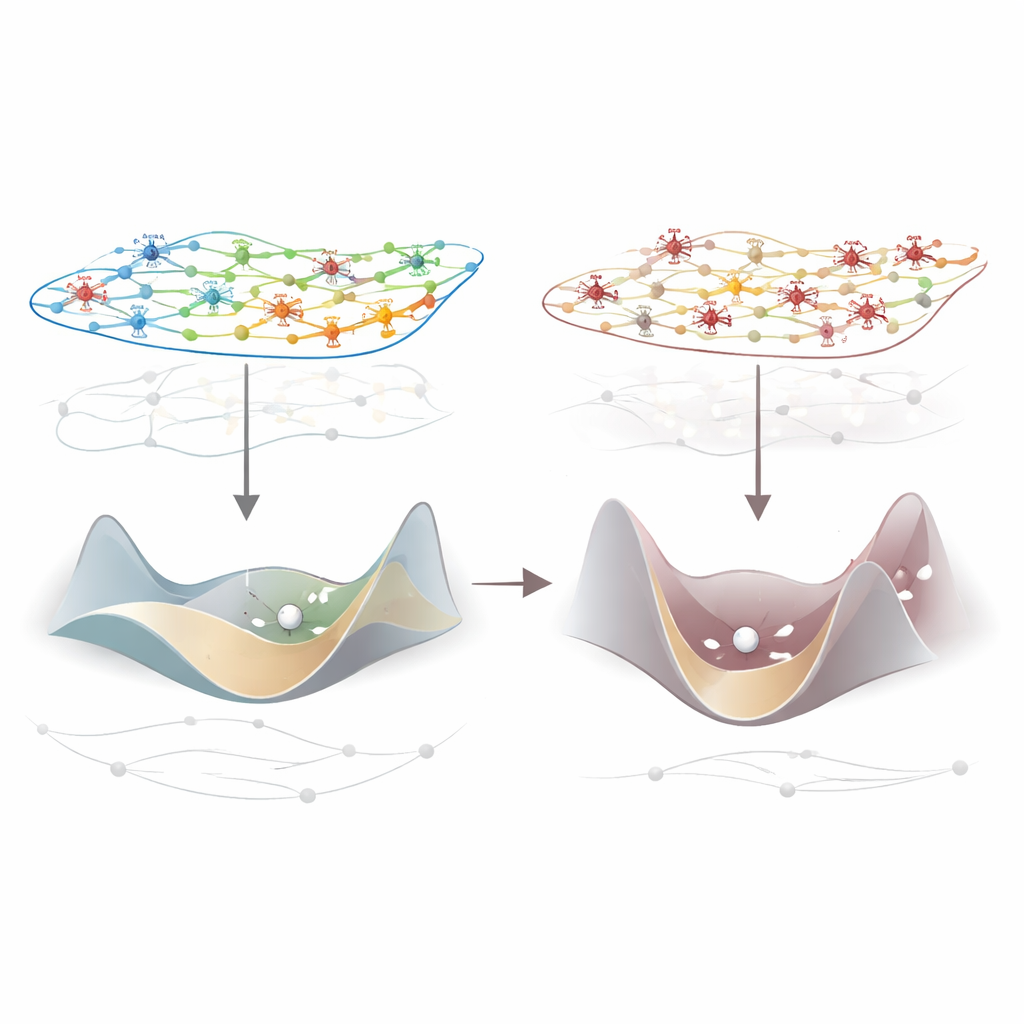
Geny regulujące lokalne hamulce aktywności mózgu
Nie wszystkie obszary były dotknięte jednakowo. Największe utraty integracji pojawiły się w pierwotnych obszarach sensorycznych i motorycznych, lecz zmiany występowały szeroko. Aby zrozumieć przyczyny, badacze zestawili te wzorce z detalicznymi mapami ekspresji genów w korze człowieka, makaka i myszy. Jeden gen wyróżniał się we wszystkich gatunkach: PVALB, który oznacza klasę szybko działających interneuronów hamujących, pełniących funkcję „hamulców” w lokalnych obwodach. Regiony o silniejszej ekspresji PVALB miały tendencję do większych spadków zintegrowanej informacji wywołanych znieczuleniem. U myszy te rejony także wykazywały najsilniejsze zmiany — zarówno wzrosty, jak i spadki — gdy stosowano lżejsze znieczulenie, co sugeruje, że obszary bogate w PVALB są szczególnie skutecznymi dźwigniami do przeobrażania przepływu informacji.
Testowanie mechanizmu w wirtualnych mózgach
Aby wyjść poza korelację, zespół zbudował biofizycznie inspirowane modele całego mózgu dla ludzi, makaków i myszy, łącząc je rzeczywistymi połączeniami anatomicznymi każdego gatunku. Następnie zwiększali hamowanie w każdym regionie modelu zgodnie z poziomem PVALB. We wszystkich trzech gatunkach ta manipulacja zmniejszała zintegrowaną informację w symulowanej aktywności mózgu bardziej niż dowolny losowy wzorzec hamowania, i podnosiła energię sterowania potrzebną do przejścia między stanami — tak jak czynią to rzeczywiste anestetyki. W odrębnym modelu makaka dodali regiony wzgórza i zasymulowali stymulację: pobudzenie centralnego wzgórza powodowało znacznie większy powrót zintegrowanej informacji niż pobudzenie pobliskiego jądra kontrolnego, co odzwierciedla eksperymenty na zwierzętach.
Co to znaczy dla świadomości i odzyskiwania
Wspólnie, te zbieżne linie dowodów wskazują na wspólną opowieść: w mózgach ssaków różne leki znieczulające działają, bezpośrednio lub pośrednio, na obwody hamujące oznaczone przez gen PVALB, czyniąc aktywność na dużą skalę trudniejszą do kontrolowania i mniej zintegrowaną. Gdy ta integracja zawodzi, mózg nie potrafi już sklejać napływających sygnałów w spójny, reaktywny stan i świadomość zanika. Precyzyjnie skierowana stymulacja centralnego wzgórza może częściowo odwrócić ten proces. Poza wyjaśnieniem mechanizmu działania znieczulenia, wyniki te sugerują nowe strategie przywracania świadomości u pacjentów z ciężkimi uszkodzeniami mózgu, wykorzystując mapy połączeń i ekspresji genów do przewidywania najlepszych regionów do stymulacji, by odnowić zintegrowaną dynamikę podtrzymującą doświadczenie świadome.
Cytowanie: Luppi, A.I., Uhrig, L., Tasserie, J. et al. Convergent transcriptomic and connectomic controllers of information integration and its anaesthetic breakdown across mammalian brains. Nat Hum Behav 10, 777–802 (2026). https://doi.org/10.1038/s41562-025-02381-5
Słowa kluczowe: świadomość, znieczulenie, sieci mózgowe, integracja informacji, stymulacja wzgórza