Clear Sky Science · zh
通过工程化共信号受体生成具有降低离靶交叉反应性的T细胞
将抗癌细胞打造成更精准的武器
工程化免疫细胞正在成为对抗癌症的强大工具,但它们有时会将健康组织误识为肿瘤,造成致命后果。这项研究探讨了一种新方法,使这些抗癌T细胞更具选择性——在猛烈攻击肿瘤的同时,尽可能忽略身体其他部位的相似靶点。
为什么离靶攻击如此危险
许多试验性疗法通过给予患者装配了定制受体的T细胞,这些受体能识别肿瘤细胞表面的短蛋白片段。挑战在于,每个T细胞受体原则上可以响应大量不同的片段,而不仅仅是目标肿瘤片段。在过去的临床试验中,这种交叉反应导致工程化T细胞攻击心脏或神经组织,造成致命副作用。当前的安全策略主要试图重新设计受体本身,这是一个繁琐的过程,需要针对每种新疗法重复进行,且容易引入新的、不可预见的风险。
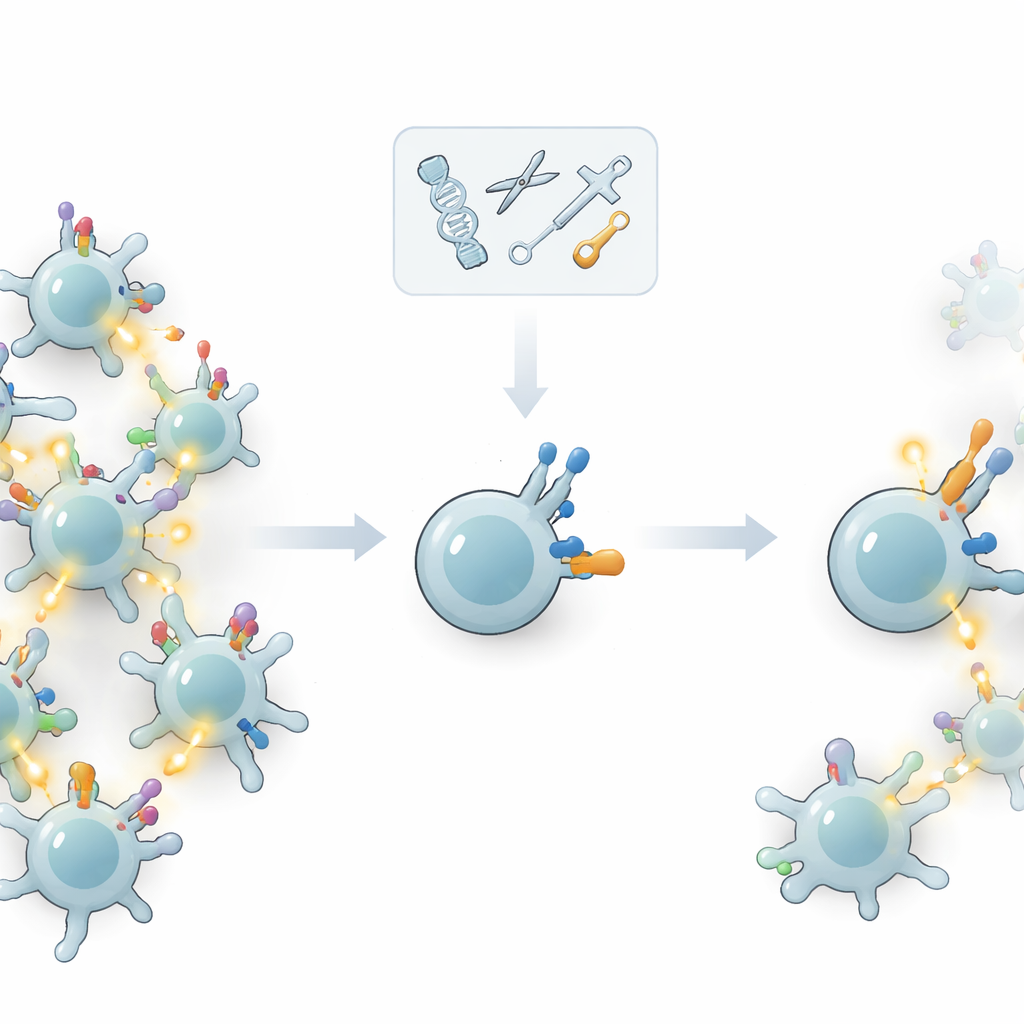
改造“辅助硬件”而不是传感器
作者没有去改动主要受体,而是探问是否可以调节控制T细胞在受体结合后反应强度的“辅助硬件”。T细胞表面携带附加分子——共受体和其他共信号蛋白——它们帮助设定激活阈值。通过使用基因编辑有选择地去除或添加这些分子,团队测试了T细胞如何区分结合强烈、很可能来自肿瘤的靶点与结合较弱、可能来自自身的靶点。他们的关键想法是提高细胞忽略低质量信号的能力,同时不削弱其对高质量信号的反应。
交换共受体以创造超选择性细胞
研究者集中研究了三种著名的共受体:CD8、CD4 和 CD5。他们发现,删除 CD5 会使T细胞更容易被多种靶点激活,可能增强抗肿瘤能力,但也扩大了交叉反应范围。相反,去除 CD8——一种通常帮助杀伤性T细胞识别靶点的分子——则效果相反:它显著降低了对弱结合肽的反应,同时保留了对强结合肿瘤肽的强烈反应。更进一步,研究团队在这些缺失 CD8 的杀伤性细胞中引入了 CD4(这是一种通常由另一类T细胞亚群使用的共受体)。这种“CD8→CD4 共受体转换”大幅提高了激活门槛,使得只有高亲和力的肿瘤靶点能触发完全杀伤,而各种较弱的离靶刺激基本被忽略。
在众多潜在靶点上检验安全性
为了验证这种更严格的选择性是否真实转化为更安全的行为,作者用几组逐步更接近现实的试验来挑战他们的工程化细胞。首先他们使用包含数千种随机肽的文库,其中大多数应当结合较弱。标准工程化T细胞会杀死许多呈递这些随机序列的细胞,显示出高度交叉反应。相比之下,缺失 CD8 的细胞,尤其是完成 CD8→CD4 转换的细胞,在相同条件下表现出明显更少的杀伤。接着,团队检查了已知肿瘤肽的单氨基酸变体的聚焦文库,并测量每个变体与受体的结合强度。再次证明,带有共受体转换的细胞忽略了许多仍能激活普通工程化T细胞的低亲和力变体。最后,他们测试了来自人体蛋白的、被预测并经实验证实能激活受体的自源肽。结果同样表明,转换后的细胞反应性远低于常规细胞,但在对原始高亲和力肿瘤靶点上仍保持强效。
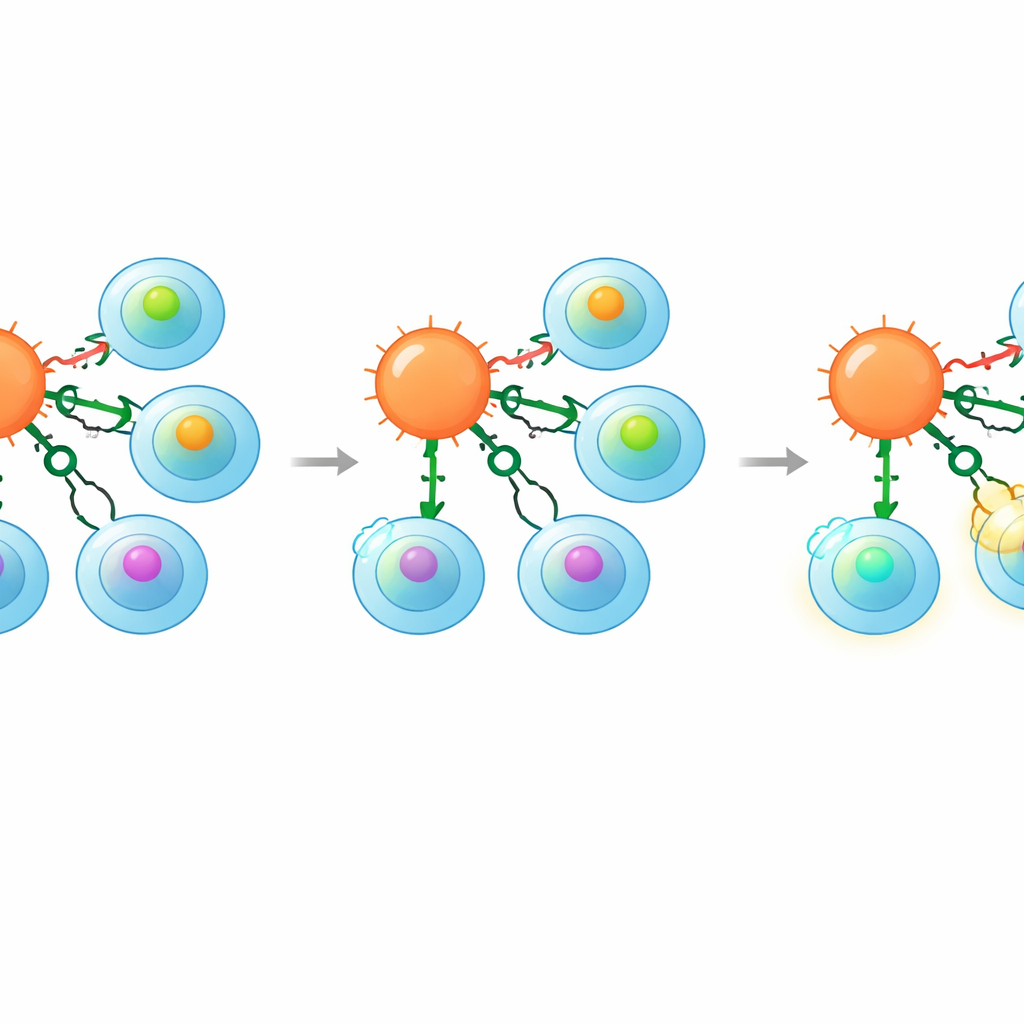
从过去的悲剧中吸取教训
研究者还回顾了一个在临床上具有重要警示意义的案例。早期一项试验使用携带针对癌症蛋白 MAGE‑A3 的受体的T细胞;这些细胞意外地也识别了来自心肌蛋白 Titin 的一个较弱肽段,导致致命的心脏损伤。在新工作中,作者展示了在携带相同受体的杀伤性T细胞中敲除 CD8 可彻底消除对 Titin 肽的反应,同时保留对实际表达 MAGE‑A3 的肿瘤细胞的攻击。这一示范表明,共受体工程可能有助于挽救那些因安全问题而被放弃的、有前景的受体。
这对未来癌症疗法意味着什么
从外行角度看,核心信息是研究团队通过调整内部连线而不是不断重设计“镜头”,找到了一种锐化免疫细胞“视野”的方法。通过切换T细胞上的辅助分子组合——特别是在受体与其癌症靶点强结合时移除 CD8 并添加 CD4——研究者创造了“超选择性”T细胞。这些细胞仍然能猛烈攻击肿瘤,但更不容易被呈现相似、较弱信号的正常组织所诱导去攻击。由于该方法不改变主受体序列,原则上可以广泛应用于多种不同的T细胞疗法,为更安全、更精确的癌症免疫治疗提供一条通用路线。
引用: Cabezas-Caballero, J., Huhn, A., Kutuzov, M.A. et al. Generation of T cells with reduced off-target cross-reactivities by engineering co-signalling receptors. Nat. Biomed. Eng 10, 753–764 (2026). https://doi.org/10.1038/s41551-025-01563-w
关键词: 癌症免疫疗法, T细胞工程, T细胞受体, 离靶毒性, 共受体转换