Clear Sky Science · he
ייצור תאי T עם צולבות תגובה ממוקדות פחות על‑ידי הנדסת קולטני סימון‑צדדי
הפיכת התאים הלוחמים בסרטן לכלי חד יותר
תאי חיסון מהונדסים מתגלים ככלי רב‑עוצמה נגד סרטן, אך לפעמים הם טועים ומזהים רקמות בריאות כלייצמן של הגידול — עם תוצאות קטלניות. המחקר הזה בוחן דרך חדשה להפוך את תאי ה‑T האלה לבעלי סלקטיביות גבוהה הרבה יותר, כך שיעברו על הגידולים באגרסיביות אך יתעלמו ברוב המקרים ממטרות דומות שמופיעות באזורים בריאים בגוף.
מדוע תקיפות עקיפות מסוכנות כל‑כך
טיפולים ניסיוניים רבים פועלים על ידי הענקת תאי T המצוידים בקולטנים מותאמים שמזהים קטעי חלבון קטנים על תאי הגידול. האתגר הוא שכל קולטן של תא T יכול, בהגיון, להגיב למספר עצום של קטעים שונים — לא רק לאלה המיועדים. בניסויים קליניים בעבר, צולבות תגובה כזו הובילה לתגובות של תאי ה‑T המהונדסים כנגד רקמות לב או עצב, וגרמה לתופעות לוואי קטלניות. אסטרטגיות הבטיחות הקיימות מנסות בעיקר לעצב מחדש את הקולטן עצמו — תהליך מורכב שצריך לחזור עליו לכל טיפול חדש ועלול להכניס סיכונים בלתי צפויים.
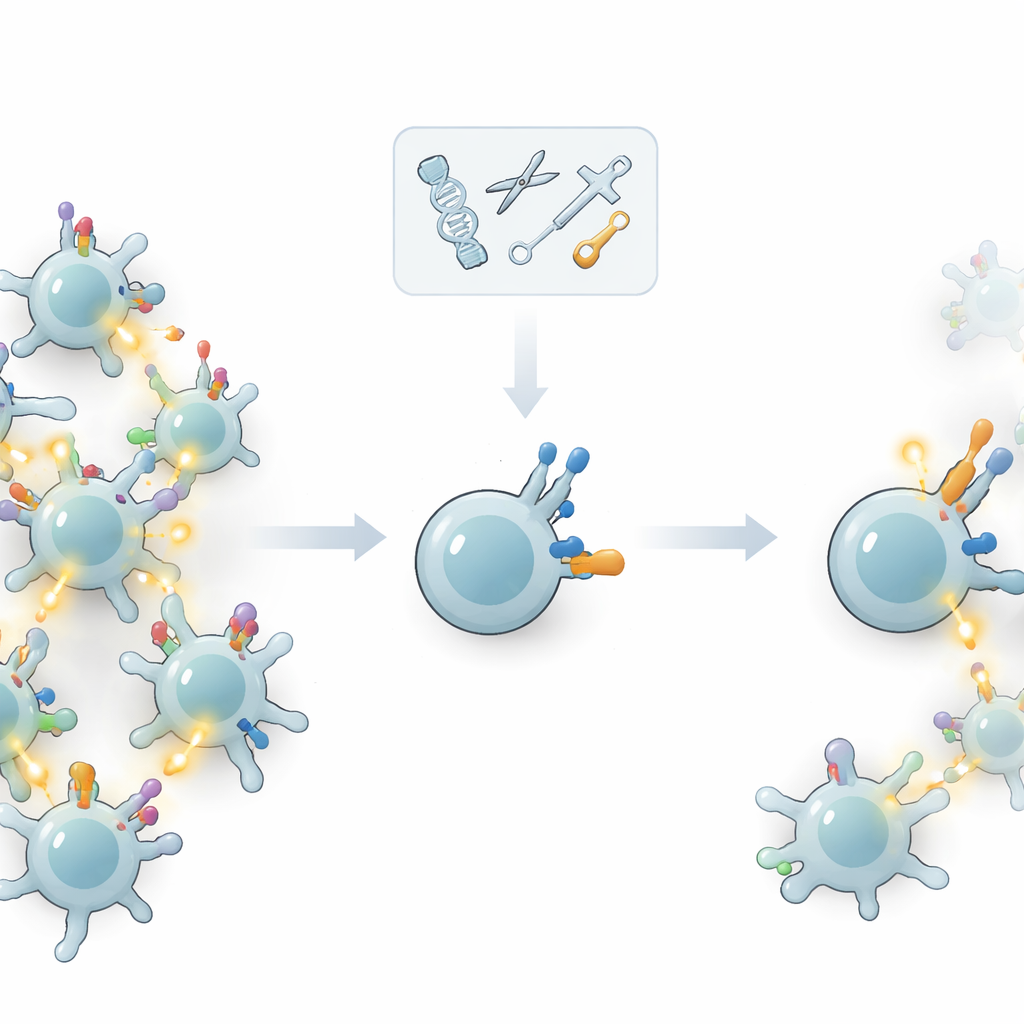
כיוונון הציוד התומך במקום החיישן
במקום לשנות את הקולטן הראשי, המחברים שאלו האם ניתן לכוונן את ה"ציוד התומך" שקובע עד כמה תא T מגיב לאחר שהקולטן קושר משהו. תאי T נושאים מולקולות נוספות על המשטח — קו‑קולטנים וחלבוני סימון‑צדדי אחרים — שמסייעים לקבוע את סף ההפעלה. על‑ידי הסרה או הוספה סלקטיבית של מולקולות אלה באמצעות עריכת גנים, הצוות בדק עד כמה תאים יודעים להבחין בין מטרות חזקות, סבירות להיות גידול, לבין מטרות חלשות שנגזרו מהגוף עצמו. הרעיון המרכזי היה לשפר את היכולת להתעלם מאותות באיכות נמוכה מבלי להחליש את התגובה לאותות באיכות גבוהה.
החלפת קו‑קולטנים ליצירת תאים סופר‑סלקטיביים
המחקרים התמקדו בשלושה קו‑קולטנים ידועים: CD8, CD4 ו‑CD5. הם מצאו כי מחיקת CD5 הקלה על הפעלת תאי ה‑T על ידי מטרות רבות שונות, מה שעשוי להגביר את כוח הנוגד‑הגידול אך גם להרחיב את הצולבות תגובה. לעומתם, הסרת CD8 — מולקולה שבדרך כלל מסייעת לתאי הקילר לזהות מטרות — השפיעה הפוכית: היא הקטינה בצורה חדה תגובות לפפטידים הקושרים בחוזקה חלשה, תוך שמירה על תגובות חזקות לפפטידים סרטניים הקושרים בחוזקה גבוהה. עוד צעד: הצוות הוסיף CD4 — קו‑קולטן שבדרך כלל קיים בתת‑סוג אחר של תאי T — לתאים קילרים מהם הוסר CD8. ה"החלפת CD8→CD4" זו העלתה באופן דרמטי את סף ההפעלה, כך שרק מטרות סרטניות בקשירה גבוהה גרמו להשמדה מלאה, בעוד מגוון רחב של גירויים חלשים יותר זוהו במידה קטנה או לא זוהו כלל.
בדיקת הבטיחות מול מגוון מטרות פוטנציאליות
כדי לבדוק האם הסלקטיביות המחמירה באמת מתרגמת להתנהגות בטוחה יותר, המחברים אתגרו את התאים המתהנדסים בסדרה של בדיקות מציאותיות יותר ויותר. תחילה הם השתמשו בספריות המכילות אלפי פפטידים אקראיים, שרובם אמורים לקשר בחוזקה חלשה. תאי ה‑T המהונדסים הרגילים השמידו תאים שהציגו רצפים אקראיים רבים, סימן לצולבות תגובה גבוהה. לעומת זאת, תאי KO ל‑CD8, ובמיוחד תאי ההחלפה CD8→CD4, הפגינו הרג מועט בהרבה בתנאים זהים. לאחר מכן בחנו את הספרייה הממוקדת של וריאנטים עם החלפה של חומצה אמינית אחת בפפטיד סרטני ידוע ומדדו עד כמה כל וריאנט קושר את הקולטן. שוב, התאים עם החלפת הקו‑קולטן התעלמו מהרבה וריאנטים בקשירה נמוכה שעדיין הפעילו תאי T מהונדסים רגילים. לבסוף, הם בדקו פפטידים עצמאיים צפויים מחלבונים אנושיים שאושרו לניסוי כפעילים; כאן גם תאי ההחלפה הראו תגובתיות נמוכה בהרבה, אך שמרו על עוצמה חזקה כנגד המטרה הסרטנית המקורית בקשירה גבוהה.
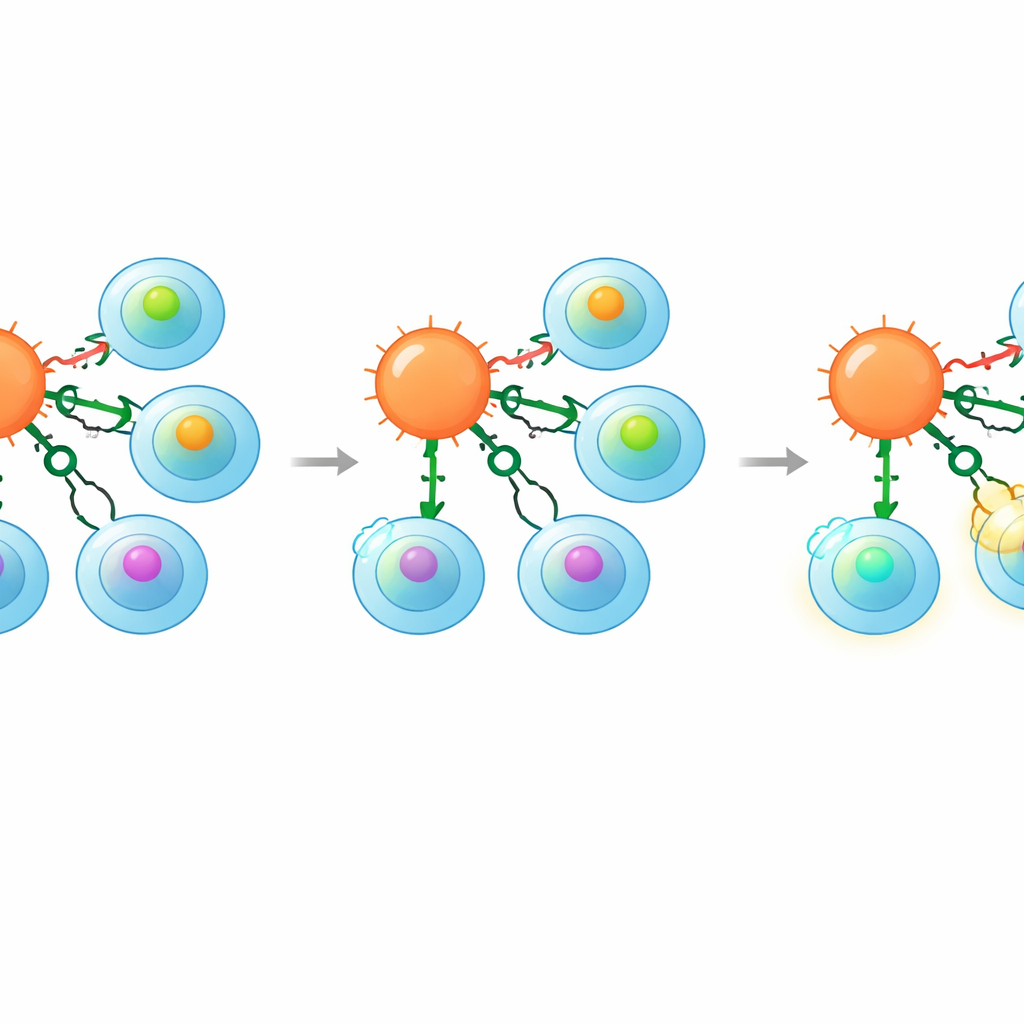
למידה מהטרגדיות של העבר
החוקרים גם חזרו על מקרה זהיר חשוב מבחינה קלינית. ניסוי קודם השתמש בתאי T שנשאו קולטן לחלבון סרטני בשם MAGE‑A3; אותם תאים זיהו באופן בלתי צפוי פפטיד חלש מחלבון שריר הלב Titin, מה שהוביל לנזק לבבי קטלני. בעבודה החדשה הראו המחברים כי ביטול CD8 בתאי קילר שנושאים את אותו קולטן ביטל את תגובתם לפפטיד Titin תוך שמירה על התקיפה של תאי הגידול המבטאים בפועל MAGE‑A3. הדגמה זו מצביעה על כך שהנדסת קו‑קולטנים עשויה להציל קולטנים מבטיחים שנאלצו להיות מושלכים מטעמי בטיחות.
מה זה יכול להצביע עבור טיפולים עתידיים בסרטן
מנקודת מבט שאיננה מקצועית, המסר המרכזי הוא שהצוות מצא דרך לחדד את "הראייה" של תאי החיסון על‑ידי כוונון החיווט הפנימי במקום עיצוב אינסופי של העדשה. על‑ידי החלפת שילוב המולקולות המסייעות על תאי ה‑T — ובמיוחד על‑ידי הסרת CD8 והוספת CD4 כאשר הקולטן קושר חזק את המטרה הסרטנית — החוקרים יוצרים תאי T "סופר‑סלקטיביים". תאים אלה עדיין תוקפים גידולים בעוז אך פחות נוטים להטעות ולתקוף רקמות תקינות שמציגות אותות חלשים דומים. מאחר שהגישה משאירה את רצף הקולטן הראשי ללא שינוי, היא עשויה, בעקרון, להיות ישימה באופן רחב לטיפולים רבים של תאי T, ולהציע דרך כללית לאימונותרפיה סרטנית בטוחה ומדויקת יותר.
ציטוט: Cabezas-Caballero, J., Huhn, A., Kutuzov, M.A. et al. Generation of T cells with reduced off-target cross-reactivities by engineering co-signalling receptors. Nat. Biomed. Eng 10, 753–764 (2026). https://doi.org/10.1038/s41551-025-01563-w
מילות מפתח: אימונותרפיה של סרטן, הנדסת תאי T, קולטני תאי T, רעילות עקיפה (off-target), החלפת קו‑קולטן