Clear Sky Science · pl
Generowanie komórek T o zmniejszonych reaktywnościach poza‑celem poprzez inżynierię receptorów współsygnałowych
Przekształcanie komórek walczących z rakiem w precyzyjniejsze narzędzia
Zmodyfikowane komórki odpornościowe stają się potężnym narzędziem w walce z rakiem, ale czasem mylą zdrowe tkanki z guzami, z katastrofalnymi skutkami. W tym badaniu autorzy badają nową metodę, która pozwala uczynić te komórki T znacznie bardziej selektywnymi — tak aby nadal gwałtownie atakowały nowotwory, jednocześnie w dużej mierze ignorując podobne cele w innych miejscach organizmu.
Dlaczego ataki poza‑celem są tak niebezpieczne
Wiele eksperymentalnych terapii polega na podaniu pacjentom komórek T wyposażonych w receptory zaprojektowane do rozpoznawania krótkich fragmentów białek na komórkach nowotworowych. Problem polega na tym, że każdy receptor komórki T może potencjalnie reagować na ogromną liczbę różnych fragmentów, nie tylko na te docelowe. W poprzednich badaniach klinicznych takie krzyżowe reakcje sprawiły, że zmodyfikowane komórki T zaatakowały tkanki serca lub nerwowe, powodując śmiertelne efekty uboczne. Obecne strategie bezpieczeństwa koncentrują się głównie na przeprojektowywaniu samego receptora — żmudnym procesie, który trzeba powtarzać dla każdej nowej terapii i który łatwo może wprowadzić nieprzewidziane ryzyka.
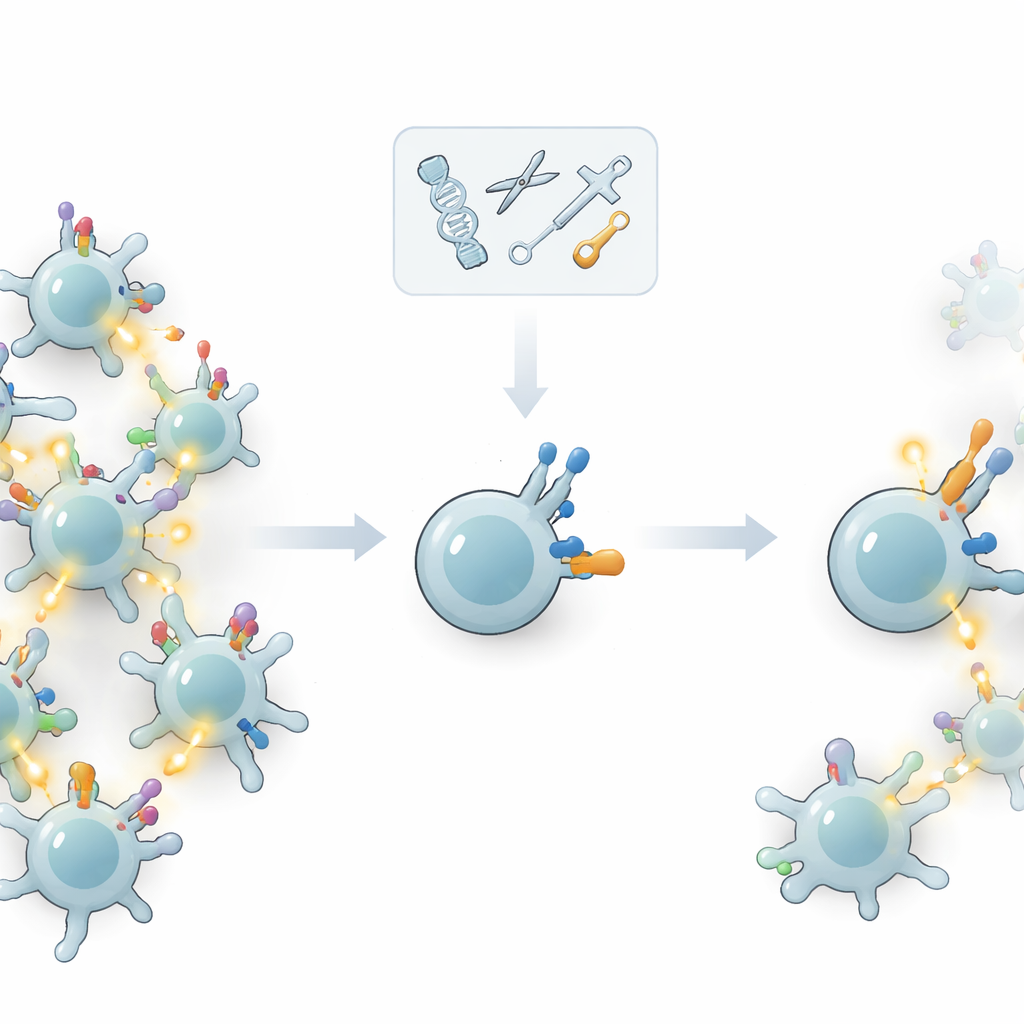
Przewiązanie sprzętu pomocniczego zamiast ingerencji w czujnik
Zamiast majstrować przy głównym receptorze, autorzy postawili pytanie, czy można wyregulować „sprzęt pomocniczy”, który kontroluje, jak silnie komórka T reaguje po związaniu liganda przez receptor. Komórki T noszą na powierzchni dodatkowe cząsteczki — koreceptory i inne białka współsygnałowe — które ustalają próg aktywacji. Poprzez selektywne usuwanie lub dodawanie tych molekuł za pomocą edycji genów zespół sprawdził, na ile komórki T potrafią odróżnić mocne, prawdopodobnie nowotworowe cele od słabszych, potencjalnie pochodzących z własnych tkanek. Kluczowy pomysł polegał na zwiększeniu zdolności komórki do ignorowania niskiej jakości sygnałów bez osłabiania odpowiedzi na sygnały wysokiej jakości.
Wymiana koreceptorów w celu stworzenia superselektorów
Badacze skupili się na trzech dobrze znanych koreceptorach: CD8, CD4 i CD5. Stwierdzili, że usunięcie CD5 sprawia, iż komórki T są łatwiej aktywowane przez wiele różnych celów, co może zwiększyć siłę przeciwnowotworową, ale także poszerzyć zakres krzyżowych reakcji. Natomiast usunięcie CD8 — cząsteczki, która zwykle pomaga cytotoksycznym komórkom T rozpoznawać cele — miało odwrotny efekt: wyraźnie zmniejszało odpowiedzi na peptydy wiążące słabiej, przy zachowaniu silnych reakcji na mocno wiążące peptydy nowotworowe. Idąc dalej, zespół wprowadził CD4 — koreceptor typowy dla innego podtypu komórek T — do tych komórek zabójczych pozbawionych CD8. To „przełączenie koreceptora CD8→CD4” znacząco podniosło próg aktywacji, tak że tylko cele nowotworowe o wysokim powinowactwie wywoływały pełną cytotoksyczność, podczas gdy szeroka gama słabszych, pozacelowych bodźców była w dużej mierze ignorowana.
Testowanie bezpieczeństwa na wielu potencjalnych celach
Aby sprawdzić, czy ta większa selektywność rzeczywiście przekłada się na bezpieczniejsze zachowanie, autorzy poddali swoje zmodyfikowane komórki kilku coraz bardziej realistycznym próbom. Najpierw użyli bibliotek zawierających tysiące losowych peptydów, z których większość powinna wiązać słabo. Standardowe zmodyfikowane komórki T zabijały wiele komórek prezentujących te losowe sekwencje, co wskazywało na wysoką krzyżową reaktywność. Natomiast komórki z usuniętym CD8, a w szczególności komórki z przełączonym koreceptorem CD8→CD4, wykazywały znacznie mniej zabijania w tych samych warunkach. Następnie zespół zbadał skoncentrowaną bibliotekę wariantów pojedynczych aminokwasów znanego peptydu nowotworowego i zmierzył, jak silnie każdy wariant wiąże receptor. Znów komórki z przełączonym koreceptorem ignorowały wiele wariantów o niższym powinowactwie, które wciąż aktywowały zwykłe zmodyfikowane komórki T. Na koniec przetestowano przewidywane „samo‑peptydy” pochodzące z ludzkich białek, które eksperymentalnie potwierdzono jako aktywujące receptor. Tutaj również komórki po przełączeniu były znacznie mniej reaktywne, zachowując jednocześnie wysoką skuteczność wobec oryginalnego, wysokopowinowactwowego celu nowotworowego.
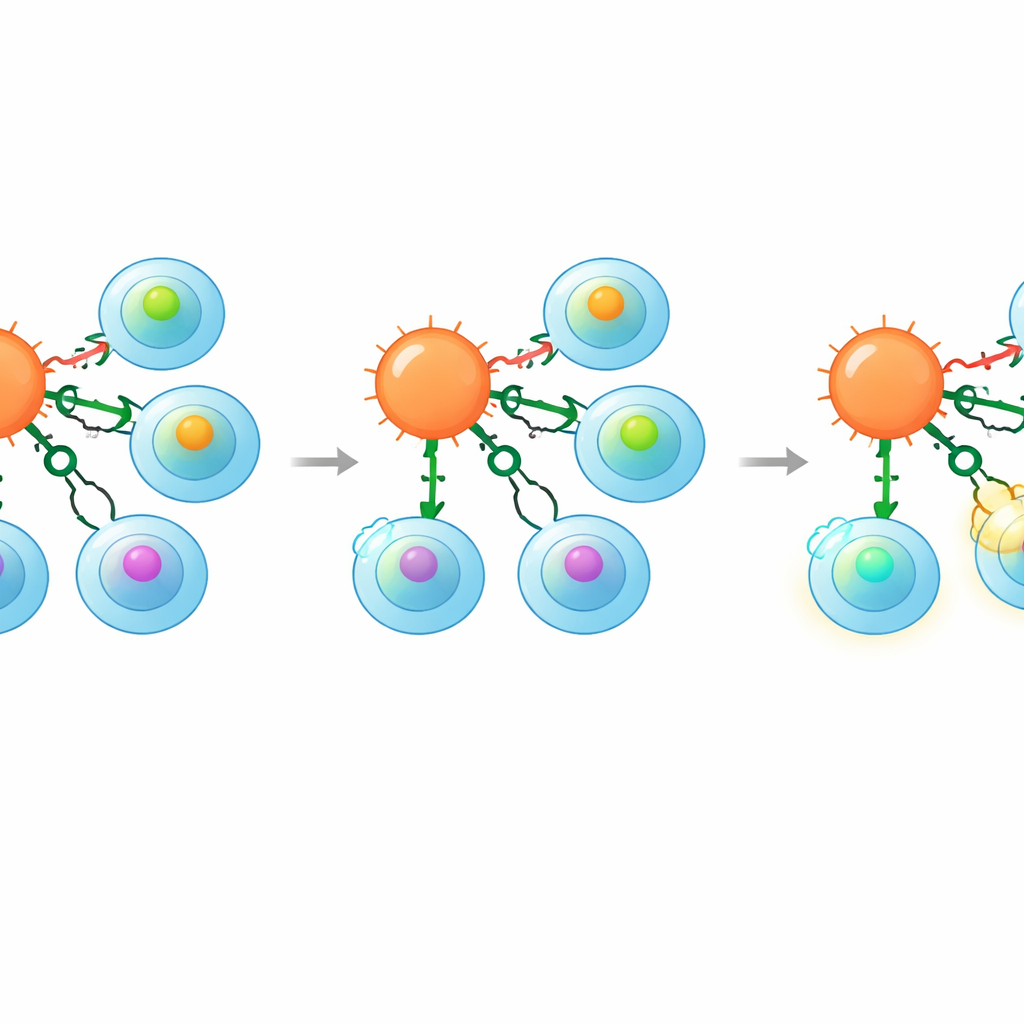
Nauka na podstawie wcześniejszych tragedii
Badacze powrócili także do klinicznie istotnej, ostrzegawczej historii. We wcześniejszym badaniu użyto komórek T niosących receptor rozpoznający białko nowotworowe MAGE‑A3; te komórki nieoczekiwanie rozpoznawały także słabszy peptyd pochodzący z białka mięśnia sercowego Titin, co doprowadziło do śmiertelnego uszkodzenia serca. W nowej pracy autorzy pokazali, że wyeliminowanie CD8 w komórkach zabójczych niosących ten sam receptor znosiło ich odpowiedź na peptyd Titin, przy jednoczesnym zachowaniu ataku na komórki nowotworowe naprawdę ekspresjonujące MAGE‑A3. Demonstracja ta sugeruje, że inżynieria koreceptorów może pomóc przywrócić obiecujące receptory, które zostały wcześniej porzucone ze względów bezpieczeństwa.
Co to może oznaczać dla przyszłych terapii przeciwnowotworowych
Z punktu widzenia laika, główny przekaz jest taki, że zespół znalazł sposób na wyostrzenie „wzroku” komórek odpornościowych przez dostosowanie wewnętrznego okablowania zamiast nieustannego przeprojektowywania soczewki. Przez zmianę kombinacji pomocniczych molekuł na komórkach T — szczególnie przez usunięcie CD8 i dodanie CD4, gdy receptor silnie wiąże swój cel nowotworowy — badacze tworzą „superselektorowe” komórki T. Komórki te nadal gwałtownie atakują guzy, ale są znacznie mniej skłonne do bycia zwiedzionymi do ataku na normalne tkanki prezentujące podobne, słabsze sygnały. Ponieważ podejście to pozostawia sekwencję głównego receptora nienaruszoną, w zasadzie może być szeroko stosowane w wielu różnych terapiach komórkowych, oferując ogólną drogę do bezpieczniejszej i precyzyjniejszej immunoterapii przeciwnowotworowej.
Cytowanie: Cabezas-Caballero, J., Huhn, A., Kutuzov, M.A. et al. Generation of T cells with reduced off-target cross-reactivities by engineering co-signalling receptors. Nat. Biomed. Eng 10, 753–764 (2026). https://doi.org/10.1038/s41551-025-01563-w
Słowa kluczowe: immunoterapia przeciwnowotworowa, inżynieria komórek T, receptory komórek T, toksyczność poza‑celem, przełączenie koreceptora