Clear Sky Science · fr
Génération de cellules T avec des réactivités hors cible réduites par l’ingénierie des récepteurs de co‑signalisation
Transformer les cellules anti‑cancer en armes plus précises
Les cellules immunitaires modifiées deviennent des outils puissants contre le cancer, mais elles peuvent parfois confondre des tissus sains avec des tumeurs, avec des conséquences mortelles. Cette étude explore une nouvelle manière de rendre ces cellules T combattant le cancer beaucoup plus sélectives, afin qu’elles attaquent toujours les tumeurs avec vigueur tout en ignorant largement des cibles semblables présentes ailleurs dans le corps.
Pourquoi les attaques hors cible sont si dangereuses
Beaucoup de thérapies expérimentales fonctionnent en donnant aux patients des cellules T équipées de récepteurs sur mesure qui reconnaissent de petits fragments protéiques à la surface des cellules tumorales. Le problème est que chaque récepteur de cellule T peut, en principe, répondre à un nombre énorme de fragments différents, pas seulement à ceux ciblés pour le cancer. Dans des essais cliniques antérieurs, de telles réactions croisées ont amené des cellules T modifiées à attaquer le cœur ou les tissus nerveux, provoquant des effets secondaires fatals. Les stratégies de sécurité actuelles cherchent principalement à redesigner le récepteur lui‑même, un processus laborieux qui doit être répété pour chaque nouvelle thérapie et peut facilement introduire de nouveaux risques imprévus.
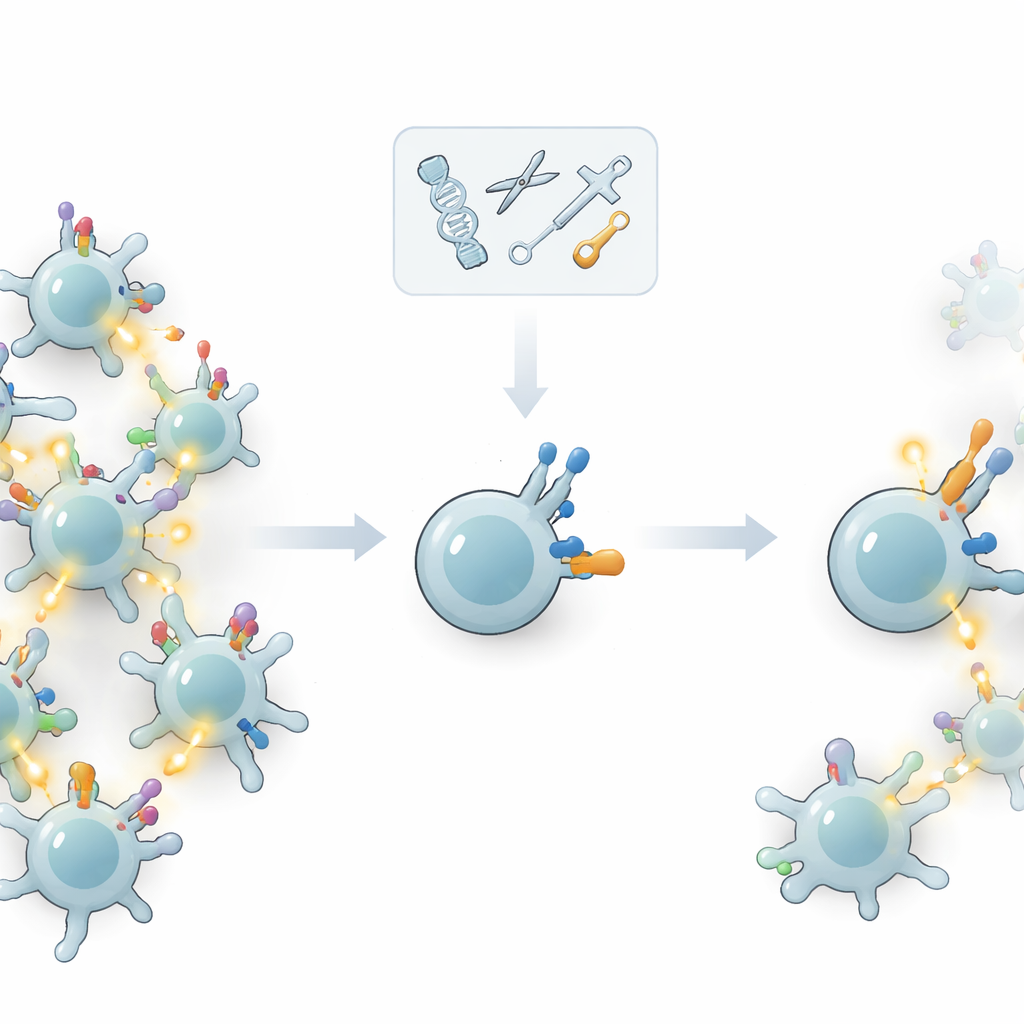
Reconfigurer l’électronique de soutien plutôt que le capteur
Plutôt que de bricoler le récepteur principal, les auteurs se sont demandé s’ils pouvaient ajuster le « matériel de soutien » qui contrôle la force de la réaction d’une cellule T une fois que son récepteur a lié quelque chose. Les cellules T portent des molécules supplémentaires à leur surface — corécepteurs et autres protéines de co‑signalisation — qui contribuent à fixer le seuil d’activation. En supprimant ou en ajoutant sélectivement ces molécules par édition génique, l’équipe a testé la capacité des cellules T à distinguer des cibles fortes, probablement tumorales, de cibles plus faibles, potentiellement dérivées du soi. Leur idée clé était d’augmenter la faculté de la cellule à ignorer les signaux de faible qualité sans émousser sa réponse aux signaux de haute qualité.
Échanger les corécepteurs pour créer des cellules super‑sélectives
Les chercheurs se sont concentrés sur trois corécepteurs bien connus : CD8, CD4 et CD5. Ils ont constaté que la suppression de CD5 rendait les cellules T plus facilement activables par de nombreuses cibles, ce qui pouvait renforcer le pouvoir anti‑tumoral mais aussi élargir la réactivité croisée. À l’inverse, la suppression de CD8, une molécule qui aide normalement les cellules T tueuses à reconnaître leurs cibles, avait l’effet opposé : elle réduisait fortement les réponses aux peptides à affinité faible tout en préservant des réponses robustes aux peptides tumoraux à forte affinité. En allant plus loin, l’équipe a introduit CD4 — un corécepteur normalement utilisé par un autre sous‑type de cellules T — dans ces cellules tueuses dépourvues de CD8. Ce « changement de corécepteur CD8→CD4 » a élevé de façon spectaculaire le seuil d’activation, de sorte que seuls des antigènes tumoraux à haute affinité déclenchaient une mise à mort complète, tandis qu’une grande variété de stimuli plus faibles et hors cible étaient en grande partie ignorés.
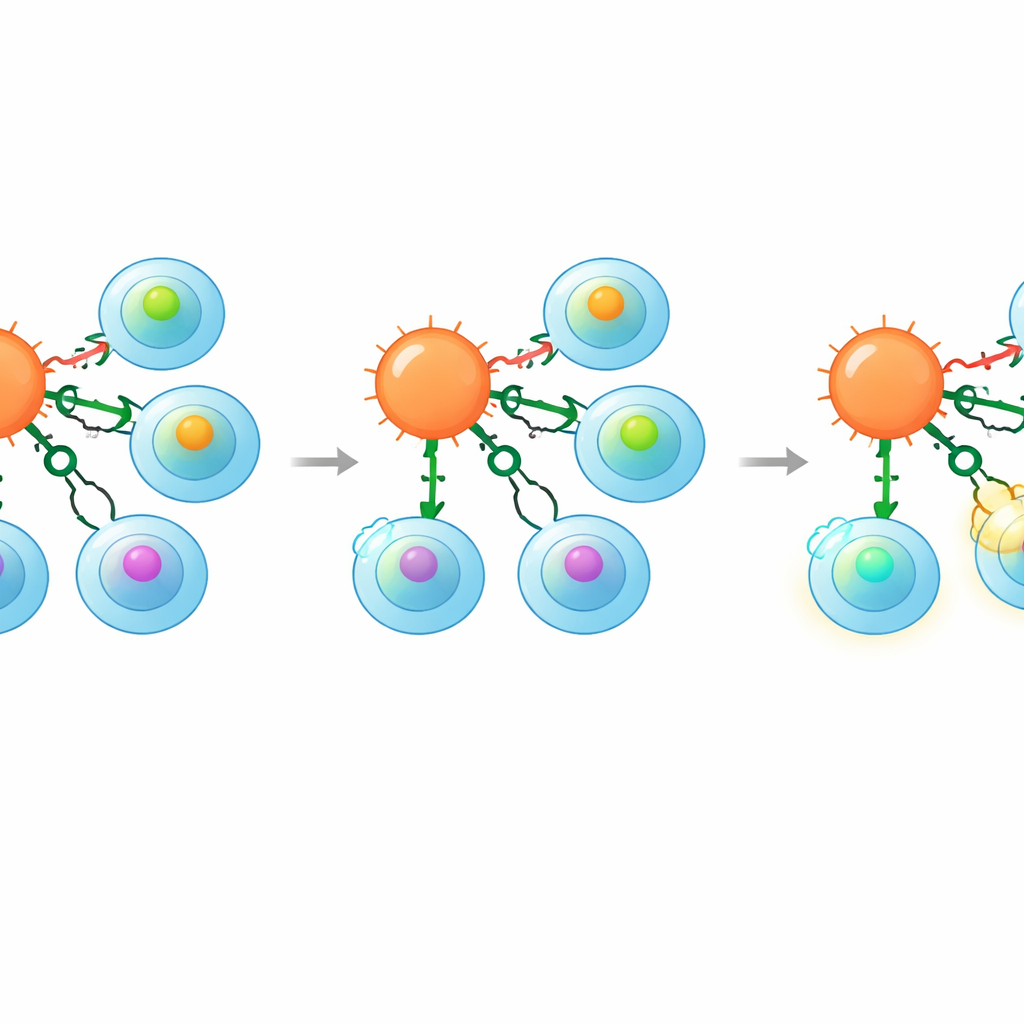
Mettre la sécurité à l’épreuve sur de nombreuses cibles potentielles
Pour vérifier si cette sélectivité renforcée se traduisait vraiment par un comportement plus sûr, les auteurs ont soumis leurs cellules modifiées à plusieurs tests de plus en plus réalistes. Ils ont d’abord utilisé des banques contenant des milliers de peptides aléatoires, dont la plupart devraient se lier faiblement. Les cellules T standard modifiées tuaient de nombreuses cellules présentant ces séquences aléatoires, révélant une forte réactivité croisée. En revanche, les cellules avec suppression de CD8, et surtout celles avec le changement CD8→CD4, montraient beaucoup moins de mise à mort dans les mêmes conditions. Ensuite, l’équipe a examiné une bibliothèque ciblée de variantes à un seul acide aminé d’un peptide tumoral connu et a mesuré la force de liaison de chaque variante au récepteur. Là encore, les cellules avec le changement de corécepteur ont ignoré de nombreuses variantes d’affinité plus faible qui activaient encore les cellules T modifiées ordinaires. Enfin, elles ont testé des peptides dérivés du soi humain prédits et confirmés expérimentalement pour activer le récepteur. Là aussi, les cellules switchées étaient beaucoup moins réactives, tout en conservant une forte puissance contre la cible tumorale originale à haute affinité.
Apprendre des tragédies passées
Les chercheurs ont aussi revisité une mise en garde clinique importante. Un essai antérieur avait utilisé des cellules T portant un récepteur pour une protéine tumorale appelée MAGE‑A3 ; ces cellules reconnaissaient de manière imprévue un peptide plus faible issu de la protéine musculaire cardiaque Titine, entraînant des lésions cardiaques fatales. Dans ce nouveau travail, les auteurs ont montré que l’ablation de CD8 dans des cellules T tueuses portant ce même récepteur supprimait leur réponse au peptide de Titine tout en préservant l’attaque des cellules tumorales exprimant réellement MAGE‑A3. Cette démonstration suggère que l’ingénierie des corécepteurs pourrait permettre de sauver des récepteurs prometteurs qui avaient dû être abandonnés pour des raisons de sécurité.
Ce que cela pourrait signifier pour les thérapies anticancéreuses futures
D’un point de vue grand public, le message central est que l’équipe a trouvé un moyen d’affiner la « vision » des cellules immunitaires en ajustant le câblage interne plutôt qu’en redesignant sans fin l’objectif. En changeant la combinaison de molécules d’aide à la surface des cellules T — en particulier en supprimant CD8 et en ajoutant CD4 lorsque le récepteur lie fortement sa cible tumorale — les chercheurs créent des cellules T « super‑sélectives ». Ces cellules attaquent toujours les tumeurs avec vigueur mais sont beaucoup moins susceptibles d’être attirées vers l’attaque de tissus normaux présentant des signaux similaires mais plus faibles. Parce que cette approche laisse la séquence du récepteur principal intacte, elle pourrait, en principe, être appliquée largement à de nombreuses thérapies cellulaires, offrant une voie générale vers une immunothérapie du cancer plus sûre et plus précise.
Citation: Cabezas-Caballero, J., Huhn, A., Kutuzov, M.A. et al. Generation of T cells with reduced off-target cross-reactivities by engineering co-signalling receptors. Nat. Biomed. Eng 10, 753–764 (2026). https://doi.org/10.1038/s41551-025-01563-w
Mots-clés: immunothérapie du cancer, ingénierie des cellules T, récepteurs des cellules T, toxicité hors cible, changement de corécepteur