Clear Sky Science · it
Generazione di cellule T con reattività incrociata ridotta tramite l’ingegneria dei recettori co‑segnalanti
Trasformare le cellule che combattono il cancro in armi più precise
Le cellule immunitarie ingegnerizzate stanno emergendo come strumenti potenti contro il cancro, ma a volte possono confondere i tessuti sani con i tumori, con conseguenze letali. Questo studio esplora un nuovo modo per rendere queste cellule T antitumorali molto più selettive, in modo che continuino ad attaccare i tumori con decisione ignorando in gran parte i bersagli somiglianti presenti altrove nell’organismo.
Perché gli attacchi fuori bersaglio sono così pericolosi
Molte terapie sperimentali funzionano fornendo ai pazienti cellule T dotate di recettori costruiti su misura che riconoscono piccoli frammenti proteici sulle cellule tumorali. La difficoltà è che ogni recettore delle cellule T può, in linea di principio, rispondere a un numero enorme di frammenti diversi, non solo a quelli cancerosi desiderati. In studi clinici passati, tali reazioni incrociate hanno portato cellule T ingegnerizzate ad attaccare tessuti cardiaci o nervosi, causando effetti collaterali fatali. Le attuali strategie di sicurezza cercano principalmente di riprogettare il recettore stesso, un processo laborioso da ripetere per ogni nuova terapia e che può facilmente introdurre nuovi rischi imprevisti.
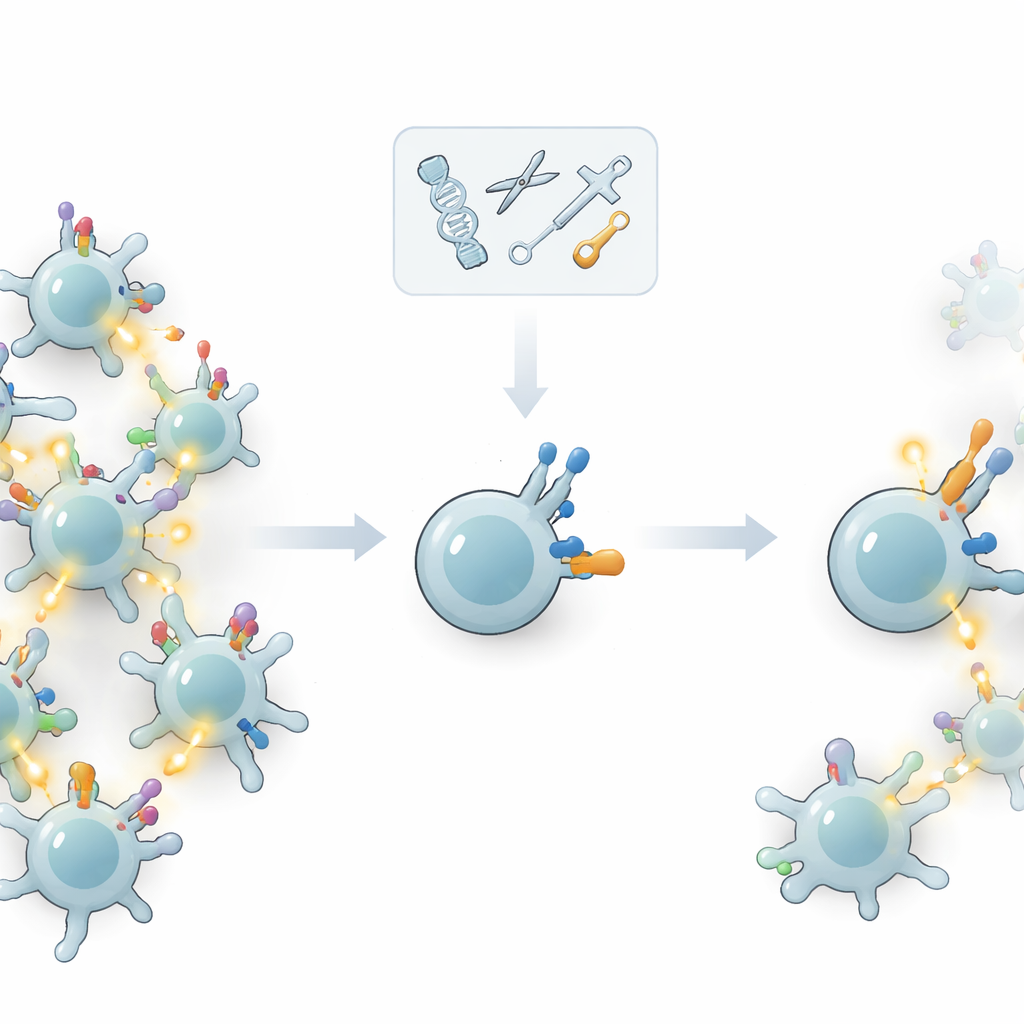
Riconfigurare l’hardware di supporto invece del sensore
Invece di manomettere il recettore principale, gli autori si sono chiesti se fosse possibile modulare l’“hardware di supporto” che controlla quanto intensamente una cellula T risponde una volta che il suo recettore è legato a qualcosa. Le cellule T portano molecole di superficie aggiuntive—co‑recettori e altre proteine co‑segnalanti—che aiutano a stabilire la soglia di attivazione. Rimuovendo o aggiungendo selettivamente queste molecole mediante editing genetico, il gruppo ha testato quanto bene le cellule T riuscissero a distinguere bersagli forti, verosimilmente tumorali, da bersagli più deboli e potenzialmente derivati dal sé. L’idea chiave era aumentare la capacità della cellula di ignorare segnali di bassa qualità senza smorzare la risposta ai segnali di alta qualità.
Sostituire i co‑recettori per creare cellule super‑selettive
I ricercatori si sono concentrati su tre co‑recettori noti: CD8, CD4 e CD5. Hanno scoperto che la cancellazione di CD5 rendeva le cellule T più facilmente attivabili da molti bersagli diversi, potenzialmente aumentando la potenza antitumorale ma ampliando anche la reattività incrociata. Al contrario, la rimozione di CD8, una molecola che normalmente aiuta le cellule T citotossiche a riconoscere i bersagli, aveva l’effetto opposto: riduceva drasticamente le risposte a peptidi con legame più debole preservando però risposte robuste ai peptidi tumorali con legame forte. Facendo un passo ulteriore, il team ha introdotto CD4—un co‑recettore normalmente utilizzato da un diverso sottotipo di cellule T—nelle cellule killer con CD8 eliminato. Questo “scambio co‑recettore CD8→CD4” ha innalzato drasticamente la soglia di attivazione, in modo che solo bersagli tumorali ad alta affinità scatenassero l’uccisione completa, mentre una vasta gamma di stimoli più deboli e fuori bersaglio veniva in gran parte ignorata.
Mettere alla prova la sicurezza su molti potenziali bersagli
Per verificare se questa selettività più stretta si traducesse davvero in un comportamento più sicuro, gli autori hanno sottoposto le loro cellule ingegnerizzate a diversi test via via più realistici. Per prima cosa hanno usato librerie contenenti migliaia di peptidi casuali, la maggior parte dei quali dovrebbe legarsi debolmente. Le cellule T ingegnerizzate standard hanno ucciso molte cellule che presentavano queste sequenze casuali, segnalando un’elevata reattività incrociata. Al contrario, le cellule con knockout di CD8, e soprattutto quelle con lo scambio CD8→CD4, hanno mostrato molta meno uccisione nelle stesse condizioni. Successivamente, il team ha esaminato una libreria mirata di varianti con singolo amminoacido di un noto peptide tumorale e ha misurato quanto fortemente ciascuna variante legasse il recettore. Anche in questo caso, le cellule con lo scambio di co‑recettore hanno ignorato molte delle varianti a bassa affinità che attivavano ancora le cellule T ingegnerizzate ordinarie. Infine, hanno testato peptidi self predetti da proteine umane che erano stati sperimentalmente confermati come in grado di attivare il recettore. Anche qui, le cellule scambiate erano molto meno reattive, pur mantenendo una forte potenza contro il bersaglio tumorale originale ad alta affinità.
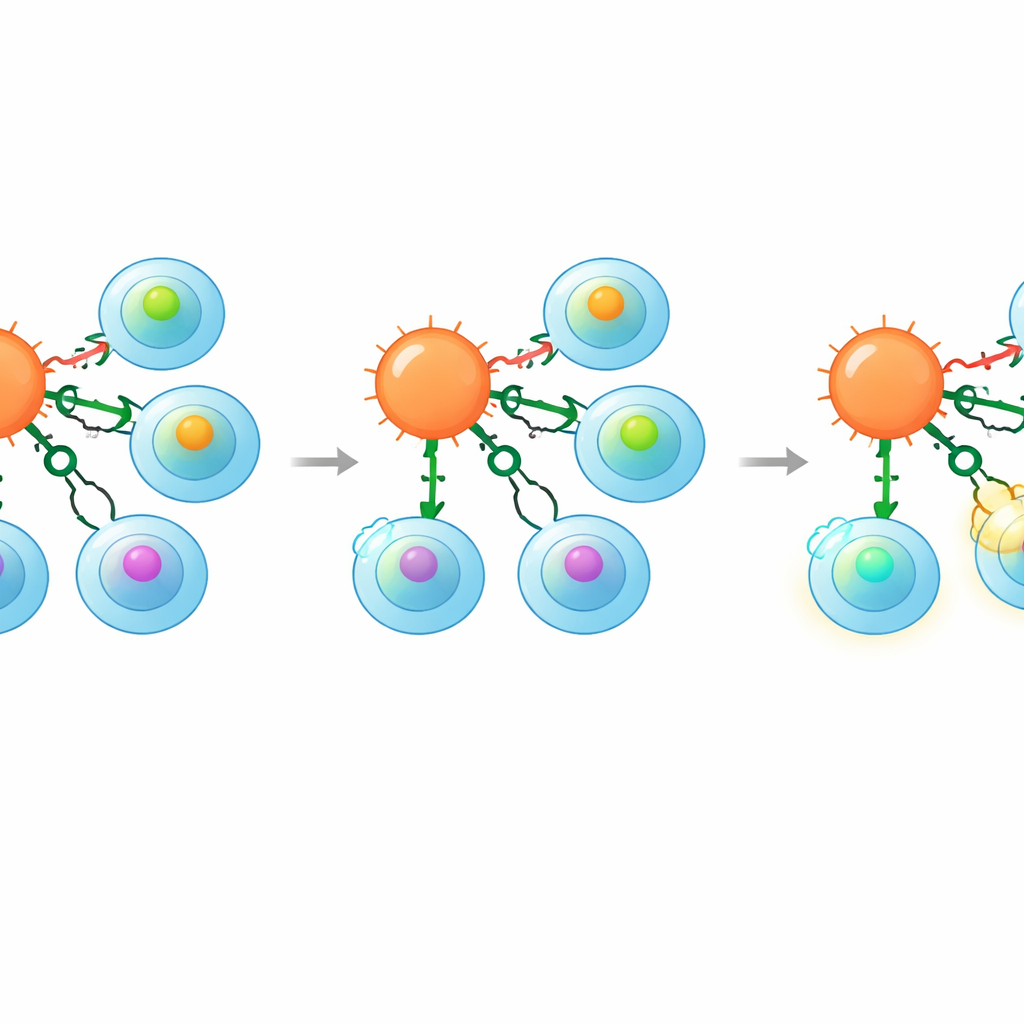
Imparare dalle tragedie passate
I ricercatori hanno anche rivisitato un racconto clinicamente importante e di avvertimento. Uno studio precedente aveva usato cellule T portatrici di un recettore per una proteina tumorale chiamata MAGE‑A3; quelle cellule riconoscevano inaspettatamente anche un peptide più debole della proteina cardiaca Titina, causando danni cardiaci fatali. Nel nuovo lavoro, gli autori hanno mostrato che l’eliminazione di CD8 nelle cellule T killer che portavano lo stesso recettore annullava la loro risposta al peptide di Titina pur preservando l’attacco alle cellule tumorali che esprimevano effettivamente MAGE‑A3. Questa dimostrazione suggerisce che l’ingegneria dei co‑recettori potrebbe aiutare a recuperare recettori altrimenti promettenti che erano stati abbandonati per ragioni di sicurezza.
Cosa potrebbe significare per le terapie antitumorali future
Dal punto di vista non tecnico, il messaggio centrale è che il gruppo ha trovato un modo per affinare la “visione” delle cellule immunitarie regolando il cablaggio interno invece di riprogettare all’infinito l’obiettivo. Modificando la combinazione di molecole di supporto sulle cellule T—soprattutto rimuovendo CD8 e aggiungendo CD4 quando il recettore lega fortemente il suo bersaglio tumorale—i ricercatori creano cellule T “super selettive”. Queste cellule continuano ad attaccare i tumori con vigore ma sono molto meno propense a essere attirate ad attaccare i tessuti normali che presentano segnali simili e più deboli. Poiché questo approccio lascia intatta la sequenza del recettore principale, potrebbe in linea di principio essere applicato in modo ampio a molte diverse terapie cellulari, offrendo una strada generale verso un’immunoterapia oncologica più sicura e più precisa.
Citazione: Cabezas-Caballero, J., Huhn, A., Kutuzov, M.A. et al. Generation of T cells with reduced off-target cross-reactivities by engineering co-signalling receptors. Nat. Biomed. Eng 10, 753–764 (2026). https://doi.org/10.1038/s41551-025-01563-w
Parole chiave: immunoterapia contro il cancro, ingegneria delle cellule T, recettori delle cellule T, tossicità fuori bersaglio, scambio dei co‑recettori