Clear Sky Science · nl
Generatie van T-cellen met verminderde off-target kruisreactiviteiten door het ontwerpen van co-signalerende receptoren
Cancervechtende cellen scherper maken
Geredigeerde immuuncellen rijzen op als krachtige instrumenten tegen kanker, maar ze kunnen soms gezonde weefsels verwarren met tumoren, met dodelijke gevolgen. Deze studie onderzoekt een nieuwe manier om deze kankervretende T-cellen veel selectiever te maken, zodat ze tumoren nog steeds fel aanvallen maar veelal gelijkende doelwitten elders in het lichaam negeren.
Waarom off-target aanvallen zo gevaarlijk zijn
Veel experimentele therapieën werken door patiënten T-cellen te geven die zijn uitgerust met op maat gemaakte receptoren die kleine eiwitfragmenten op tumorcellen herkennen. Het probleem is dat elke T-celreceptor in principe op een enorm aantal verschillende fragmenten kan reageren, niet alleen op de bedoelde kankerversies. In eerdere klinische proefnemingen leidden zulke kruisreacties ertoe dat gemodificeerde T-cellen hart- of zenuwweefsel aanvielen, wat fatale bijwerkingen veroorzaakte. Huidige veiligheidsstrategieën proberen vooral de receptor zelf te herontwerpen — een arbeidsintensief proces dat voor elke nieuwe therapie opnieuw moet worden uitgevoerd en gemakkelijk nieuwe, onvoorziene risico’s kan introduceren.
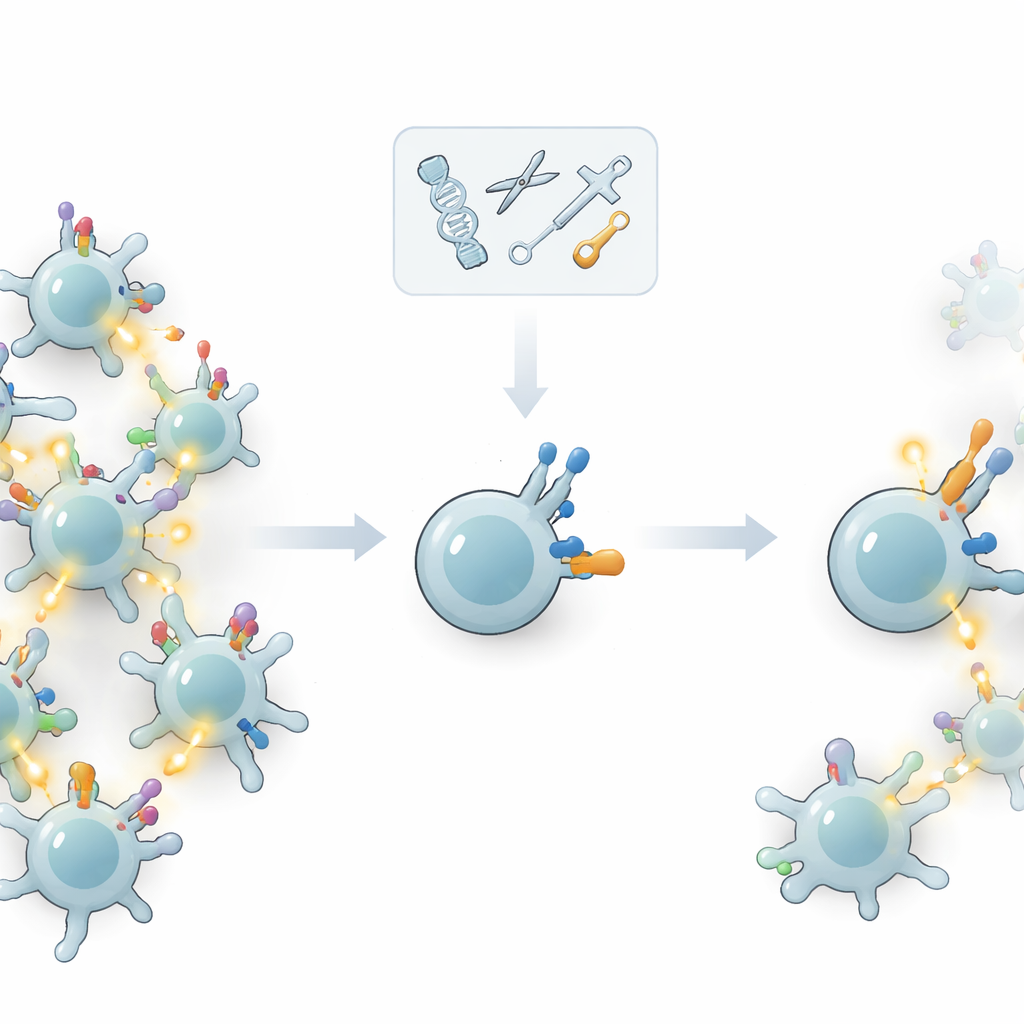
De ondersteunende hardware herbedraden in plaats van de sensor
In plaats van te rommelen met de hoofdreceptor vroegen de auteurs zich af of ze de “ondersteunende hardware” konden afstemmen die bepaalt hoe sterk een T-cel reageert zodra zijn receptor iets gebonden heeft. T-cellen dragen aanvullende oppervlaktemoleculen — co-receptoren en andere co-signalerende eiwitten — die helpen de drempel voor activatie in te stellen. Door deze moleculen selectief te verwijderen of toe te voegen met genbewerking, testte het team hoe goed T-cellen sterke, waarschijnlijk tumorgerelateerde doelwitten konden onderscheiden van zwakkere, mogelijk door het eigen lichaam afkomstige doelwitten. Hun kernidee was het vermogen van de cel te vergroten om signalen van lage kwaliteit te negeren zonder de respons op signalen van hoge kwaliteit te verminderen.
Co-receptoren verwisselen om super-selectieve cellen te creëren
De onderzoekers concentreerden zich op drie goed bekende co-receptoren: CD8, CD4 en CD5. Ze vonden dat het verwijderen van CD5 T-cellen makkelijker maakte te activeren door veel verschillende doelwitten, wat de antitumorkracht zou kunnen vergroten maar ook de kruisreactiviteit verbreedde. Daarentegen had het wegnemen van CD8, een molecuul dat normaal killer-T-cellen helpt doelwitten te herkennen, het tegengestelde effect: het verminderde sterk de reacties op zwakker bindende peptiden terwijl robuuste reacties op sterk bindende kankerpéptiden behouden bleven. Vervolgens introduceerde het team CD4 — een co-receptor die normaal door een ander T-celtype wordt gebruikt — in deze CD8-verwijderde killer-cellen. Deze "CD8→CD4 co-receptorwisseling" verhoogde de activatiedrempel aanzienlijk, zodat alleen hoge-affiniteits kankerd oelwitten volledige killing teweegbrachten, terwijl een brede variëteit aan zwakkere, off-target stimuli grotendeels werd genegeerd.
Veiligheid testen over vele potentiële doelwitten
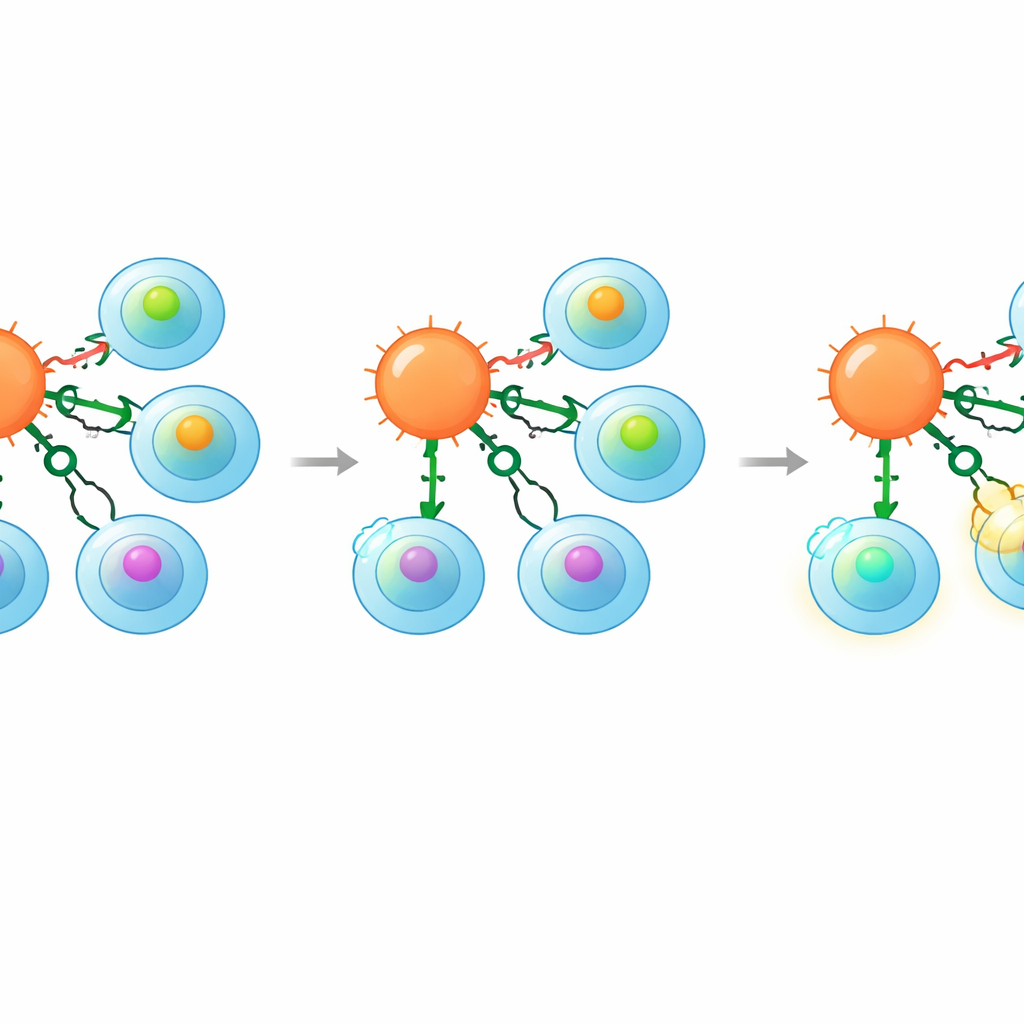
Om te beoordelen of deze striktere selectiviteit werkelijk tot veiliger gedrag leidde, daagden de auteurs hun gemodificeerde cellen uit met verschillende, steeds realistischer tests. Ze gebruikten eerst bibliotheken met duizenden willekeurige peptiden, waarvan de meeste zwak zouden moeten binden. Standaard gemodificeerde T-cellen doodden veel cellen die deze willekeurige sequenties presenteerden, wat hoge kruisreactiviteit aangaf. In contrast toonden CD8-knockoutcellen, en in het bijzonder de CD8→CD4-gewisselde cellen, veel minder killing onder dezelfde omstandigheden. Vervolgens onderzocht het team een gerichte bibliotheek van enkelvoudige aminozuurvarianten van een bekend tumorpeptide en mat hoe sterk elke variant aan de receptor bond. Ook hier negeerden cellen met de co-receptorwisseling veel van de lagere-affiniteitsvarianten die nog wel gewone gemodificeerde T-cellen activeerden. Ten slotte testten ze voorspelde zelf-peptiden uit humane eiwitten die experimenteel waren bevestigd als receptoractiverend. Ook hier waren de gewisselde cellen veel minder reactief, terwijl ze hun sterke potentie tegen het oorspronkelijke, hoge-affiniteits tumordoel behielden.
Leren van eerdere tragedies
De onderzoekers gingen ook terug naar een klinisch belangrijk waarschuwingstarief. Een eerdere proef gebruikte T-cellen met een receptor voor een kankereiwit genaamd MAGE‑A3; die cellen herkenden onverwacht ook een zwakker peptide van het hartspiereiwit Titin, wat leidde tot fatale hartschade. In het nieuwe werk toonden de auteurs aan dat het uitzetten van CD8 in killer-T-cellen met dezelfde receptor hun reactie op het Titin-peptide tenietdeed terwijl de aanval op tumorcellen die daadwerkelijk MAGE‑A3 tot expressie brachten behouden bleef. Deze demonstratie suggereert dat co-receptorengineering veelbelovende receptoren die om veiligheidsredenen waren afgestoten, mogelijk kan redden.
Wat dit kan betekenen voor toekomstige kankertherapieën
Voor een lekenpubliek komt de kernboodschap neer op het vinden van een manier om het "zicht" van immuuncellen te verscherpen door de interne bedrading aan te passen in plaats van de lens eindeloos te herontwerpen. Door de combinatie van helpermoleculen op T-cellen te wisselen — met name door CD8 te verwijderen en CD4 toe te voegen wanneer de receptor sterk aan zijn kankerdoel bindt — creëren de onderzoekers "super-selectieve" T-cellen. Deze cellen vallen tumoren nog steeds krachtig aan maar lopen veel minder kans verleid te worden normale weefsels aan te vallen die vergelijkbare, zwakkere signalen presenteren. Omdat deze aanpak de sequentie van de hoofdreceptor ongemoeid laat, zou ze in principe breed toepasbaar kunnen zijn op vele verschillende T-celtherapieën en zo een algemene route bieden naar veiligere, nauwkeurigere kankerimmunotherapie.
Bronvermelding: Cabezas-Caballero, J., Huhn, A., Kutuzov, M.A. et al. Generation of T cells with reduced off-target cross-reactivities by engineering co-signalling receptors. Nat. Biomed. Eng 10, 753–764 (2026). https://doi.org/10.1038/s41551-025-01563-w
Trefwoorden: kankerimmunotherapie, T-celengineering, T-celreceptoren, off-target toxiciteit, co-receptorwisseling