Clear Sky Science · ar
توليد خلايا تي ذات تفاعلات متبادلة ضئيلة خارج الهدف من خلال هندسة مستقبلات الإشارات المشتركة
تحويل خلايا مكافحة السرطان إلى أسلحة أكثر دقة
تظهر الخلايا المناعية المهندسة كأدوات قوية ضد السرطان، لكنها قد تخلط أحيانًا بين الأنسجة السليمة والأورام، مع عواقب قاتلة. تستكشف هذه الدراسة طريقة جديدة لجعل خلايا تي المناعية هذه أكثر انتقائية إلى حد كبير، بحيث تواصل مهاجمة الأورام بشراسة بينما تتجاهل إلى حد كبير الأهداف الشبيهة بها في أماكن أخرى من الجسم.
لماذا تُشكّل الهجمات خارج الهدف خطراً كبيراً
تعتمد العديد من العلاجات التجريبية على تزويد المرضى بخلايا تي مزودة بمستقبلات مخصصة تتعرف على شظايا بروتينية صغيرة على خلايا الورم. والتحدي أن كل مستقبل خلية تي يمكن، من حيث المبدأ، أن يستجيب لعدد هائل من الشظايا المختلفة، وليس فقط لتلك المقصودة المتعلقة بالسرطان. في تجارب سريرية سابقة، أدت هذه التفاعلات المتبادلة إلى أن تهاجم الخلايا المهندسة أنسجة القلب أو الأعصاب، محدثة آثارًا جانبية قاتلة. تحاول استراتيجيات السلامة الحالية في الغالب إعادة تصميم المستقبل نفسه، وهي عملية مرهقة يجب تكرارها لكل علاج جديد وقد تُدخل بسهولة مخاطر غير متوقعة جديدة.
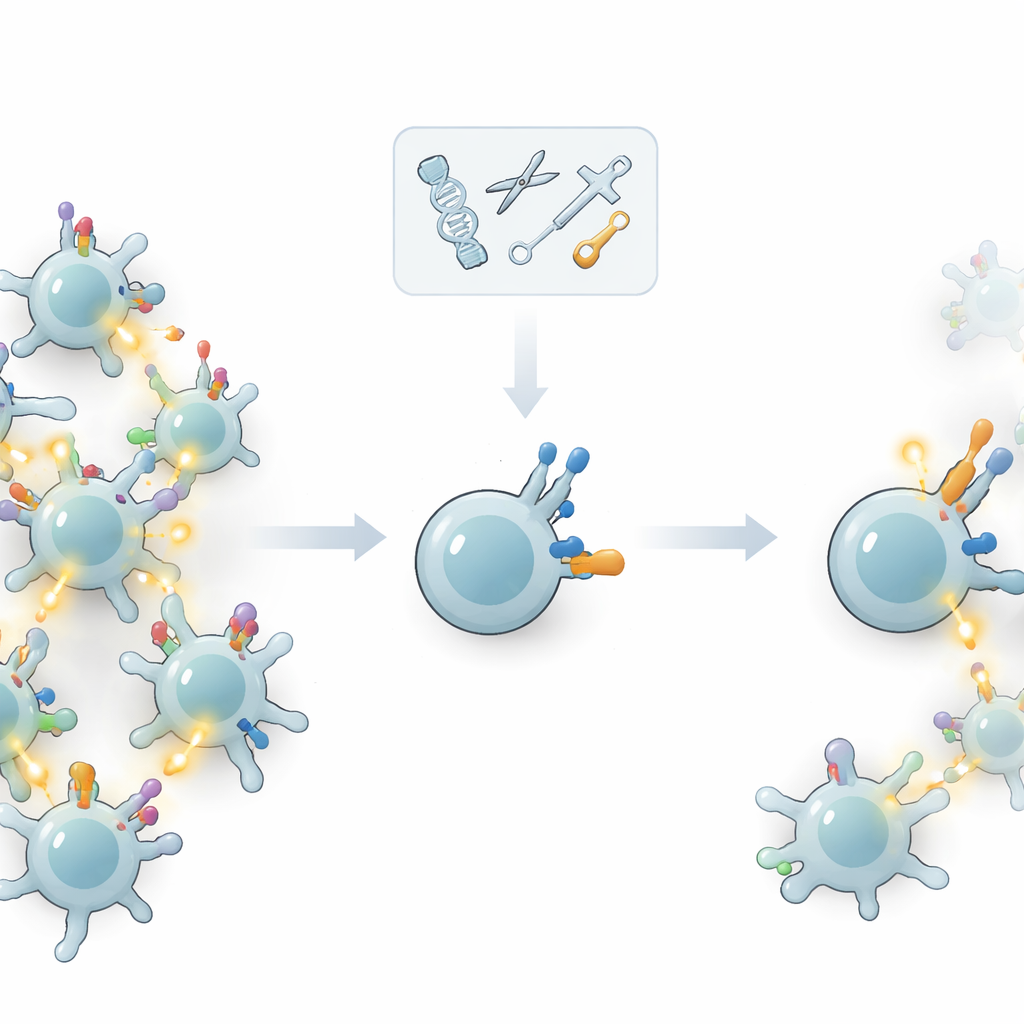
إعادة توصيل الأجهزة المساعدة بدلًا من المستشعر
بدلاً من العبث بالمستقبل الرئيسي، تساءل المؤلفون عما إذا كان بإمكانهم ضبط «الأجهزة المساعدة» التي تتحكم في قوة استجابة خلية تي بمجرد ارتباط مستقبلها بشيء ما. تحمل خلايا تي جزيئات سطحية إضافية — مستقبلات مشاركة وبروتينات إشارات مشتركة أخرى — تُساعد في تحديد عتبة التنشيط. من خلال إزالة أو إضافة هذه الجزيئات انتقائيًا باستخدام التحرير الجيني، اختبر الفريق مدى قدرة خلايا تي على تمييز الأهداف القوية المحتملة (المحتملة أن تكون أورامًا) عن الأهداف الأضعف المحتملة المنشأ ذاتيًا. كانت الفكرة الأساسية زيادة قدرة الخلية على تجاهل الإشارات منخفضة الجودة دون إضعاف استجابتها للإشارات عالية الجودة.
تبديل المستقبلات المشاركة لصنع خلايا فائقة الانتقائية
ركز الباحثون على ثلاثة مستقبلات مشاركة معروفة جيدًا: CD8 وCD4 وCD5. وجدوا أن حذف CD5 جعل خلايا تي أكثر سهولة في التنشيط بواسطة العديد من الأهداف المختلفة، مما قد يعزز القوة المضادة للأورام لكنه يوسع أيضًا التفاعلات المتبادلة. على النقيض من ذلك، كان لإزالة CD8 — الجزيء الذي يساعد عادة خلايا تي القاتلة على التعرف على الأهداف — تأثير معاكس: قلّل بشكل حاد من الاستجابات تجاه الببتيدات ذات الارتباط الأضعف مع الحفاظ على استجابات قوية تجاه الببتيدات السرطانية ذات الارتباط القوي. وبالذهاب خطوة أبعد، أدخل الفريق CD4 — مستقبل مشاركة يستخدمه نوع آخر من خلايا تي عادةً — في هذه الخلايا القاتلة التي حُذِف منها CD8. هذا «تبديل مستقبل المشاركة من CD8 إلى CD4» رفع بشكل دراماتيكي عتبة التنشيط، بحيث لم تعد سوى الأهداف السرطانية ذات اللَّزَم العالي affinity تحفز القتل الكامل، بينما تم تجاهل مجموعة واسعة من المنبهات الأضعف خارج الهدف إلى حد كبير.
اختبار السلامة عبر العديد من الأهداف المحتملة
لمعرفة ما إذا كانت هذه الانتقائية الأشد تُترجَم بالفعل إلى سلوك أكثر أمانًا، تحدى المؤلفون خلاياهم المهندسة بعدة اختبارات متزايدة الواقعية. استخدموا أولاً مكتبات تحتوي على آلاف الببتيدات العشوائية، والتي من المتوقع أن ترتبط معظمها بشكل ضعيف. قتلت خلايا تي المهندسة التقليدية العديد من الخلايا التي تقدّم هذه التسلسلات العشوائية، مما يشير إلى تفاعلية متبادلة عالية. في المقابل، أظهرت خلايا حذف CD8، وخاصة خلايا التبديل CD8→CD4، قتلاً أقل بكثير تحت نفس الظروف. بعد ذلك، فحص الفريق مكتبة مركزة من متغيرات حمض أميني واحد لببتيد ورمي معروف وقيَسوا مدى قوة ارتباط كل متغير بالمستقبل. مرة أخرى، تجاهلت الخلايا ذات تبديل المستقبل العديد من المتغيرات منخفضة الارتباط التي كانت لا تزال تنشط خلايا تي المهندسة العادية. أخيرًا، اختبروا ببتيدات ذاتية متوقعة من بروتينات بشرية تم التأكد تجريبيًا من أنها تنشط المستقبل. هنا أيضًا، كانت الخلايا المتبدلة أقل تفاعلاً بكثير، ومع ذلك احتفظت بفاعلية قوية ضد الهدف الورمي الأصلي ذي الارتباط العالي.
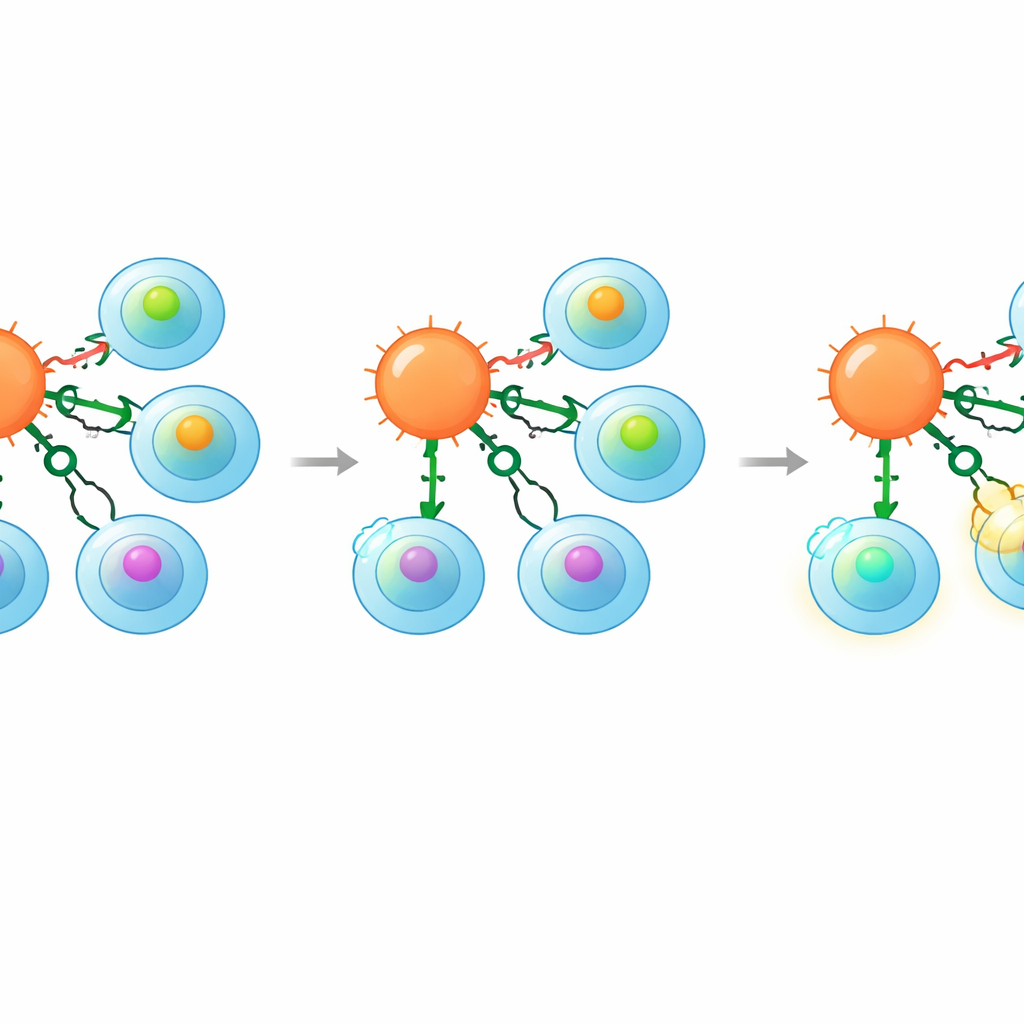
التعلّم من مآسي سابقة
أعاد الباحثون أيضًا النظر في قصة تحذيرية ذات أهمية سريرية. في تجربة سابقة، استُخدمت خلايا تي تحمل مستقبلًا لبروتين سرطاني يُدعى MAGE‑A3؛ فقد تعرفت تلك الخلايا بشكل غير متوقع أيضًا على ببتيد أضعف من بروتين عضلة القلب تيتين، مما أدى إلى ضرر قلبي قاتل. في العمل الجديد، أظهر المؤلفون أن حذف CD8 في خلايا تي القاتلة الحاملة لذلك المستقبل ذاته أبطل استجابتهم لببتيد تيتين مع الحفاظ على الهجوم على الخلايا السرطانية التي تعبر فعليًا عن MAGE‑A3. تشير هذه النتيجة إلى أن هندسة المستقبلات المشاركة قد تساعد في إنقاذ مستقبلات واعدة اضطروا إلى التخلي عنها لأسباب تتعلق بالسلامة.
ما الذي قد يعنيه هذا لعلاجات السرطان المستقبلية
من منظور عام، الرسالة الأساسية أن الفريق وجد وسيلة لصقل «بصر» الخلايا المناعية عن طريق تعديل التوصيلات الداخلية بدلًا من إعادة تصميم العدسة بلا نهاية. من خلال تبديل مجموعة جزيئات المساعدة على خلايا تي — وخصوصًا بإزالة CD8 وإضافة CD4 عندما يرتبط المستقبل بقوة بخاصية سرطانية — يخلق الباحثون خلايا تي «فائقة الانتقائية». تهاجم هذه الخلايا الأورام بحيوية لكنها أقل عرضة بكثير لأن تُغرَى بمهاجمة الأنسجة الطبيعية التي تعرض إشارات شبيهة وأضعف. وبما أن هذا النهج يترك تسلسل المستقبل الرئيسي دون تغيير، فقد يكون من الناحية النظرية قابلاً للتطبيق على نطاق واسع عبر العديد من علاجات خلايا تي، موفراً طريقًا عامًا نحو مناعة ضد السرطان أكثر أمانًا ودقة.
الاستشهاد: Cabezas-Caballero, J., Huhn, A., Kutuzov, M.A. et al. Generation of T cells with reduced off-target cross-reactivities by engineering co-signalling receptors. Nat. Biomed. Eng 10, 753–764 (2026). https://doi.org/10.1038/s41551-025-01563-w
الكلمات المفتاحية: المناعة ضد السرطان, هندسة خلايا تي, مستقبلات خلايا تي, سُمّية خارج الهدف, تبديل مستقبلات المساعدة