Clear Sky Science · de
Erzeugung von T‑Zellen mit reduzierten Off‑Target‑Kreuzreaktivitäten durch gezielte Veränderung von Ko‑Signalisierungsrezeptoren
Krebsbekämpfende Zellen zu präziseren Waffen machen
Gezüchtete Immunzellen entwickeln sich zu starken Werkzeugen gegen Krebs, können aber manchmal gesundes Gewebe mit Tumoren verwechseln — mit tödlichen Folgen. Diese Studie untersucht einen neuen Ansatz, um diese krebsbekämpfenden T‑Zellen deutlich selektiver zu machen, sodass sie Tumoren weiterhin aggressiv angreifen, dabei aber weitgehend ähnliche Zielstrukturen an anderen Stellen des Körpers ignorieren.
Warum Off‑Target‑Angriffe so gefährlich sind
Viele experimentelle Therapien funktionieren, indem Patientinnen und Patienten T‑Zellen mit maßgeschneiderten Rezeptoren erhalten, die kleine Proteinfragmente auf Tumorzellen erkennen. Das Problem ist, dass jeder T‑Zell‑Rezeptor prinzipiell auf eine enorme Zahl unterschiedlicher Fragmente reagieren kann, nicht nur auf die beabsichtigten krebsassoziierten. In früheren klinischen Studien haben solche Kreuzreaktionen dazu geführt, dass gentechnisch veränderte T‑Zellen Herz‑ oder Nervengewebe angriffen und tödliche Nebenwirkungen verursachten. Aktuelle Sicherheitsstrategien versuchen meist, den Rezeptor selbst umzugestalten — ein mühsamer Prozess, der für jede neue Therapie wiederholt werden muss und leicht neue, unvorhergesehene Risiken einführen kann.
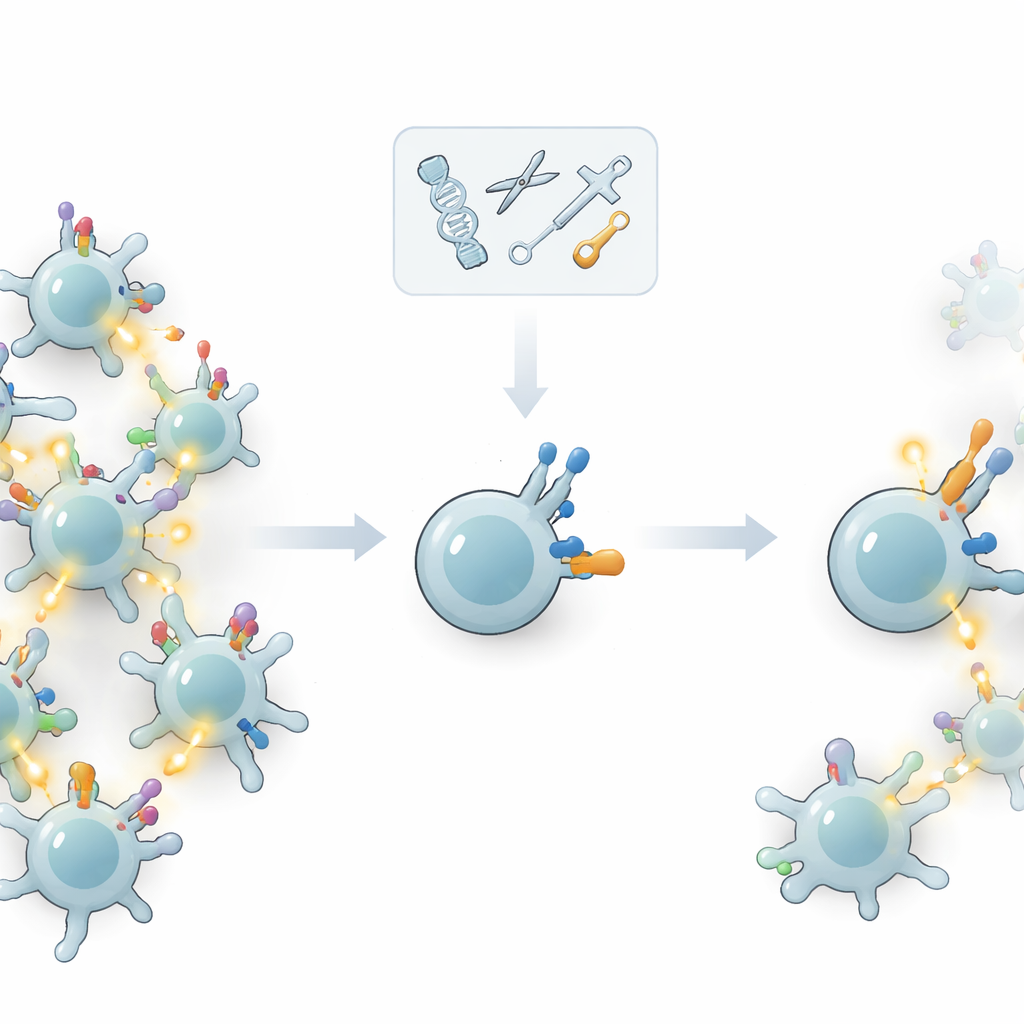
Die Hilfssysteme umverkabeln statt den Sensor
Statt am Hauptrezeptor zu fummeln, fragten die Autorinnen und Autoren, ob sich die „Hilfshardware“ einstellen lässt, die bestimmt, wie stark eine T‑Zelle reagiert, nachdem ihr Rezeptor etwas gebunden hat. T‑Zellen tragen zusätzliche Oberflächenmoleküle — Ko‑Rezeptoren und andere Ko‑Signalisierungsproteine — die die Aktivierungsschwelle mitbestimmen. Durch selektives Entfernen oder Hinzufügen dieser Moleküle mittels Geneditierung testete das Team, wie gut T‑Zellen starke, wahrscheinlich tumorassoziierte Ziele von schwächeren, potenziell körpereigenen Zielen unterscheiden können. Die Kernidee war, die Fähigkeit der Zelle zu erhöhen, minderwertige Signale zu ignorieren, ohne die Reaktion auf hochwertige Signale zu dämpfen.
Ko‑Rezeptoren austauschen, um superselektive Zellen zu erzeugen
Die Forschenden konzentrierten sich auf drei bekannte Ko‑Rezeptoren: CD8, CD4 und CD5. Sie fanden heraus, dass das Entfernen von CD5 T‑Zellen leichter aktivierbar machte, was die Anti‑Tumor‑Kraft potenziell verstärken, aber auch die Kreuzreaktivität verbreitern konnte. Im Gegensatz dazu führte das Entfernen von CD8 — einem Molekül, das Killer‑T‑Zellen normalerweise bei der Erkennung unterstützt — zum gegenteiligen Effekt: Die Reaktion auf schwächer bindende Peptide wurde stark reduziert, während robuste Antworten auf stark bindende Krebspeptide erhalten blieben. Einen Schritt weiter ging das Team, indem es CD4 — einen Ko‑Rezeptor, der normalerweise von einer anderen T‑Zell‑Untergruppe genutzt wird — in diese CD8‑deletierten Killerzellen einführte. Dieser „CD8→CD4‑Ko‑Rezeptor‑Switch“ erhöhte die Aktivierungsschwelle dramatisch, sodass nur hochaffine Krebsziele vollständige Tötungsreaktionen auslösten, während eine breite Palette schwächerer Off‑Target‑Stimuli weitgehend ignoriert wurde.
Sicherheit über viele potenzielle Ziele hinweg prüfen
Um zu prüfen, ob diese engere Selektivität wirklich in ein sichereres Verhalten übersetzt, setzten die Autorinnen und Autoren ihre gentechnisch veränderten Zellen mehreren zunehmend realistischen Tests aus. Zunächst verwendeten sie Bibliotheken mit Tausenden zufälliger Peptide, von denen die meisten schwach binden sollten. Standard‑engineering‑T‑Zellen töteten viele Zellen, die diese Zufallssequenzen präsentierten, was auf hohe Kreuzreaktivität hinwies. Im Gegensatz dazu zeigten CD8‑Knockout‑Zellen und insbesondere die CD8→CD4‑Switch‑Zellen unter denselben Bedingungen deutlich weniger Tötung. Anschließend untersuchte das Team eine fokussierte Bibliothek von Einzelaminoacid‑Varianten eines bekannten Tumorpeptids und maß, wie stark jede Variante den Rezeptor bindet. Auch hier ignorierten die Zellen mit Ko‑Rezeptor‑Switch viele der geringaffinen Varianten, die normale gentechnisch veränderte T‑Zellen noch aktivierten. Schließlich testeten sie vorhergesagte Selbstpeptide aus menschlichen Proteinen, die experimentell bestätigt worden waren, den Rezeptor zu aktivieren. Auch hier waren die geschalteten Zellen deutlich weniger reaktiv, behielten jedoch eine starke Potenz gegen das ursprüngliche, hochaffine Tumor‑Target bei.
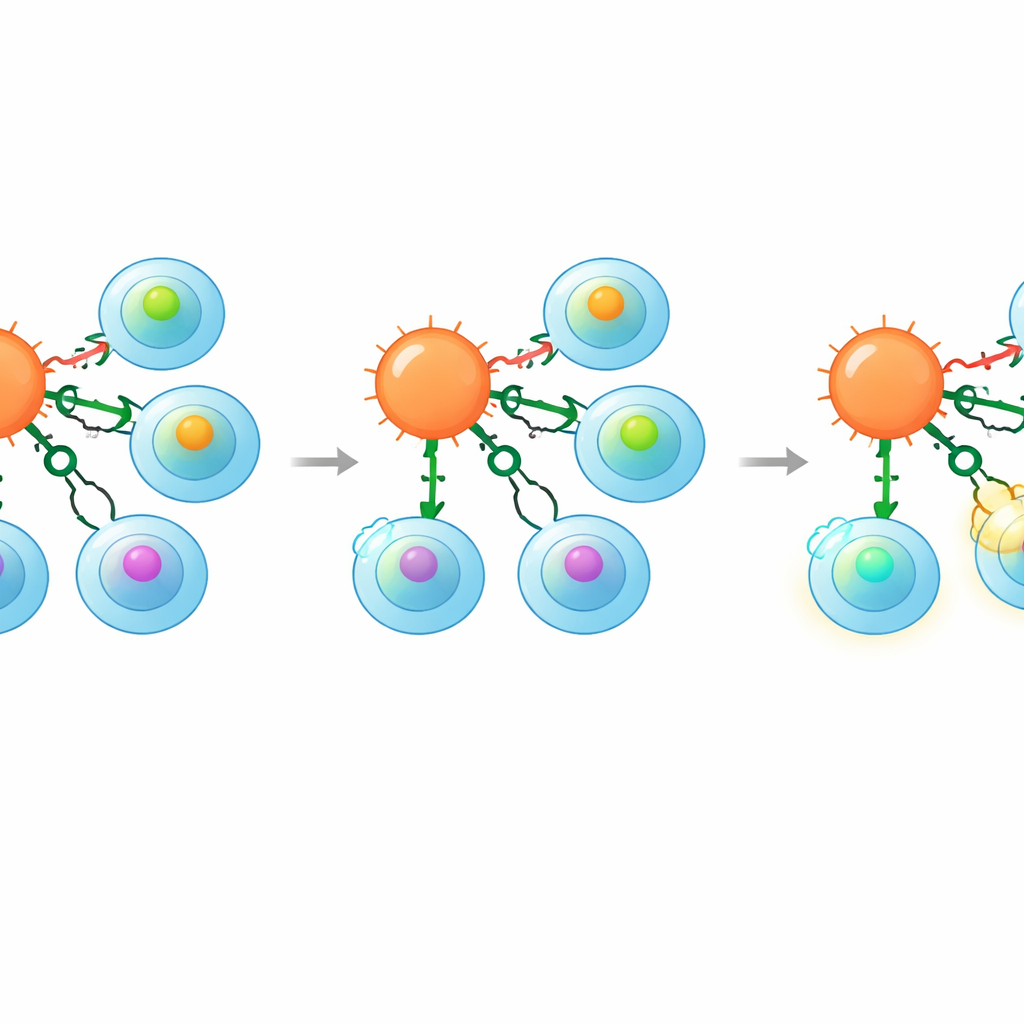
Lehren aus früheren Tragödien
Die Forschenden betrachteten auch eine klinisch bedeutsame Warnungsgeschichte neu. In einer früheren Studie kamen T‑Zellen mit einem Rezeptor gegen das Krebsprotein MAGE‑A3 zum Einsatz; diese Zellen erkannten unerwartet auch ein schwächeres Peptid aus dem Herzmuskelprotein Titin, was zu tödlichen Herzschäden führte. In der neuen Arbeit zeigten die Autorinnen und Autoren, dass das Ausschalten von CD8 in Killer‑T‑Zellen mit demselben Rezeptor deren Reaktion auf das Titin‑Peptid beseitigte, während der Angriff auf Tumorzellen, die tatsächlich MAGE‑A3 exprimieren, erhalten blieb. Diese Demonstration legt nahe, dass Ko‑Rezeptor‑Engineering helfen könnte, ansonsten vielversprechende Rezeptoren zu retten, die aus Sicherheitsgründen aufgegeben werden mussten.
Was das für zukünftige Krebstherapien bedeuten könnte
Aus allgemeiner Sicht lautet die zentrale Botschaft, dass das Team eine Methode gefunden hat, das „Sehen“ von Immunzellen zu schärfen, indem die interne Verkabelung angepasst wird, statt ständig die Linse neu zu designen. Durch das Wechseln der Kombination von Helfermolekülen auf T‑Zellen — insbesondere durch Entfernen von CD8 und Hinzufügen von CD4, wenn der Rezeptor sein Krebsziel stark bindet — entstehen „superselektive“ T‑Zellen. Diese Zellen greifen Tumoren weiterhin energisch an, sind jedoch deutlich weniger anfällig dafür, normales Gewebe anzugreifen, das ähnliche, schwächere Signale präsentiert. Da dieser Ansatz die Hauptrezeptorsequenz unangetastet lässt, könnte er prinzipiell auf viele verschiedene T‑Zell‑Therapien anwendbar sein und einen allgemeinen Weg zu sichererer, präziserer Krebsimmuntherapie eröffnen.
Zitation: Cabezas-Caballero, J., Huhn, A., Kutuzov, M.A. et al. Generation of T cells with reduced off-target cross-reactivities by engineering co-signalling receptors. Nat. Biomed. Eng 10, 753–764 (2026). https://doi.org/10.1038/s41551-025-01563-w
Schlüsselwörter: Krebsimmuntherapie, T‑Zell‑Engineering, T‑Zell‑Rezeptoren, Off‑Target‑Toxizität, Ko‑Rezeptor‑Switching