Clear Sky Science · zh
在具有流感感染免疫记忆的宿主体内重塑对流感疫苗的免疫反应
既往流感感染为何影响未来疫苗接种
大多数人在接种成人流感疫苗之前很久就已经感染过流感。本研究提出了一个简单但重要的问题:早期感染形成的免疫记忆如何改变我们对后续疫苗的反应?研究者使用了一个模拟人类经历的小鼠模型,结果显示,既往流感感染可以将一种标准的蛋白质类流感疫苗,从单纯增强抗体的工具,转变为在肺部——最需要防护的部位——募集强大抗病毒 T 细胞的发动机。
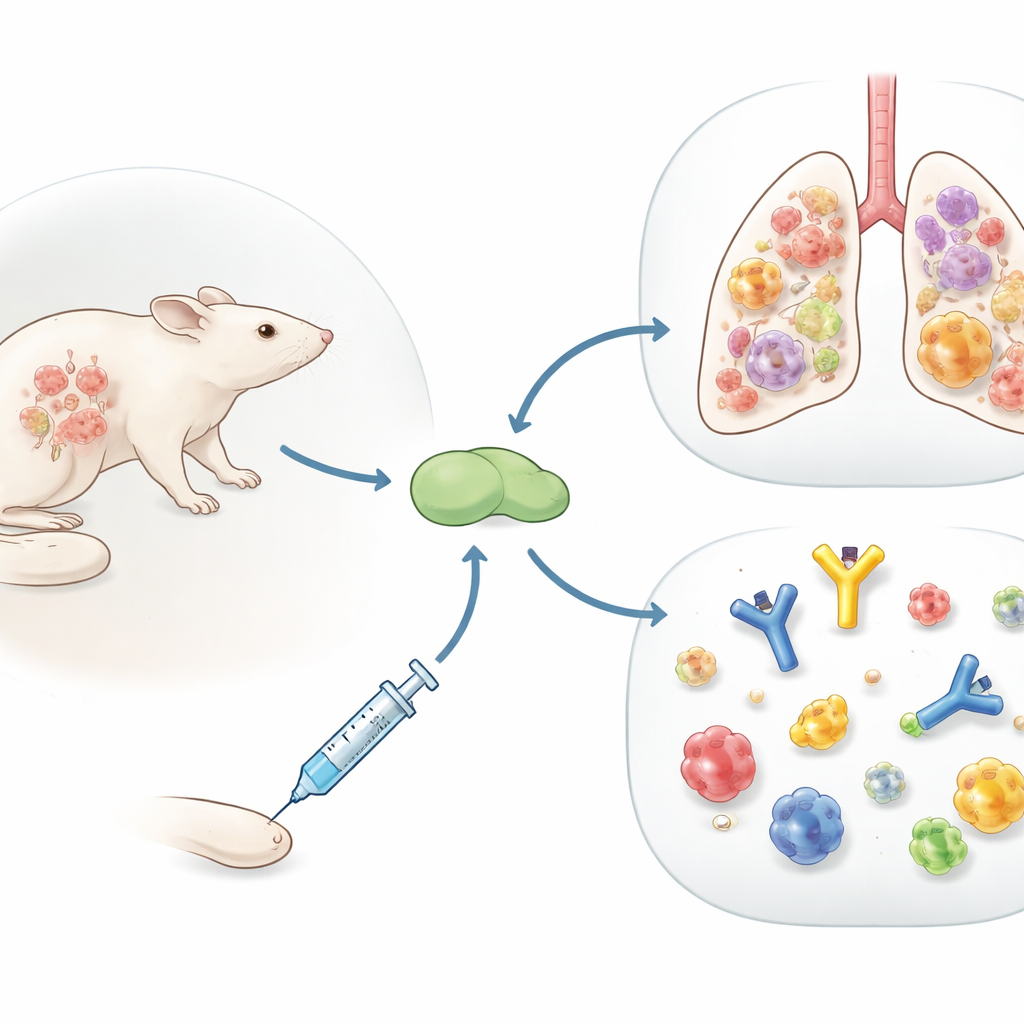
超越抗体的视角
当前的流感疫苗主要旨在诱导针对病毒外衣的抗体,这在病毒未发生太大变异时效果良好。该团队则把注意力放在 CD4 T 细胞上,这类白细胞帮助其他免疫细胞并能识别那些随时间变化较小的病毒片段。他们研究了获批的纯化病毒蛋白疫苗 Flublok,并与两种能激活免疫系统的佐剂之一合用:一种类似于 MF59 的油包水混合物,和一种较新的带正电的脂质颗粒 R-DOTAP。在从未接触过流感的小鼠中,两种配方都能诱导 CD4 T 细胞,但 R-DOTAP 产生了更多且功能谱更广的抗病毒细胞。
首次流感遭遇后发生了什么变化
研究者随后让小鼠感染了 B 型流感,等到远离恢复期后再接种疫苗。此时反应显著不同:引流注射部位的淋巴结中的 CD4 T 细胞迅速被激活,峰值大约在第六天而非第九天。在使用 R-DOTAP 时,这些淋巴结中针对流感的 CD4 T 细胞数量比初次接触的动物高出十倍以上。同样显著的是细胞“性状”的转变:这些细胞不再主要偏向支持抗体产生的信号,而是大量释放与直接抑制病毒和帮助杀伤性 T 细胞相关的强抗病毒因子(如 TNF-α 和干扰素-γ)。
受引导的向肺部迁移
为什么淋巴结中细胞在达到峰值后很快减少?研究团队发现,在有既往感染经历的小鼠中,许多被疫苗激活的 CD4 T 细胞打开了趋化因子受体——这些表面分子类似于在体内移动的 GPS,尤其是 CCR5 和 CXCR3。这些标志已知能引导细胞进入诸如肺部等发炎组织。随着时间推移,带有这些受体的细胞从淋巴结中消失,而特异性针对流感的 CD4 T 细胞在肺组织中积累,并至少持续一个月。这一模式符合这样的模型:疫苗首先在淋巴结扩增流感特异性辅助细胞,然后将被选择的亚群重新定向到气道中定居,成为为下一次感染待命的哨兵。
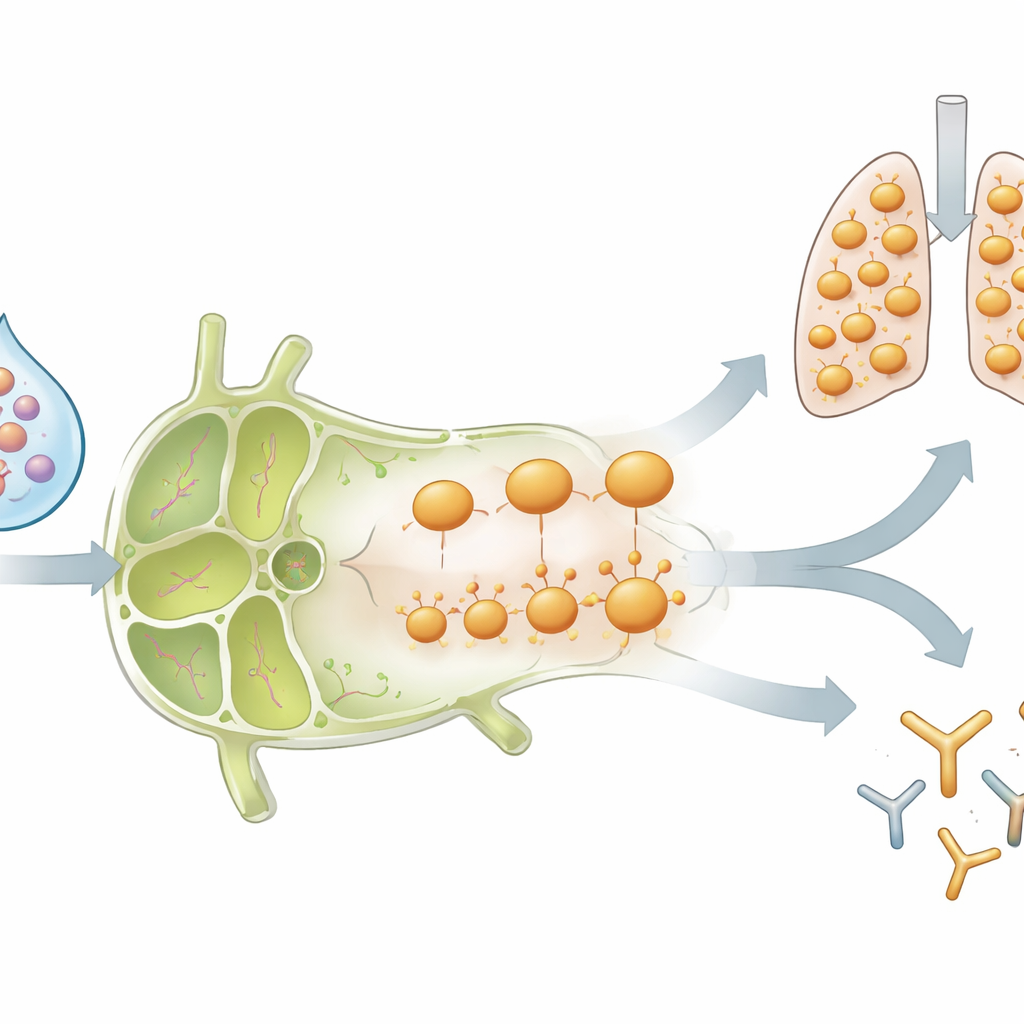
记忆改变了整个疫苗“邻域”
一个重要的检验是,这些效应是否仅限于导致首次感染的特定流感株。Flublok 含有多种流感蛋白类型,其中一种(H3)是感染过的小鼠此前没有 T 细胞记忆的。令人惊讶的是,在既往感染的小鼠中,新诱导的 H3 特异性 CD4 T 细胞的行为与识别原始 B 型流感株的增强细胞非常相似:它们迅速扩增,产生强烈的抗病毒信号,开启趋化因子受体,随后在淋巴结中减少并出现在肺中。对旧有和新出现的病毒蛋白的抗体水平在有感染经历的动物中也更高。这表明早期感染通过炎性分子和招募的免疫细胞改变了引流淋巴结内的“气候”,以致进入该空间的任何新疫苗抗原都会被以不同方式处理。
对更好流感防护的意义
对非专业读者而言,关键信息是:机体以往的流感接触史可以从一个复杂因素转化为一项资产。在这个小鼠模型中,将蛋白疫苗与脂质纳米颗粒佐剂结合使用,所起的作用不仅仅是提高抗体滴度:在有既往流感感染的动物中,它能快速产生学会归巢到肺部的强效辅助 T 细胞,并且还增强了对不相关流感成分的抗体反应。这项工作指向未来的流感疫苗设计方向——不仅追赶最新病毒变体,而是利用既有免疫记忆,有意将长期存在的防御细胞植入气道,从而对不断变化的呼吸道病毒提供更广泛、更持久的保护。
引用: White, C.L., Mengu, L., Sidhu, I.S. et al. Re-shaping the immune response to influenza vaccination in a host with immune memory from influenza infection. npj Vaccines 11, 73 (2026). https://doi.org/10.1038/s41541-026-01397-w
关键词: 流感疫苗接种, 免疫记忆, CD4 T 细胞, 疫苗佐剂, 肺部免疫