Clear Sky Science · it
Rimodellare la risposta immunitaria alla vaccinazione antinfluenzale in un ospite con memoria immune da infezione influenzale
Perché le infezioni influenzali passate contano per le vaccinazioni future
La maggior parte delle persone contrae l’influenza molto prima di sottoporsi a un vaccino antinfluenzale da adulto. Questo studio pone una domanda semplice ma importante: in che modo la memoria lasciata da un’infezione precoce modifica la risposta del nostro organismo a vaccini somministrati successivamente? Utilizzando un modello murino progettato per imitare l’esperienza umana, i ricercatori mostrano che un’infezione influenzale pregressa può trasformare un vaccino proteico standard da un semplice potenziatore di anticorpi in un motore per potenti cellule T antivirali che migrano verso i polmoni, dove la protezione è più necessaria.
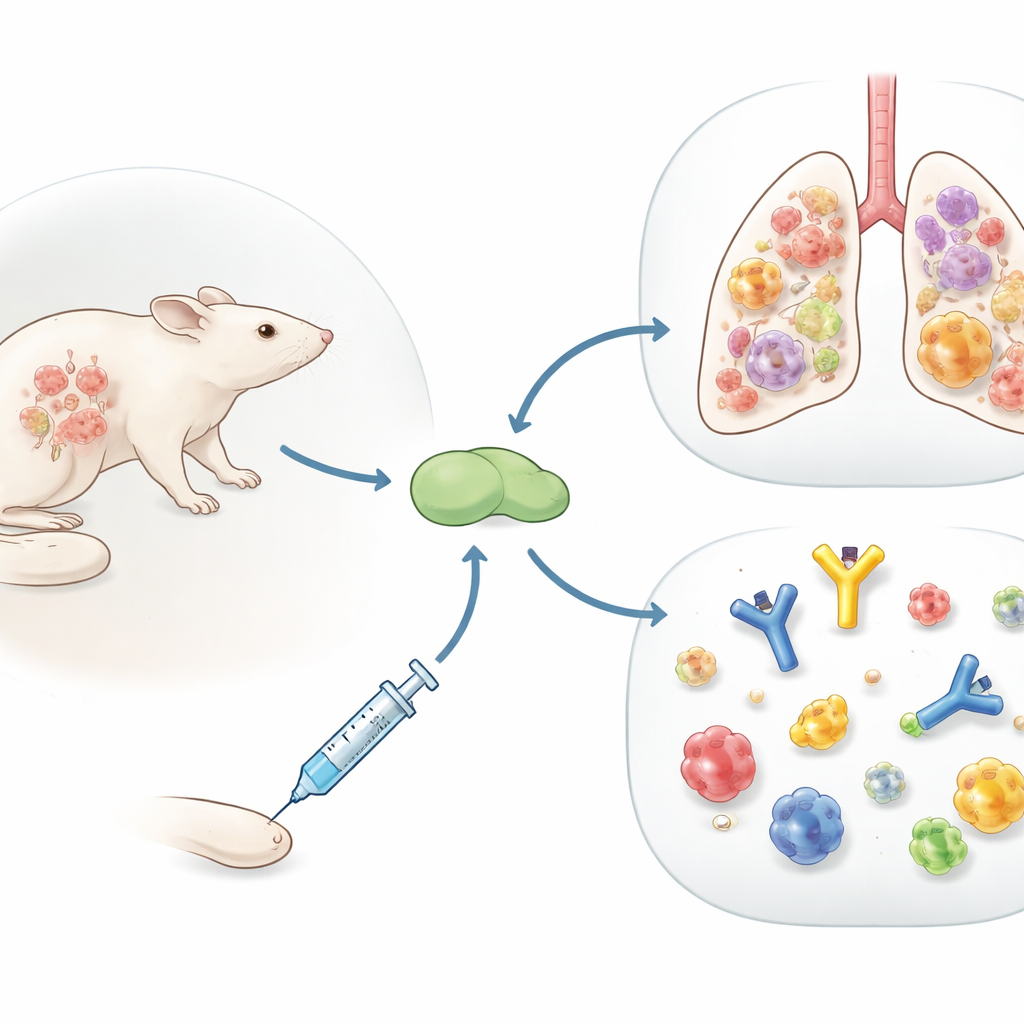
Oltre gli anticorpi
I vaccini antinfluenzali odierni sono progettati principalmente per stimolare anticorpi contro lo strato esterno del virus, cosa che funziona finché il virus non muta. Il gruppo si è invece concentrato sulle cellule T CD4, una classe di globuli bianchi che aiutano altre cellule immunitarie e possono riconoscere porzioni del virus che mutano meno nel tempo. Hanno studiato Flublok, un vaccino antinfluenzale autorizzato costituito solo da proteine virali purificate, somministrato con uno di due componenti aggiuntivi che risvegliano il sistema immunitario: una miscela olio-in-acqua simile a MF59 e una più recente particella lipidica carica positivamente chiamata R-DOTAP. Nei topi mai esposti all’influenza, entrambe le formulazioni hanno attivato le cellule T CD4, ma R-DOTAP ha prodotto molte più cellule con un profilo più ampio di segnali antivirali.
Cosa cambia dopo un primo incontro con l’influenza
I ricercatori hanno quindi infettato i topi con un ceppo di influenza B, atteso fino a molto dopo la guarigione e poi li hanno vaccinati. Ora la risposta appariva molto diversa. Le cellule T CD4 nel linfonodo che drena il sito di iniezione si sono attivate rapidamente, raggiungendo il picco intorno al giorno sei invece che al giorno nove. Con R-DOTAP, il numero di cellule T CD4 specifiche per l’influenza in questi linfonodi era più di dieci volte superiore rispetto agli animali naïve. Altrettanto evidente, la “personalità” delle cellule è cambiata: invece di favorire segnali che supportano principalmente la produzione di anticorpi, le cellule ora rilasciavano forti segnali antivirali (TNF-alfa e interferone-gamma) associati al controllo diretto del virus e al supporto per le cellule T citotossiche.
Migrazione guidata verso i polmoni
Perché l’ondata di cellule nel linfonodo si è rapidamente ridotta dopo il picco? Il team ha scoperto che, nei topi con precedente infezione, molte delle cellule T CD4 indotte dal vaccino hanno attivato recettori per le chemochine—molecole di superficie che funzionano come un sistema GPS per spostarsi nel corpo—in particolare CCR5 e CXCR3. Questi marcatori sono noti per guidare le cellule verso tessuti infiammati come il polmone. Nel tempo, le cellule con questi recettori sono scomparse dal linfonodo, mentre cellule T CD4 specifiche per l’influenza si sono accumulate nel tessuto polmonare, dove sono rimaste per almeno un mese. Questo schema è coerente con un modello in cui il vaccino prima espande gli helper specifici per l’influenza nel linfonodo, quindi reindirizza un sottogruppo selezionato a stabilirsi nelle vie aeree come sentinelle pronte per la prossima infezione.
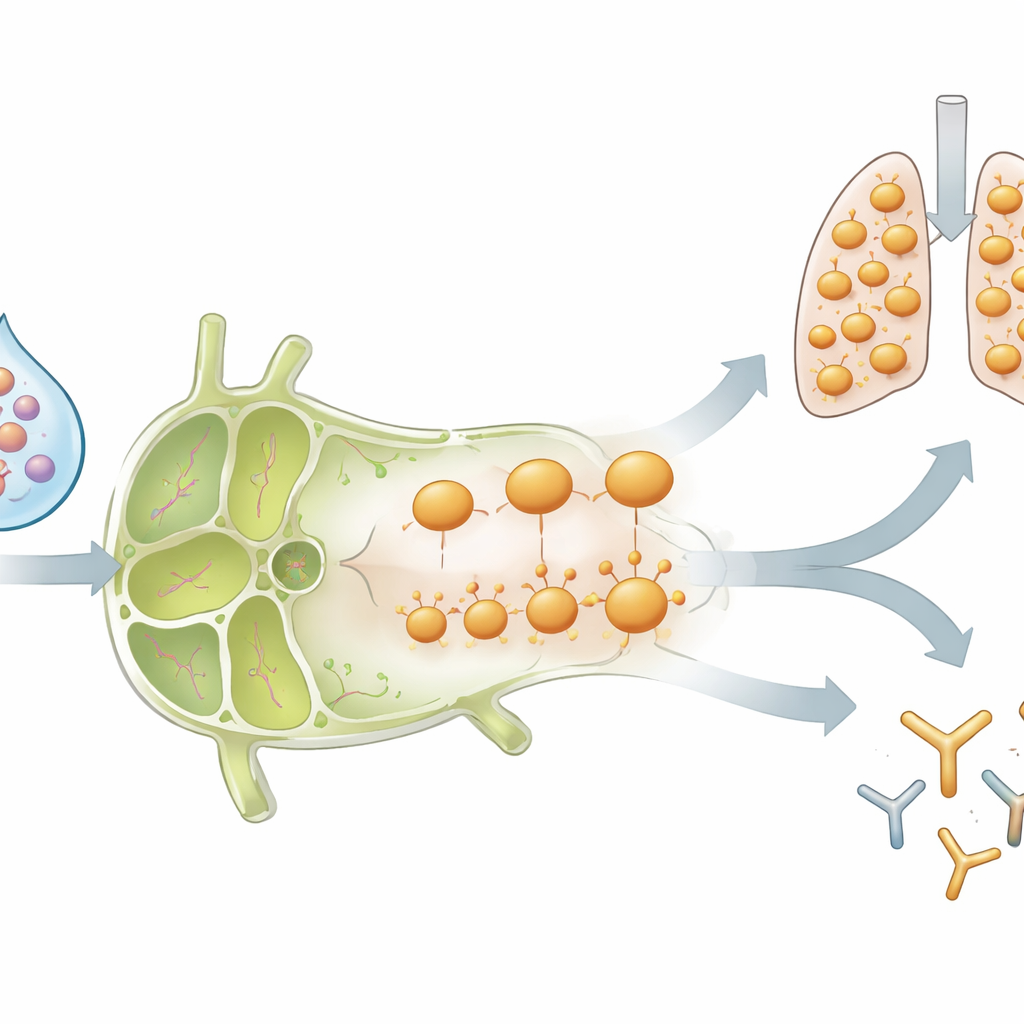
La memoria cambia l’intero ambiente del vaccino
Un test importante è stato verificare se questi effetti fossero limitati allo stesso ceppo influenzale usato per l’infezione iniziale. Flublok contiene diversi tipi di proteine influenzali, incluso un antigene (H3) per il quale i topi infettati non avevano memoria di cellule T preesistente. Sorprendentemente, le cellule T CD4 neo-primate specifiche per H3 nei topi precedentemente infettati si comportavano in modo molto simile alle cellule potenziate che riconoscevano il ceppo originale di influenza B: si espandevano rapidamente, producevano forti segnali antivirali, attivavano recettori per le chemochine e poi diminuivano nel linfonodo mentre comparivano nei polmoni. Anche i livelli di anticorpi contro le proteine virali vecchie e nuove erano più alti negli animali con precedente infezione. Ciò suggerisce che un’infezione precedente rimodella il “clima” all’interno del linfonodo drenante—attraverso molecole infiammatorie e cellule immunitarie reclutate—cosicché qualsiasi nuovo antigene vaccinale che entri in quello spazio venga gestito in modo diverso.
Cosa significa per una migliore protezione dall’influenza
Per i non specialisti, il messaggio chiave è che la storia immunitaria del corpo con l’influenza può essere trasformata da una complicazione in un vantaggio. In questo modello murino, un vaccino a base di proteine combinato con un adiuvante a nanoparticelle lipidiche ha fatto più che aumentare gli anticorpi: negli animali con precedente infezione influenzale, ha generato rapidamente forti cellule T helper che hanno imparato a dirigersi verso il polmone e ha migliorato gli anticorpi anche verso componenti influenzali non correlati. Il lavoro indica la possibilità di sviluppare future vaccinazioni antinfluenzali non solo per inseguire l’ultimo ceppo virale, ma per sfruttare la memoria immunitaria esistente e impiantare deliberatamente cellule difensive a lunga vita nelle vie aeree, dove potrebbero offrire una protezione più ampia e duratura contro virus respiratori in continua evoluzione.
Citazione: White, C.L., Mengu, L., Sidhu, I.S. et al. Re-shaping the immune response to influenza vaccination in a host with immune memory from influenza infection. npj Vaccines 11, 73 (2026). https://doi.org/10.1038/s41541-026-01397-w
Parole chiave: vaccinazione antinfluenzale, memoria immunitaria, cellule T CD4, adiuvanti vaccinali, immunità polmonare