Clear Sky Science · de
Umgestaltung der Immunantwort auf die Influenzaimpfung bei einem Wirt mit immunem Gedächtnis durch Influenza-Infektion
Warum frühere Grippeerkrankungen für spätere Impfungen wichtig sind
Die meisten Menschen bekommen die Grippe zum ersten Mal lange bevor sie jemals eine erwachsene Grippeimpfung erhalten. Diese Studie stellt eine einfache, aber wichtige Frage: Wie verändert dieses frühe Infektionsgedächtnis die Art und Weise, wie unser Körper später auf Impfstoffe reagiert? Mit einem Mausmodell, das die menschliche Erfahrung nachbilden soll, zeigen die Forschenden, dass eine vorausgegangene Grippeinfektion einen standardmäßigen proteinbasierten Grippeimpfstoff von einem einfachen Antikörper-Booster in einen Motor für starke virusbekämpfende T-Zellen verwandeln kann, die sich in die Lunge begeben — genau dorthin, wo Schutz am dringendsten benötigt wird.
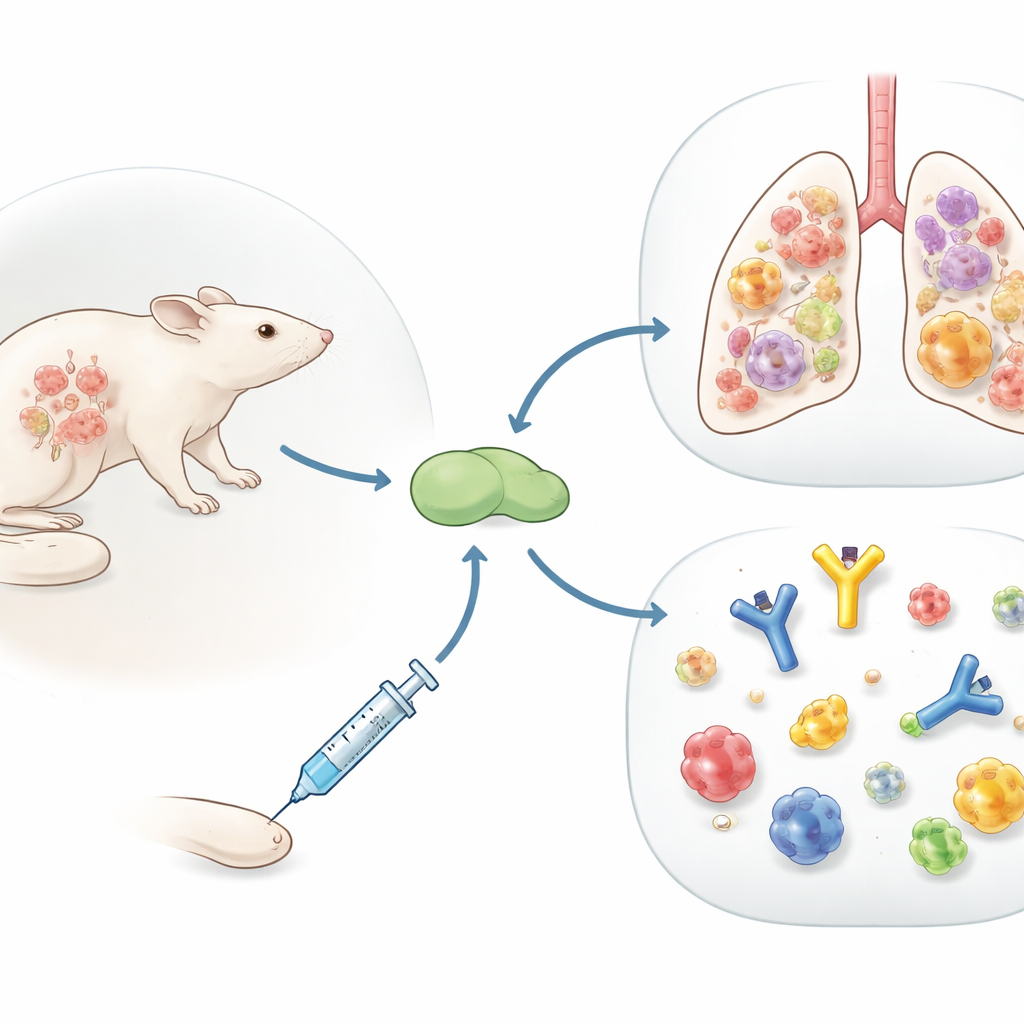
Über Antikörper hinausblicken
Die heutigen Grippeimpfstoffe zielen hauptsächlich darauf ab, Antikörper gegen die äußere Hülle des Virus zu erzeugen, was gut funktioniert, bis das Virus mutiert. Das Team konzentrierte sich stattdessen auf CD4-T-Zellen, eine Klasse weißer Blutkörperchen, die andere Immunzellen unterstützen und Teile des Virus erkennen können, die sich weniger schnell ändern. Sie untersuchten Flublok, einen zugelassenen Grippeimpfstoff, der nur aus gereinigten viralen Proteinen besteht, verabreicht zusammen mit einer von zwei Zusatzkomponenten, die das Immunsystem aktivieren: einer Öl-in-Wasser-Mischung ähnlich MF59 und einem neueren positiv geladenen Lipidpartikel namens R-DOTAP. Bei Mäusen ohne vorherige Grippeexposition lösten beide Versionen CD4-T-Zellen aus, aber R-DOTAP erzeugte viel mehr Zellen mit einer breiteren Mischung von antiviral wirkenden Signalen.
Was sich nach einer ersten Grippeerfahrung ändert
Die Forschenden infizierten Mäuse zunächst mit Influenza B, warteten bis lange nach der Genesung und impften sie dann. Nun sah die Reaktion sehr anders aus. CD4-T-Zellen im Lymphknoten, der die Injektionsstelle ableitet, flammten schnell auf und erreichten ihren Höhepunkt etwa am Tag sechs statt am Tag neun. Mit R-DOTAP war die Zahl der influenza-spezifischen CD4-T-Zellen in diesen Knoten mehr als zehnfach höher als bei naiven Tieren. Ebenso auffällig verschob sich die „Persönlichkeit“ der Zellen: Anstatt Signale zu bevorzugen, die hauptsächlich die Antikörperproduktion unterstützen, schütteten die Zellen nun starke antivirale Signale (TNF-alpha und Interferon-gamma) aus, die mit direkter Virusbekämpfung und Unterstützung für zytotoxische T-Zellen verbunden sind.
Gesteuerte Wanderung in Richtung Lunge
Warum schrumpfte die Flut von Zellen im Lymphknoten kurz nach dem Höhepunkt wieder? Das Team stellte fest, dass bei infektions-erfahrenen Mäusen viele der durch die Impfung ausgelösten CD4-T-Zellen Chemokinrezeptoren einschalteten — Oberflächenmoleküle, die wie ein GPS für die Bewegung durch den Körper wirken — insbesondere CCR5 und CXCR3. Diese Marker sind dafür bekannt, Zellen in entzündete Gewebe wie die Lunge zu lotsen. Mit der Zeit verschwanden Zellen mit diesen Rezeptoren aus dem Lymphknoten, während influenza-spezifische CD4-T-Zellen im Lungengewebe anstiegen und dort mindestens einen Monat lang persistierten. Dieses Muster passt zu einem Modell, in dem der Impfstoff zuerst influenza-spezifische Helfer im Knoten expandiert und dann eine ausgewählte Untergruppe umleitet, damit sie sich in den Luftwegen als Wächter niederlässt, bereit für die nächste Infektion.
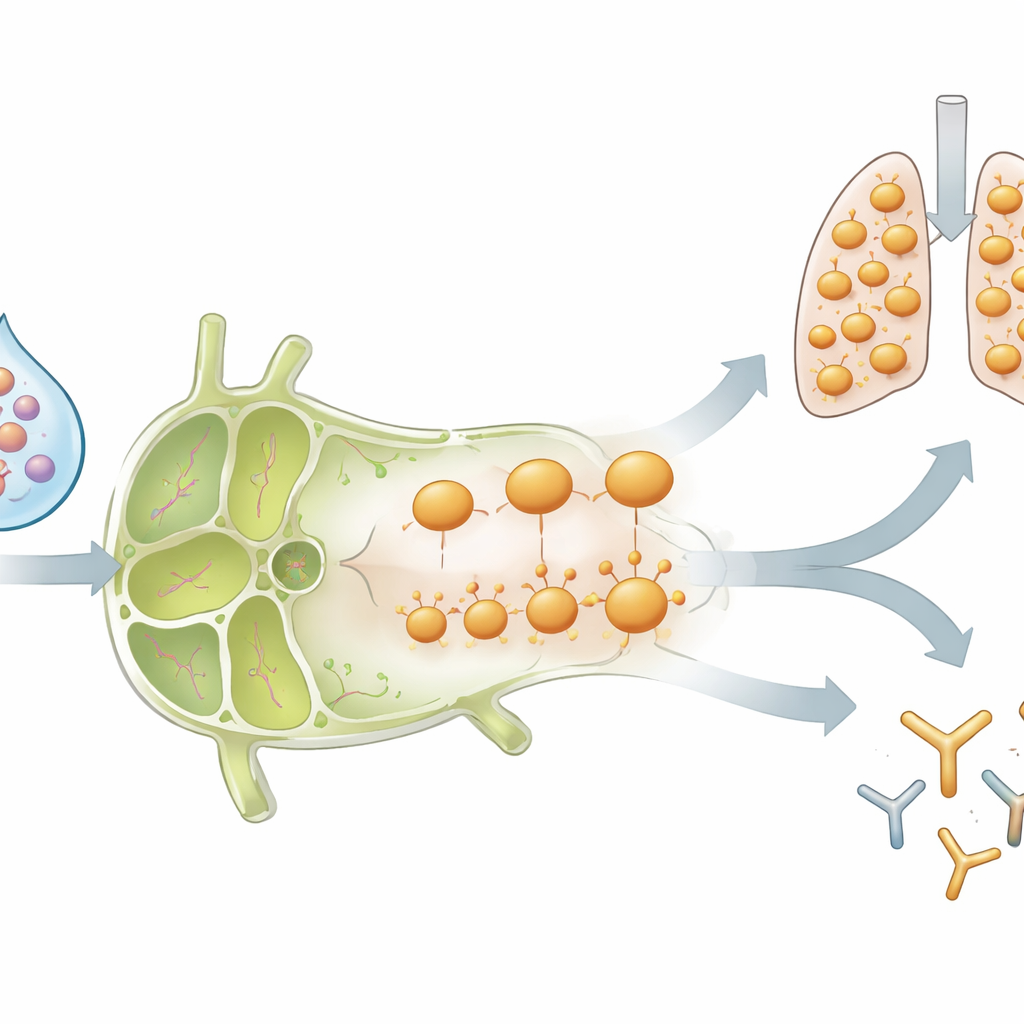
Das Gedächtnis verändert das gesamte Impfstoffumfeld
Ein wichtiger Test war, ob diese Effekte auf genau den für die Erstinfektion verwendeten Stamm begrenzt waren. Flublok enthält mehrere Typen von Grippeproteinen, darunter eines (H3), gegen das die infizierten Mäuse zuvor keine T-Zell-Erinnerung hatten. Überraschenderweise verhielten sich die neu primierten H3-spezifischen CD4-T-Zellen in zuvor infizierten Mäusen ähnlich wie die verstärkten Zellen, die den ursprünglichen Influenza-B-Stamm erkannten: Sie expandierten schnell, produzierten starke antivirale Signale, schalteten Chemokinrezeptoren ein und nahmen dann im Lymphknoten ab, während Zellen in der Lunge erschienen. Auch die Antikörperspiegel gegen sowohl die alten als auch die neuen viralen Proteine waren bei infektionserfahrenen Tieren höher. Das legt nahe, dass eine frühere Infektion das „Klima“ innerhalb des drainierenden Lymphknotens umgestaltet — durch entzündliche Moleküle und rekrutierte Immunzellen — sodass jedes neue Impfstoffantigen, das in diesen Raum gelangt, anders verarbeitet wird.
Was das für besseren Grippeschutz bedeutet
Für Nicht-Spezialisten ist die Kernbotschaft: Die Körpergeschichte mit der Grippe lässt sich von einer Komplikation in einen Vorteil verwandeln. In diesem Mausmodell bewirkte ein proteinbasierter Impfstoff kombiniert mit einem Lipid-Nanopartikel-Adjuvans mehr als nur das Auffrischen von Antikörpern: Bei Tieren mit früherer Grippeinfektion erzeugte er schnell starke Helfer-T-Zellen, die lernten, in die Lunge zu wandern, und erhöhte zudem Antikörper auch gegen nicht verwandte Grippekomponenten. Die Arbeit weist auf zukünftige Grippeimpfungen hin, die nicht nur der neuesten Virenvariante nachjagen, sondern bestehendes Immungedächtnis nutzen und gezielt langlebige Verteidigerzellen in den Atemwegen ansiedeln, wo sie breiteren und dauerhafteren Schutz gegen sich ständig verändernde Atemwegsviren bieten könnten.
Zitation: White, C.L., Mengu, L., Sidhu, I.S. et al. Re-shaping the immune response to influenza vaccination in a host with immune memory from influenza infection. npj Vaccines 11, 73 (2026). https://doi.org/10.1038/s41541-026-01397-w
Schlüsselwörter: Influenzaimpfung, immunes Gedächtnis, CD4-T-Zellen, Impfadjuvantien, Lungenimmunität