Clear Sky Science · pt
Reconfigurando a resposta imune à vacinação contra influenza em um hospedeiro com memória imune de infecção por influenza
Por que infecções anteriores de gripe importam para futuras doses
A maioria das pessoas contrai a gripe muito antes de tomar uma vacina antigripal adulta. Este estudo faz uma pergunta simples, mas importante: como essa memória de infecção precoce altera a forma como nossos corpos respondem a vacinas posteriores? Usando um modelo murino projetado para imitar a experiência humana, os pesquisadores mostram que uma infecção prévia por gripe pode transformar uma vacina proteica padrão de um simples impulsionador de anticorpos em um motor para células T antivirais poderosas que migram para os pulmões, onde a proteção é mais urgentemente necessária.
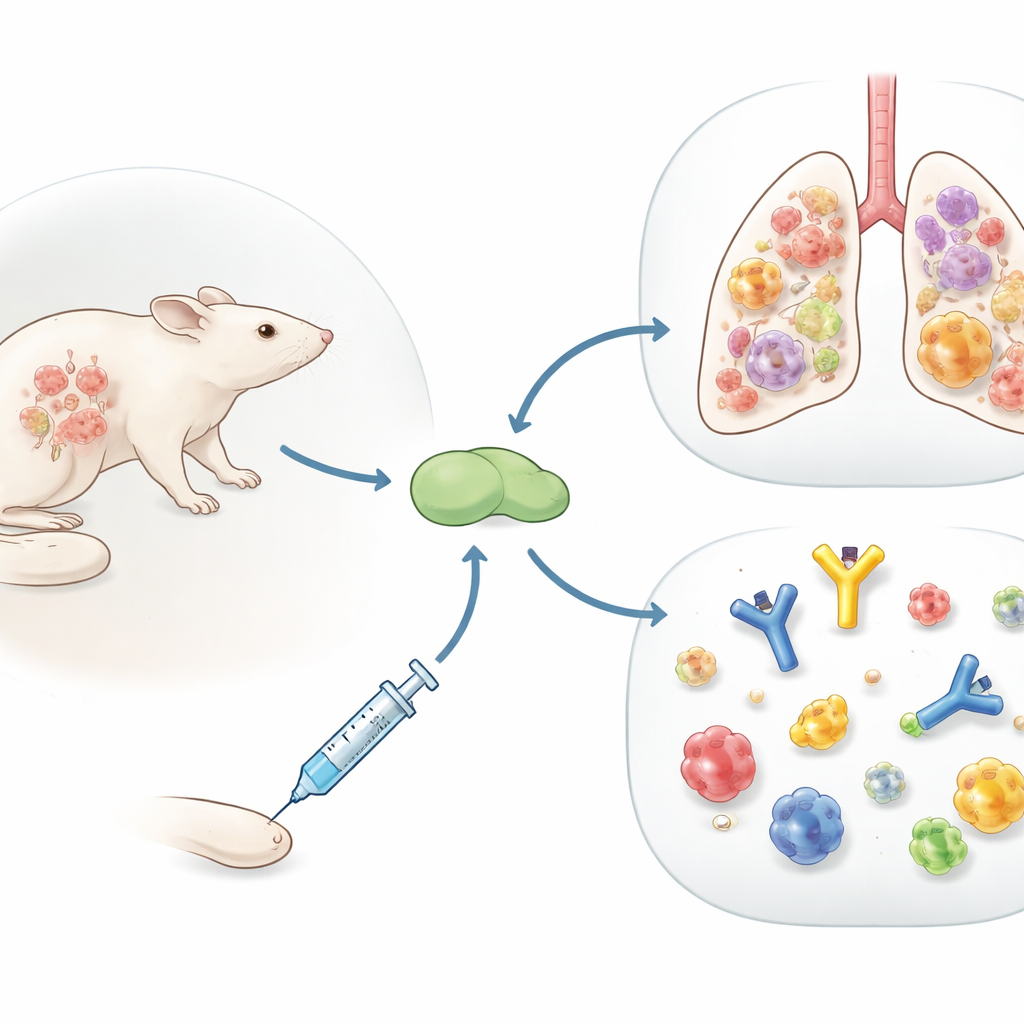
Olhando além dos anticorpos
As vacinas contra a gripe de hoje são formuladas principalmente para elevar anticorpos contra o revestimento externo do vírus, o que funciona bem até o vírus sofrer mutações. A equipe, em vez disso, concentrou-se nas células T CD4, uma classe de glóbulos brancos que ajudam outras células imunes e podem reconhecer partes do vírus que mudam menos ao longo do tempo. Eles estudaram o Flublok, uma vacina licenciada feita apenas de proteínas virais purificadas, administrada com um de dois ingredientes adicionais que despertam o sistema imune: uma mistura óleo-em-água semelhante ao MF59, e uma partícula lipídica carregada positivamente mais nova chamada R-DOTAP. Em camundongos que nunca tinham visto gripe antes, ambas as versões desencadearam células T CD4, mas o R-DOTAP produziu muito mais células com uma mistura mais ampla de sinais antivirais.
O que muda após o primeiro encontro com a gripe
Os pesquisadores então infectaram camundongos com um vírus influenza B, esperaram até muito depois da recuperação e os vacinaram. Agora a resposta parecia bem diferente. As células T CD4 no linfonodo que drena o local da injeção dispararam rapidamente, atingindo o pico por volta do sexto dia em vez do nono. Com R-DOTAP, o número de células T CD4 específicas para influenza nesses linfonodos foi mais de dez vezes maior do que em animais ingênuos. Igualmente marcante, a “personalidade” dessas células mudou: em vez de favorecer sinais que suportam principalmente a produção de anticorpos, as células passaram a liberar fortes sinais antivirais (TNF-alfa e interferon-gama) associados ao controle direto do vírus e ao auxílio para células T citotóxicas.
Migração orientada em direção aos pulmões
Por que a enxurrada de células no linfonodo encolheu rapidamente após o pico? A equipe descobriu que, em camundongos com experiência de infecção, muitas das células T CD4 ativadas pela vacina passaram a expressar receptores de quimiocinas — moléculas de superfície que funcionam como um GPS para se mover pelo corpo — especialmente CCR5 e CXCR3. Esses marcadores são conhecidos por guiar células para tecidos inflamados, como o pulmão. Com o tempo, células com esses receptores desapareceram do linfonodo, enquanto células T CD4 específicas para influenza se acumulavam dentro do tecido pulmonar, onde persistiram por pelo menos um mês. Esse padrão se encaixa em um modelo no qual a vacina primeiro expande auxiliares específicos para influenza no linfonodo e então redireciona um subconjunto selecionado para se estabelecer nas vias aéreas como sentinelas prontas para a próxima infecção.
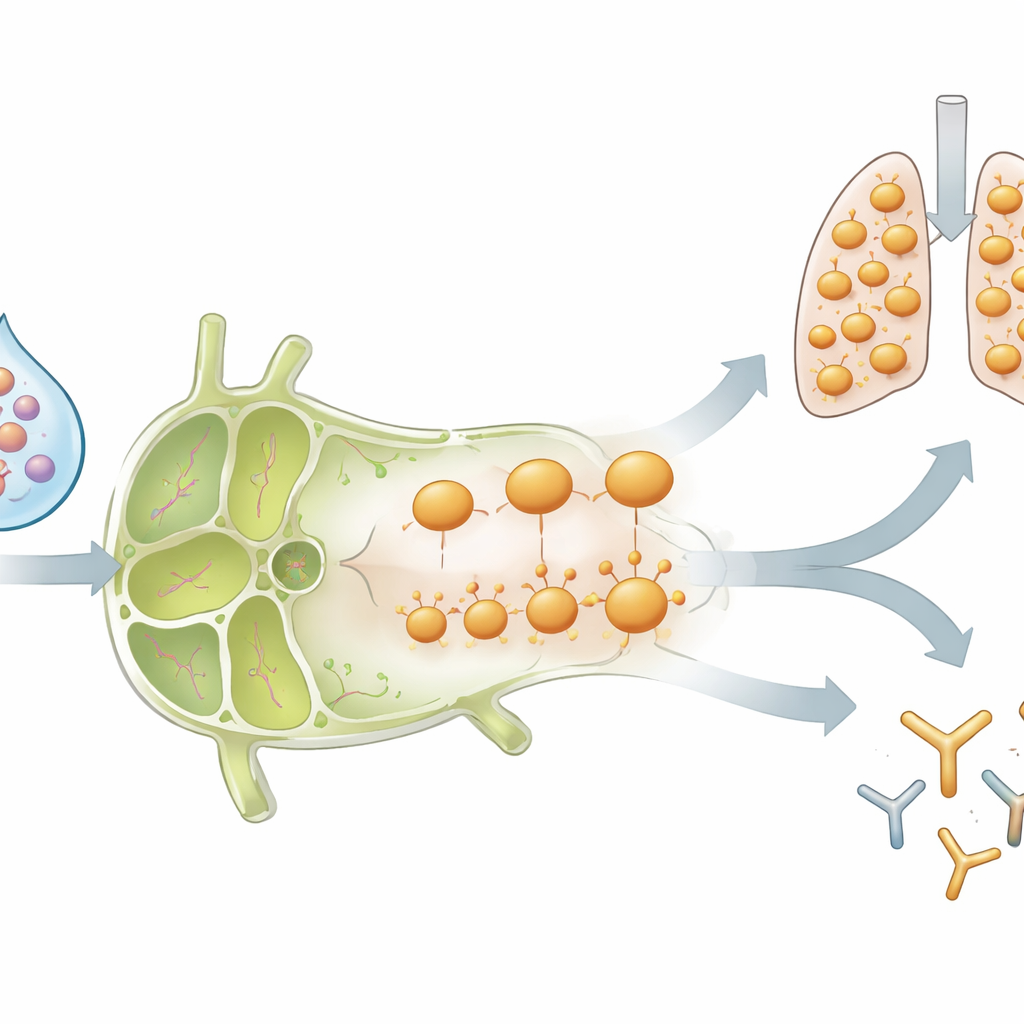
A memória transforma todo o “bairro” vacinal
Um teste importante foi saber se esses efeitos se limitavam à cepa exata de influenza usada na infecção inicial. O Flublok contém vários tipos de proteínas da gripe, incluindo uma (H3) para a qual os camundongos infectados não tinham memória prévia de células T. Surpreendentemente, as células T CD4 recém-primadas específicas para H3 em camundongos previamente infectados comportaram-se de maneira muito semelhante às células aumentadas que reconheciam a cepa original de influenza B: expandiram-se rapidamente, produziram fortes sinais antivirais, ligaram receptores de quimiocinas e então declinaram no linfonodo à medida que surgiam no pulmão. Os níveis de anticorpos contra tanto as proteínas virais antigas quanto as novas também foram maiores em animais com experiência de infecção. Isso sugere que a infecção anterior remodela o “clima” dentro do linfonodo drenante — por meio de moléculas inflamatórias e células imunes recrutadas — de modo que qualquer novo antígeno vacinal que entre nesse espaço seja tratado de forma diferente.
O que isso significa para uma proteção melhor contra a gripe
Para leigos, a mensagem principal é que o histórico do corpo com a gripe pode ser transformado de uma complicação em um ativo. Neste modelo murino, uma vacina proteica combinada com um adjuvante em nanopartícula lipídica fez mais do que complementar anticorpos: em animais com infecção prévia por gripe, gerou rapidamente fortes células T auxiliares que aprenderam a migrar para o pulmão e aumentou os anticorpos mesmo contra componentes virais não relacionados. O trabalho aponta para futuras vacinas antigripais projetadas não apenas para seguir a variante viral mais recente, mas para aproveitar a memória imune existente e plantar deliberadamente células defensoras de longa duração nas vias aéreas, onde podem oferecer proteção mais ampla e duradoura contra vírus respiratórios em constante mudança.
Citação: White, C.L., Mengu, L., Sidhu, I.S. et al. Re-shaping the immune response to influenza vaccination in a host with immune memory from influenza infection. npj Vaccines 11, 73 (2026). https://doi.org/10.1038/s41541-026-01397-w
Palavras-chave: vacinação contra influenza, memória imune, células T CD4, adjuvantes vacinais, imunidade pulmonar