Clear Sky Science · es
Reconfigurar la respuesta inmune a la vacunación contra la gripe en un huésped con memoria inmune por infección gripal
Por qué las infecciones gripales previas importan para futuras vacunas
La mayoría de las personas contrae la gripe mucho antes de ponerse la primera vacuna adulta. Este estudio plantea una pregunta simple pero importante: ¿cómo cambia esa memoria de una infección temprana la forma en que nuestros cuerpos responden a vacunas posteriores? Usando un modelo murino diseñado para imitar la experiencia humana, los investigadores muestran que una infección gripal previa puede transformar una vacuna proteica estándar de la gripe, que actúa como un simple impulsor de anticuerpos, en una máquina que genera potentes células T antivirales que se dirigen a los pulmones, donde la protección es más urgente.
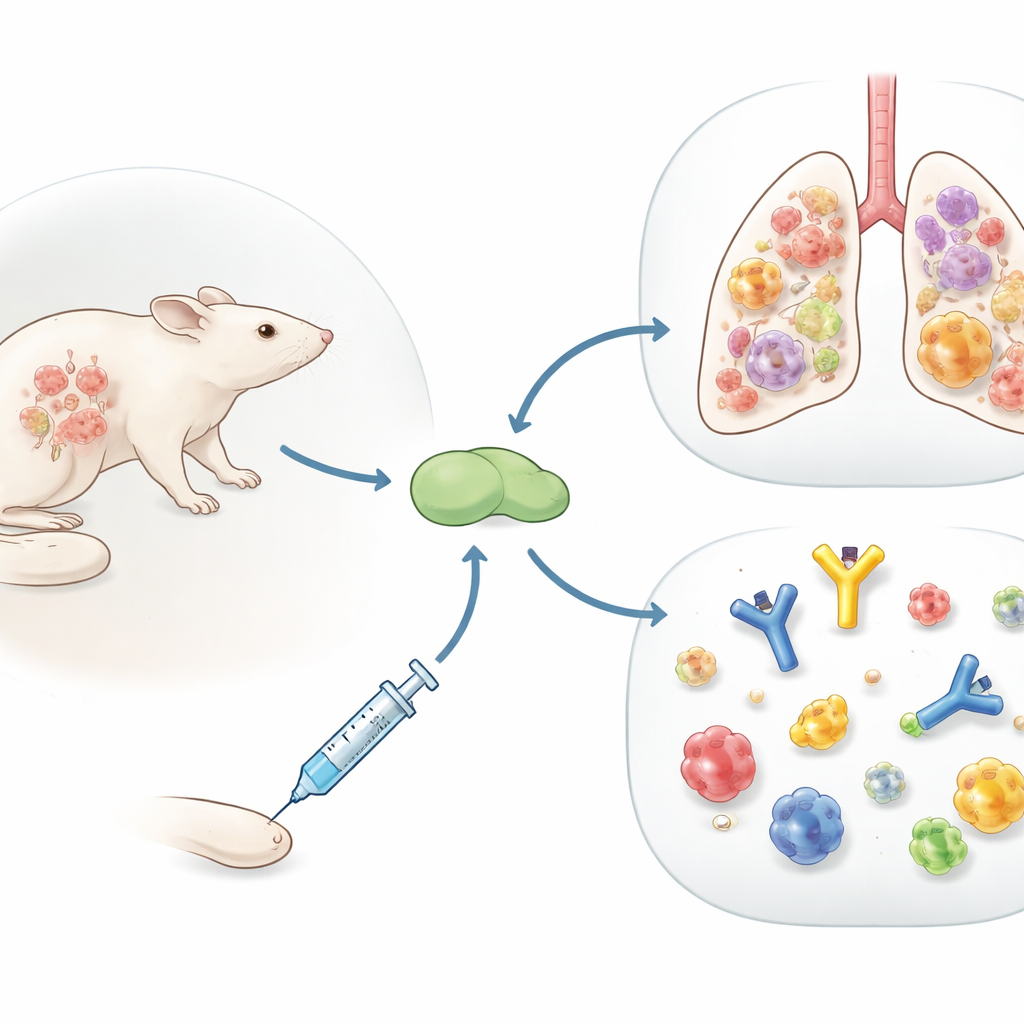
Mirando más allá de los anticuerpos
Las vacunas antigripales actuales se diseñan principalmente para elevar anticuerpos contra la cubierta externa del virus, lo que funciona bien hasta que el virus muta. El equipo, en cambio, se centró en las células T CD4, una clase de glóbulos blancos que ayudan a otras células inmunitarias y pueden reconocer partes del virus que cambian menos con el tiempo. Estudiaron Flublok, una vacuna licenciada contra la gripe compuesta únicamente por proteínas virales purificadas, administrada con uno de dos ingredientes adicionales que activan el sistema inmune: una mezcla aceite-en-agua similar a MF59, y una partícula lipídica cargada positivamente más nueva llamada R-DOTAP. En ratones que nunca habían visto la gripe, ambas versiones desencadenaron células T CD4, pero R-DOTAP produjo muchas más células con una mezcla más amplia de señales antivirales.
Qué cambia después del primer encuentro con la gripe
Luego, los investigadores infectaron ratones con gripe B, esperaron hasta mucho después de la recuperación y los vacunaron. Ahora la respuesta se vio muy diferente. Las células T CD4 en el ganglio linfático que drena el sitio de la inyección se activaron rápidamente, alcanzando su pico alrededor del día seis en lugar del día nueve. Con R-DOTAP, el número de células T CD4 específicas de la gripe en estos ganglios fue más de diez veces mayor que en animales vírgenes. Igual de llamativo fue que la “personalidad” de las células cambió: en lugar de favorecer señales que principalmente apoyan la producción de anticuerpos, las células ahora secretaron fuertes señales antivirales (TNF-alfa e interferón gamma) asociadas al control directo del virus y al apoyo a las células T citotóxicas.
Migración guiada hacia los pulmones
¿Por qué la avalancha de células en el ganglio linfático se redujo rápidamente después de alcanzar su pico? El equipo descubrió que, en ratones con experiencia de infección, muchas de las células T CD4 activadas por la vacuna encendieron receptores de quimiocinas—moléculas de superficie que actúan como un GPS para moverse por el cuerpo—especialmente CCR5 y CXCR3. Estos marcadores son conocidos por guiar células hacia tejidos inflamados como el pulmón. Con el tiempo, las células con estos receptores desaparecieron del ganglio linfático, mientras que las células T CD4 específicas de la gripe se acumularon dentro del tejido pulmonar, donde persistieron al menos durante un mes. Este patrón encaja con un modelo en el que la vacuna primero expande los ayudantes específicos de la gripe en el ganglio y luego reencamina a un subconjunto seleccionado para asentarse en las vías respiratorias como centinelas listos para la próxima infección.
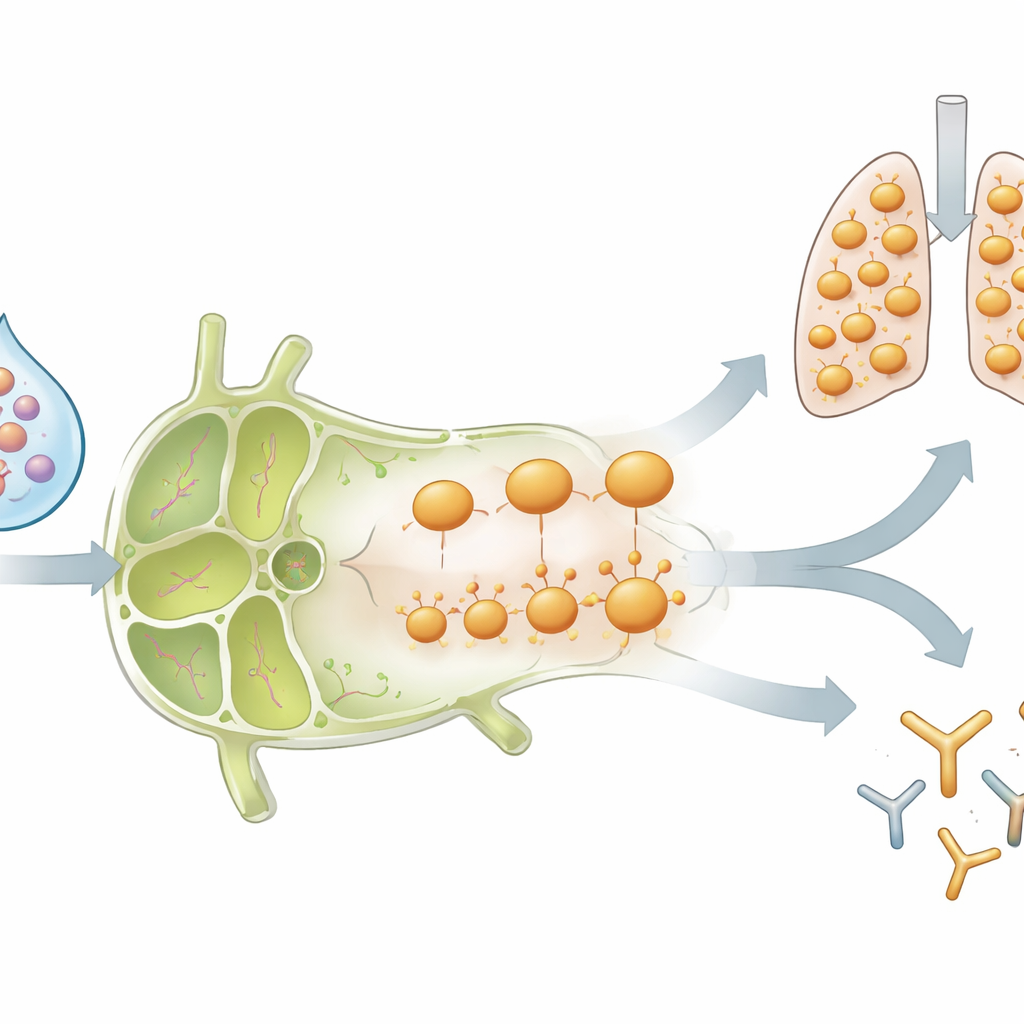
La memoria cambia todo el vecindario vacunal
Una prueba importante fue si estos efectos se limitaban exactamente a la cepa viral usada en la infección inicial. Flublok contiene varios tipos de proteínas gripales, incluida una (H3) para la cual los ratones infectados no tenían memoria previa de células T. Sorprendentemente, las células T CD4 recién iniciadas específicas de H3 en ratones previamente infectados se comportaron de forma muy parecida a las células potenciadas que reconocían la cepa original de gripe B: se expandieron rápidamente, produjeron fuertes señales antivirales, activaron receptores de quimiocinas y luego disminuyeron en el ganglio linfático a medida que aparecían células en el pulmón. Los niveles de anticuerpos contra las proteínas virales antiguas y nuevas también fueron más altos en animales con experiencia de infección. Esto sugiere que la infección anterior remodela el “clima” dentro del ganglio linfático drenante—mediante moléculas inflamatorias y células inmunes reclutadas—de modo que cualquier nuevo antígeno vacunal que entre en ese espacio se procesa de forma diferente.
Qué significa esto para una mejor protección contra la gripe
Para quienes no son especialistas, el mensaje clave es que la historia del cuerpo con la gripe puede convertirse de una complicación en un activo. En este modelo murino, una vacuna basada en proteínas combinada con un adyuvante en nanopartículas lipídicas hizo más que aumentar anticuerpos: en animales con infección previa, generó rápidamente potentes células T ayudantes que aprendieron a dirigirse al pulmón y aumentó los anticuerpos incluso frente a componentes gripales no relacionados. El trabajo apunta hacia vacunas futuras diseñadas no solo para seguir la última variante viral, sino para aprovechar la memoria inmune existente y plantar deliberadamente células defensoras de larga duración en las vías respiratorias, donde pueden ofrecer una protección más amplia y duradera contra virus respiratorios en constante cambio.
Cita: White, C.L., Mengu, L., Sidhu, I.S. et al. Re-shaping the immune response to influenza vaccination in a host with immune memory from influenza infection. npj Vaccines 11, 73 (2026). https://doi.org/10.1038/s41541-026-01397-w
Palabras clave: vacunación contra la gripe, memoria inmune, células T CD4, adyuvantes de vacunas, inmunidad pulmonar