Clear Sky Science · tr
İnfluenza enfeksiyonundan gelen immün belleği olan bir konakta influenza aşısına verilen immün yanıtı yeniden şekillendirmek
Neden geçmiş grip enfeksiyonları sonraki aşıları etkiler
Çoğu kişi yetişkin grip aşısı için kolunu sıvazlamadan çok önce ilk kez gribe yakalanır. Bu çalışma basit ama önemli bir soruyu soruyor: erken enfeksiyon belleği, vücudumuzun sonraki aşı yanıtını nasıl değiştirir? İnsan deneyimini taklit etmek üzere tasarlanmış bir fare modeli kullanan araştırmacılar, önceki grip enfeksiyonunun standart protein bazlı bir griple aşıyı basit bir antikor takviyesinden, akciğerlere göç eden ve virüsle doğrudan savaşabilecek güçlü T hücreleri üreten bir motor hâline dönüştürebileceğini gösteriyor — korunmanın en çok gerektiği yer akciğerlerdir.
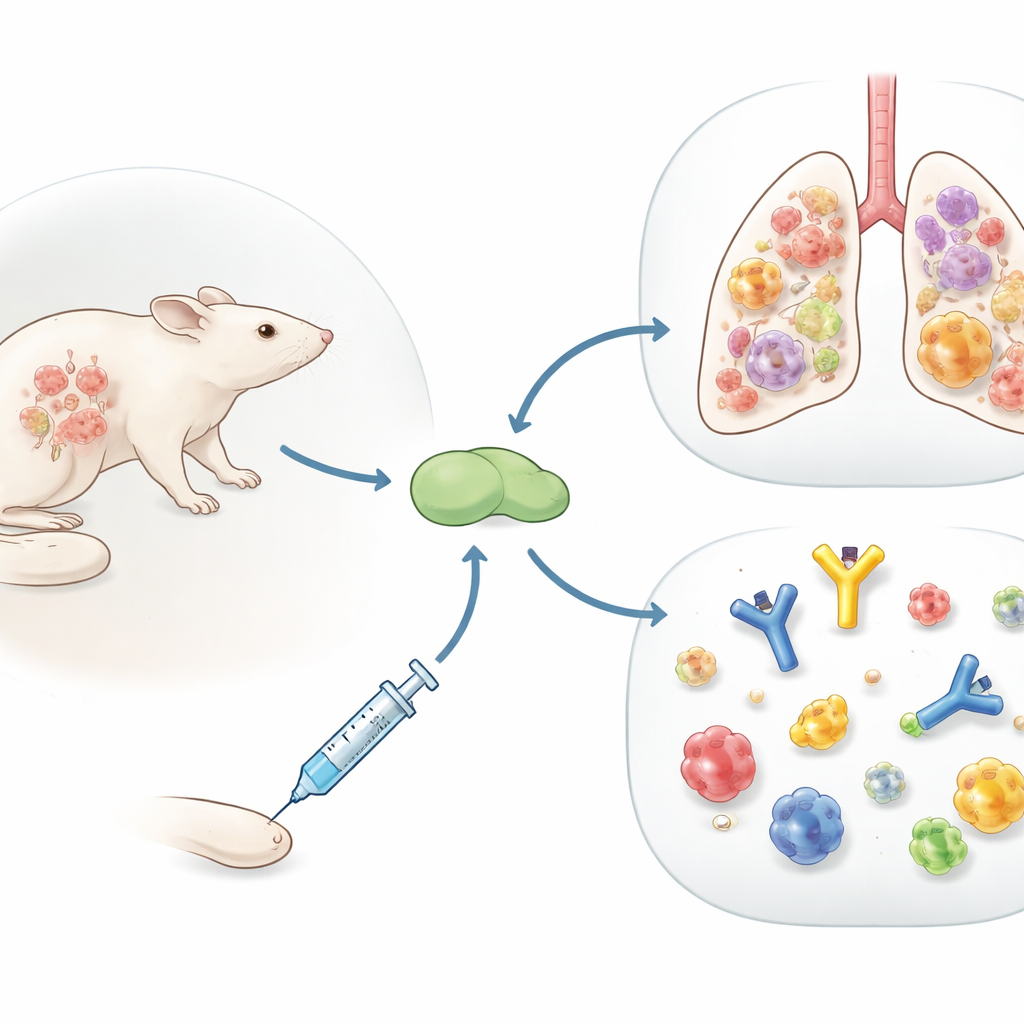
Antikorlardan öteye bakmak
Bugünün grip aşıları esas olarak virüsün dış örtüsüne karşı antikor yükseltmeye yönelik olarak tasarlanır; bu, virüs mutasyona uğrayana kadar iyi çalışır. Araştırma ekibi bunun yerine diğer immün hücrelere yardım eden ve zaman içinde daha az değişen viral parçaları tanıyabilen bir beyaz kan hücresi sınıfı olan CD4 T hücrelerine odaklandı. Saflaştırılmış viral proteinlerden oluşan ve onaylı bir aşı olan Flublok’u, immün sistemi uyaran iki yardımcı bileşenden biriyle birlikte incelediler: MF59 benzeri bir yağ‑içinde‑su karışımı ve pozitif yüklü yeni bir lipid parçacığı olan R‑DOTAP. Daha önce gribi hiç görmemiş farelerde her iki versiyon da CD4 T hücrelerini tetikledi, fakat R‑DOTAP daha geniş bir antiviral sinyal karışımıyla çok daha fazla hücre üretti.
İlk grip karşılaşmasından sonra neler değişiyor
Araştırmacılar daha sonra farelere bir influenza B enfeksiyonu verdiler, iyileşmelerinden uzun süre sonra aşıladılar. Artık yanıt çok farklı görünüyordu. Enjeksiyon bölgesini drene eden lenf nodundaki CD4 T hücreleri hızla alevlendi ve zirveye dokuzuncu gün yerine yaklaşık altıncı günde ulaştı. R‑DOTAP ile bu nodlardaki gripe özgü CD4 T hücrelerinin sayısı, naïf hayvanlardakinden on kattan fazla fazlaydı. Aynı derecede çarpıcı olarak hücrelerin “kişiliği” değişmişti: ağırlıklı olarak antikor üretimini destekleyen sinyalleri tercih etmek yerine, hücreler artık doğrudan virüs kontrolü ve katil T hücrelerine yardım ile ilişkilendirilen güçlü antiviral sinyaller (TNF‑alfa ve interferon‑gama) yayıyordu.
Akciğerlere yönlendiren göç
Lenf nodundaki hücre seli neden zirveden sonra hızla azaldı? Ekip, enfeksiyon tecrübesi olan farelerde aşıyla tetiklenen birçok CD4 T hücresinin özellikle CCR5 ve CXCR3 olmak üzere kemokin reseptörlerini —vücutta hareket etmek için bir GPS gibi çalışan yüzey moleküllerini— açtığını buldu. Bu belirteçlerin iltihaplı dokulara, örneğin akciğere rehberlik ettiği bilinmektedir. Zamanla bu reseptörleri taşıyan hücreler lenf nodundan kaybolurken, gripe özgü CD4 T hücreleri akciğer dokusunda birikti ve en az bir ay boyunca sürdü. Bu desen, aşının önce nodda gripe özgü yardımcıları genişlettiği, ardından seçilmiş bir alt kümenin hava yollarında bekçi hücreleri olarak yerleşmek üzere yönlendirildiği bir modeli destekliyor.
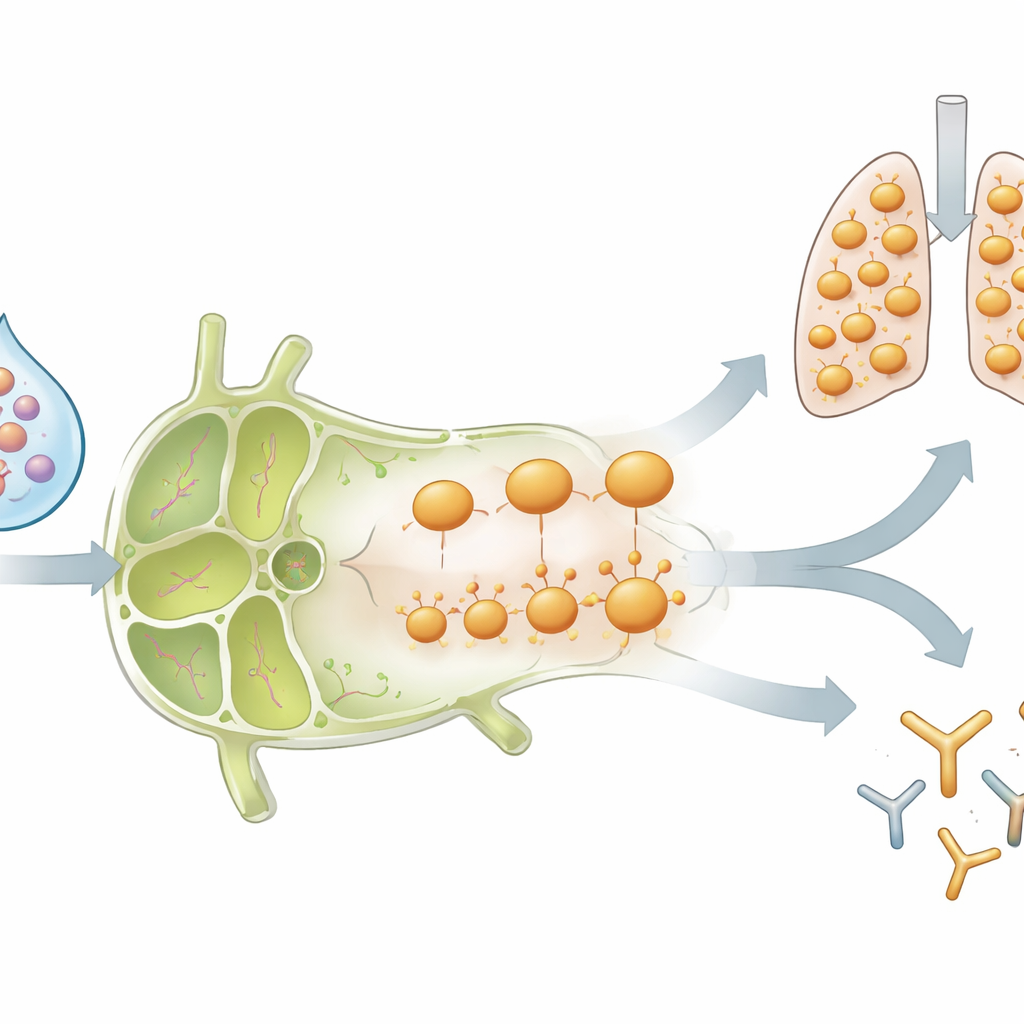
Bellek tüm aşı çevresini değiştiriyor
Önemli bir test, bu etkilerin ilk enfeksiyon için kullanılan tam suşla sınırlı olup olmadığıydı. Flublok içinde, enfekte farelerin önceden T hücre belleğine sahip olmadığı bir tür (H3) de dahil olmak üzere birkaç grip proteini bulunur. Sürpriz şekilde, önceki enfeksiyonlu farelerde yeni uyarılmış H3‑spesifik CD4 T hücreleri, orijinal influenza B suşunu tanıyan güçlendirilmiş hücreler gibi davrandı: hızla genişlediler, güçlü antiviral sinyaller ürettiler, kemokin reseptörlerini açtılar ve daha sonra hücreler akciğerde görünürken lenf nodunda azaldılar. Hem eski hem yeni viral proteinlere karşı antikor düzeyleri de enfeksiyon tecrübesi olan hayvanlarda daha yüksekti. Bu, önceki enfeksiyonun, drenaj yapan lenf nodu içindeki “iklimi” —inflamatuar moleküller ve toplanmış immün hücreler aracılığıyla— yeniden şekillendirerek o alana giren herhangi yeni aşı antijeninin farklı şekilde ele alınmasına yol açtığını düşündürür.
Bu, daha iyi grip koruması için ne anlama geliyor
Uzman olmayanlar için ana mesaj, vücudun grip geçmişinin bir sorun olmaktan ziyade bir avantaja dönüştürülebileceğidir. Bu fare modelinde, lipid nanoparçacık adjuvanı ile birlikte verilen protein bazlı bir aşı sadece antikorları tamamlamakla kalmadı: geçmişte grip geçirmiş hayvanlarda hızla akciğere göç etmeyi öğrenen güçlü yardımcı T hücreleri üretti ve ilişkili olmayan grip bileşenlerine karşı antikorları bile artırdı. Çalışma, gelecek grip aşılarının yalnızca en son viral varyantın peşinden gitmek yerine mevcut immün belleği kullanmayı ve hava yollarında uzun ömürlü savunucu hücreler yerleştirmeyi hedefleyebileceğini; böylece değişen solunum virüslerine karşı daha geniş ve daha kalıcı koruma sağlayabileceğini işaret ediyor.
Atıf: White, C.L., Mengu, L., Sidhu, I.S. et al. Re-shaping the immune response to influenza vaccination in a host with immune memory from influenza infection. npj Vaccines 11, 73 (2026). https://doi.org/10.1038/s41541-026-01397-w
Anahtar kelimeler: influenza aşılaması, immün bellek, CD4 T hücreleri, aşı adjuvanları, akciğer bağışıklığı