Clear Sky Science · fr
Remodeler la réponse immunitaire à la vaccination contre la grippe chez un hôte porteur d’une mémoire immunitaire issue d’une infection grippale
Pourquoi les infections grippales passées comptent pour les vaccinations futures
La plupart des personnes attrapent la grippe bien avant de recevoir un vaccin antigrippal adulte. Cette étude pose une question simple mais importante : comment cette mémoire issue d’infections précoces modifie-t-elle la façon dont notre organisme réagit à des vaccins ultérieurs ? À l’aide d’un modèle murin conçu pour imiter l’expérience humaine, les chercheurs montrent qu’une infection grippale antérieure peut transformer un vaccin protéique standard contre la grippe, qui sert habituellement à renforcer les anticorps, en un moteur produisant de puissantes cellules T effectrices dirigées vers les poumons, là où la protection est la plus nécessaire.
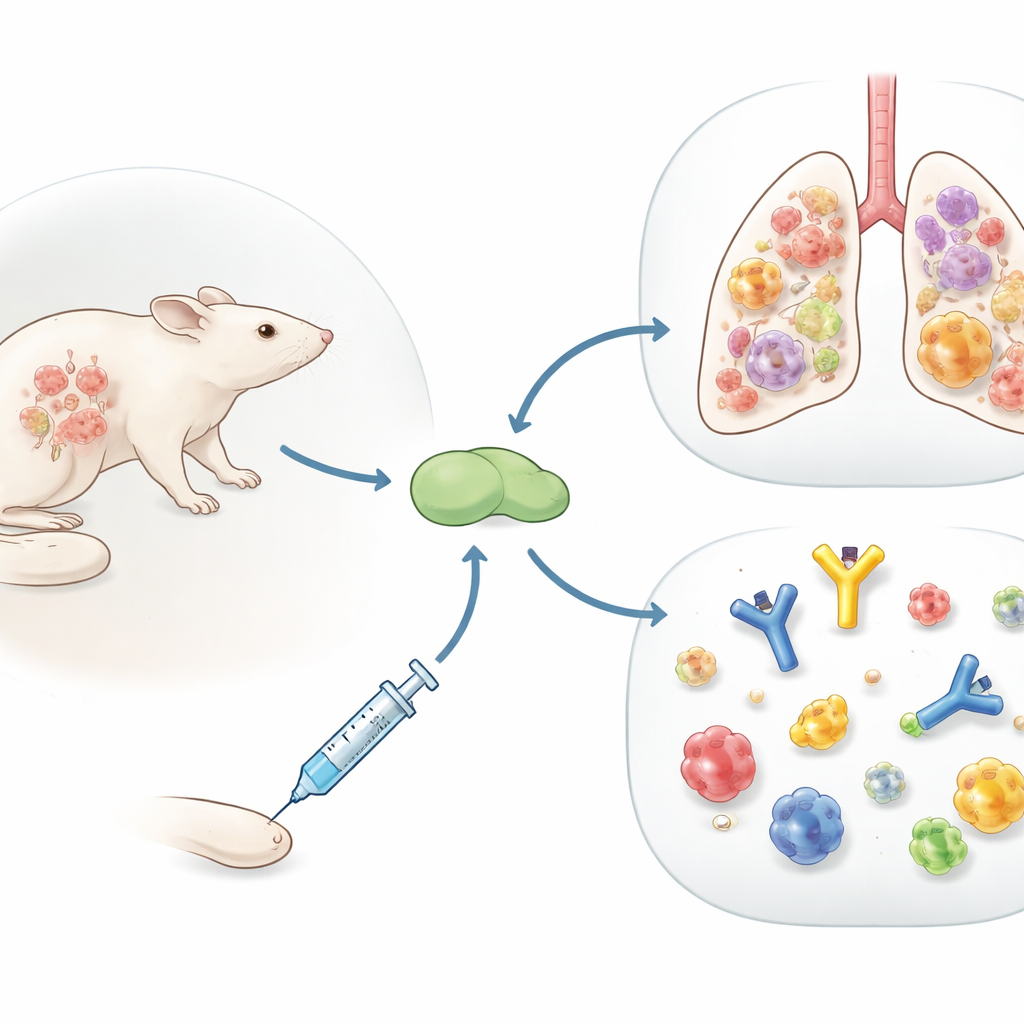
Regarder au-delà des anticorps
Les vaccins antigrippaux actuels sont principalement conçus pour induire des anticorps contre l’enveloppe virale, ce qui fonctionne tant que le virus ne mute pas. L’équipe s’est plutôt concentrée sur les cellules T CD4, une catégorie de globules blancs qui aident les autres cellules immunitaires et peuvent reconnaître des parties du virus moins sujettes aux changements. Ils ont étudié Flublok, un vaccin antigrippal autorisé composé uniquement de protéines virales purifiées, administré avec l’un des deux ingrédients stimulants du système immunitaire : un mélange huile-dans-eau proche de MF59, et une particule lipide chargée positivement plus récente appelée R-DOTAP. Chez des souris naïves à la grippe, les deux formulations ont déclenché des cellules T CD4, mais R-DOTAP a généré beaucoup plus de cellules avec un éventail plus large de signaux antiviraux.
Que change une première rencontre avec la grippe
Les chercheurs ont ensuite infecté des souris avec un virus B de la grippe, attendu la convalescence, puis les ont vaccinées. La réponse a alors été très différente. Les cellules T CD4 dans le ganglion lymphatique drainant le site d’injection se sont activées rapidement, culminant autour du sixième jour au lieu du neuvième. Avec R-DOTAP, le nombre de cellules T CD4 spécifiques à la grippe dans ces ganglions était plus de dix fois supérieur à celui des animaux naïfs. Autre point frappant : la « personnalité » des cellules a changé : au lieu de privilégier des signaux favorisant principalement la production d’anticorps, elles ont désormais sécrété de puissants signaux antiviraux (TNF-alpha et interféron-gamma) associés au contrôle direct du virus et à l’aide pour les cellules T cytotoxiques.
Migration dirigée vers les poumons
Pourquoi cet afflux de cellules dans le ganglion a-t-il rapidement diminué après son pic ? L’équipe a constaté que, chez les souris ayant déjà été infectées, nombre des cellules T CD4 déclenchées par le vaccin ont activé des récepteurs chimiques—des molécules de surface qui fonctionnent comme un GPS pour se déplacer dans l’organisme—en particulier CCR5 et CXCR3. Ces marqueurs sont connus pour guider les cellules vers des tissus enflammés comme le poumon. Au fil du temps, les cellules exprimant ces récepteurs ont disparu du ganglion lymphatique, tandis que des cellules T CD4 spécifiques de la grippe s’accumulaient dans le tissu pulmonaire, où elles ont persisté pendant au moins un mois. Ce schéma correspond à un modèle selon lequel le vaccin élargit d’abord les effecteurs spécifiques à la grippe dans le ganglion, puis redirige un sous-ensemble sélectionné pour s’installer dans les voies aériennes en tant que sentinelles prêtes pour la prochaine infection.
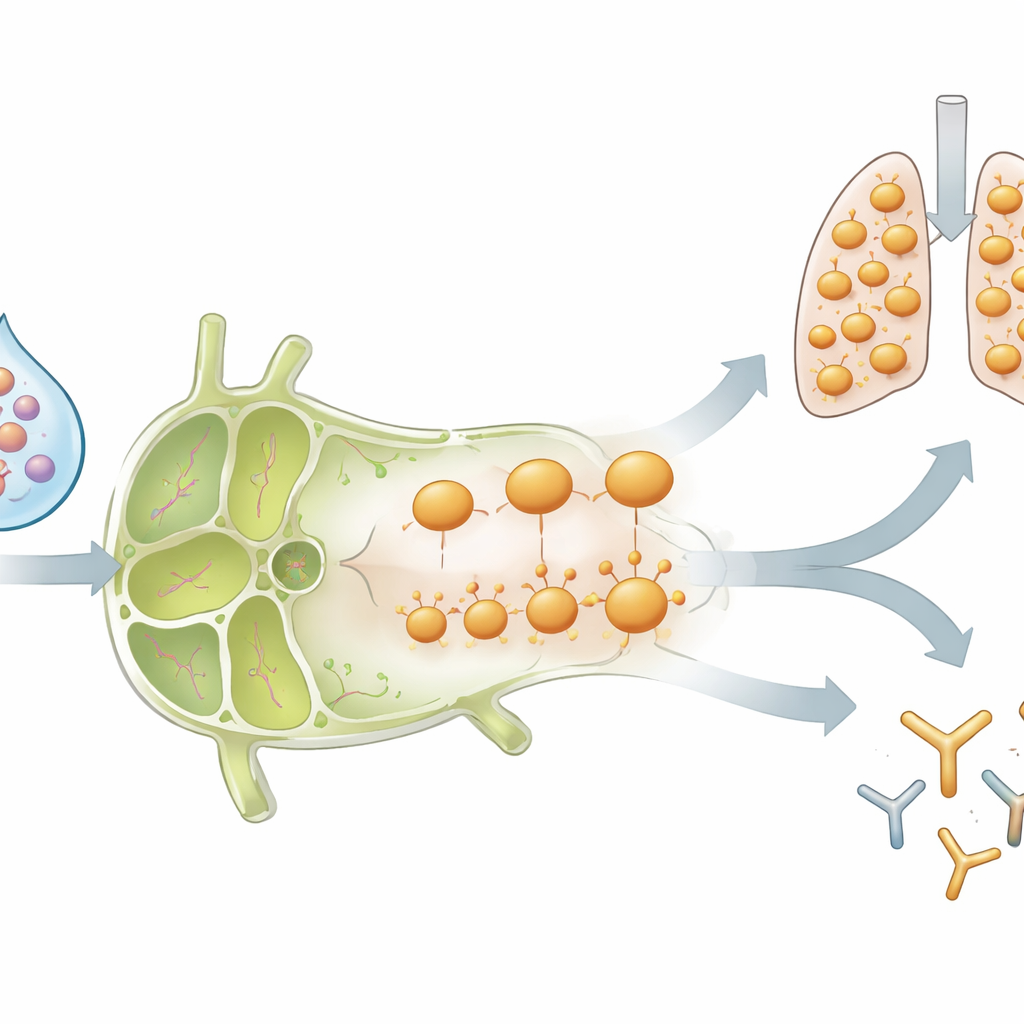
La mémoire modifie tout le « voisinage » vaccinal
Un test important était de savoir si ces effets se limitaient à la souche virale exacte utilisée pour l’infection initiale. Flublok contient plusieurs types de protéines de la grippe, y compris une (H3) pour laquelle les souris infectées n’avaient aucune mémoire T préalable. De manière surprenante, les nouvelles cellules T CD4 spécifiques à H3, amorcées chez les souris ayant déjà été infectées, se sont comportées de façon très similaire aux cellules renforcées qui reconnaissaient la souche B d’origine : elles se sont multipliées rapidement, ont produit de forts signaux antiviraux, ont activé des récepteurs de chimiokines, puis ont décliné dans le ganglion lymphatique au fur et à mesure que des cellules apparaissaient dans le poumon. Les taux d’anticorps dirigés contre les anciennes et nouvelles protéines virales étaient également plus élevés chez les animaux ayant une expérience d’infection. Cela suggère qu’une infection antérieure reconfigure le « climat » à l’intérieur du ganglion drainant—via des molécules inflammatoires et des cellules immunitaires recrutées—de sorte que tout nouvel antigène vaccinal entrant dans cet espace soit traité différemment.
Ce que cela signifie pour une meilleure protection contre la grippe
Pour un public non spécialiste, le message clé est que l’histoire immunitaire vis‑à‑vis de la grippe peut être transformée d’une complication en un atout. Dans ce modèle murin, un vaccin protéique associé à un adjuvant nanoparticulaire lipidique a fait plus que rehausser les anticorps : chez les animaux ayant eu une infection antérieure, il a rapidement généré de solides cellules T auxiliaires qui ont appris à migrer vers le poumon et a renforcé les anticorps même contre des composants grippaux non apparentés. Ce travail ouvre la voie à des vaccins antigrippaux futurs conçus non seulement pour courir après la dernière variante virale, mais pour exploiter la mémoire immunitaire existante et implanter délibérément des cellules défensives de longue durée dans les voies aériennes, où elles pourraient offrir une protection plus large et plus durable contre des virus respiratoires en constante évolution.
Citation: White, C.L., Mengu, L., Sidhu, I.S. et al. Re-shaping the immune response to influenza vaccination in a host with immune memory from influenza infection. npj Vaccines 11, 73 (2026). https://doi.org/10.1038/s41541-026-01397-w
Mots-clés: vaccination contre la grippe, mémoire immunitaire, cellules T CD4, adjuvants vaccinaux, immunité pulmonaire