Clear Sky Science · ar
إعادة تشكيل الاستجابة المناعية للقاح الإنفلونزا في مضيف لديه ذاكرة من عدوى الإنفلونزا
لماذا تهم العدوى السابقة بالإنفلونزا اللقطات المستقبلية
معظم الناس يصابون بالإنفلونزا لأول مرة قبل أن يتلقوا لقاح الإنفلونزا للكبار. تطرح هذه الدراسة سؤالاً بسيطاً لكنه مهمّاً: كيف تغيّر ذاكرة العدوى المبكرة طريقة استجابة أجسامنا للقاحات اللاحقة؟ باستخدام نموذج فئران مصمم ليحاكي تجربة الإنسان، يظهر الباحثون أن عدوى الإنفلونزا السابقة يمكن أن تحول لقاح إنفلونزا بروتيني اعتيادي من معزز للأجسام المضادة إلى مُحرّك لخلايا T قوية مقاومة للفيروس تتوجه إلى الرئتين، حيث تكون الحماية أكثر حاجة.
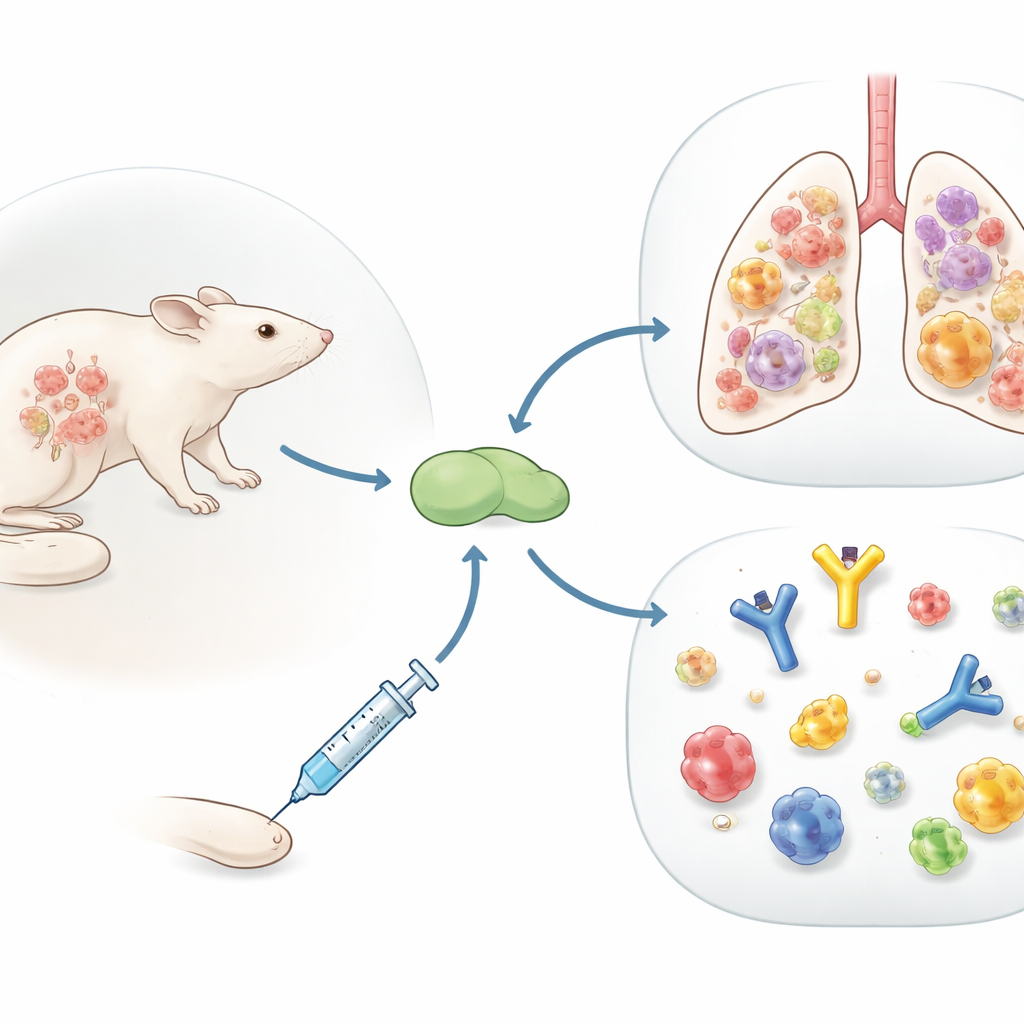
النظر أبعد من الأجسام المضادة
لقاحات الإنفلونزا الحالية مصممة أساساً لرفع مستوى الأجسام المضادة ضد غلاف الفيروس الخارجي، وهذا ينجح حتى يتحوّر الفيروس. ركز الفريق بدلاً من ذلك على خلايا CD4 T، فئة من خلايا الدم البيضاء التي تساعد خلايا مناعية أخرى ويمكنها التعرف على أجزاء من الفيروس تتغير بدرجة أقل مع مرور الزمن. درسوا Flublok، لقاح إنفلونزا مرخّص يتألف فقط من بروتينات فيروسية منظَّفة، ومعه واحد من مكونين منشّطين للجهاز المناعي: مزيج زيتي في الماء شبيه بـMF59، وجسيم دهني موجب الشحنة أحدث يُدعى R-DOTAP. في الفئران التي لم تُعرَض للإنفلونزا من قبل، حفّز كلا المكوّنَين خلايا CD4 T، لكن R-DOTAP أنتج عدداً أكبر بكثير من الخلايا وبمزيج أوسع من الإشارات المضادة للفيروس.
ما الذي يتغير بعد المواجهة الأولى مع الإنفلونزا
بعد ذلك أعطى الباحثون الفئران عدوى إنفلونزا من نوع B، وانتظروا حتى وقت طويل بعد التعافي، ثم لقّحوها. الآن بدت الاستجابة مختلفة جداً. اشتعلت خلايا CD4 T في العقد اللمفاوية المصرفة لِمَوقع الحقن بسرعة، ووصلت ذروتها حول اليوم السادس بدلاً من اليوم التاسع. مع R-DOTAP، كان عدد خلايا CD4 T الخاصة بالإنفلونزا في هذه العقد أعلى بأكثر من عشرة أضعاف مقارنة بالحيوانات المبتدئة. وعلى نحو ملفت أيضاً، تغيّرت «طبيعة» هذه الخلايا: بدلاً من تفضيل الإشارات التي تدعم إنتاج الأجسام المضادة بشكل رئيسي، بدأت الخلايا تفرز إشارات مضادة للفيروس قوية (TNF-alpha وinterferon-gamma) المرتبطة بالسيطرة المباشرة على الفيروس وبمساعدة خلايا القاتلة.
الهجرة الموجهة نحو الرئتين
لماذا تقلّ سرعة الخلايا في العقد اللمفاوية بسرعة بعد بلوغ الذروة؟ وجد الفريق أنه في الفئران التي لديها خبرة عدوى سابقة، كثير من خلايا CD4 T المحفّزة باللقاح شغّلت مستقبلات كيموكين—جزيئات سطحية تعمل كـGPS للتحرك داخل الجسم—وخاصة CCR5 وCXCR3. هذه العلامات معروفة بتوجيه الخلايا إلى أنسجة مُلتهبة مثل الرئة. مع مرور الوقت، اختفت الخلايا التي تحمل هذه المستقبلات من العقد اللمفاوية، بينما تراكمت خلايا CD4 T الخاصة بالإنفلونزا داخل نسيج الرئة، حيث استمرت لمدى لا يقل عن شهر. يتوافق هذا النمط مع نموذجٍ يفيد بأن اللقاح أولاً يوسع مجتمعات المساعدين الخاصة بالإنفلونزا في العقدة، ثم يعيد توجيه جزء مُنتقى منها ليستقر في المسالك الهوائية كحُرّاس جاهزين للعدوى التالية.
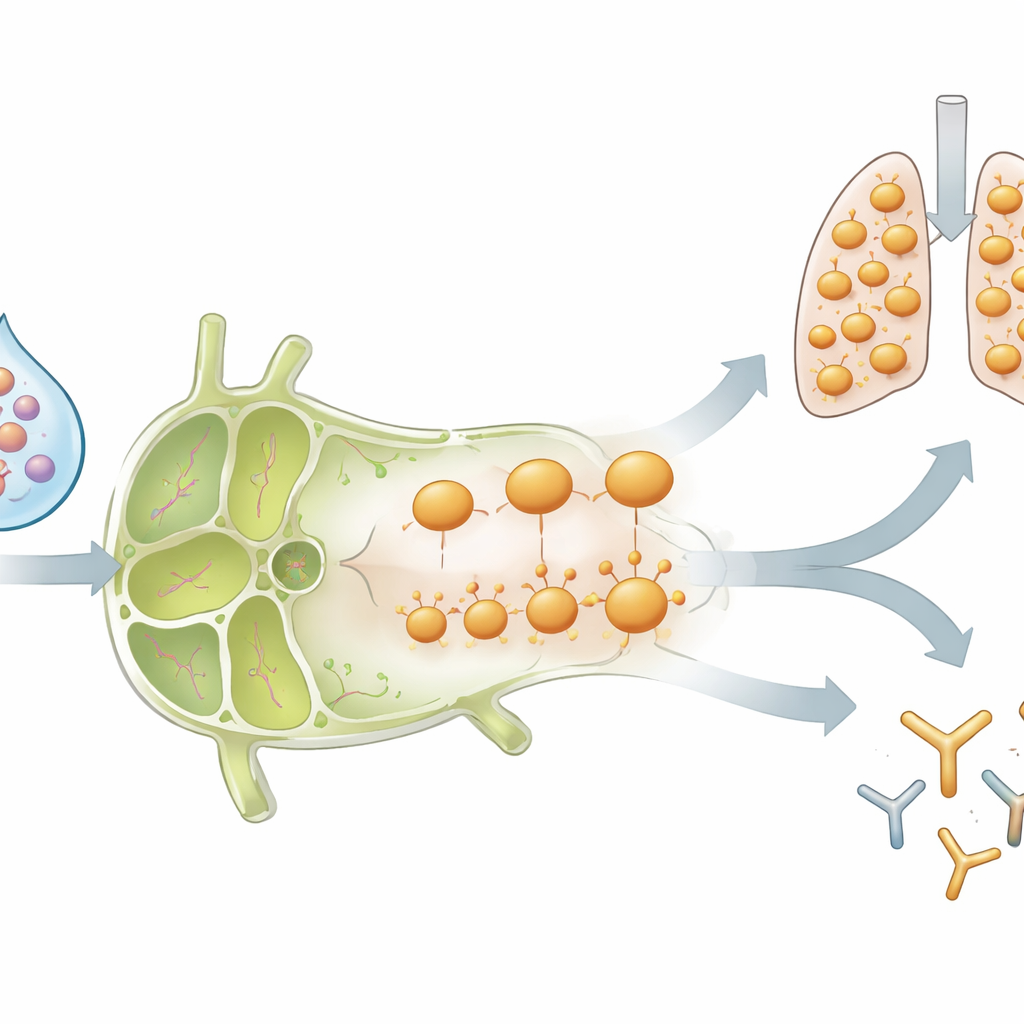
الذاكرة تغيّر الحي بأكمله حول موقع اللقاح
كان اختبارٌ مهماً هل تقتصر هذه التأثيرات على السلالة الفيروسية نفسها المستخدمة في العدوى الأولية أم لا. يحتوي Flublok على عدة أنواع من البروتينات الفيروسية، بما في ذلك واحد (H3) لم يكن لدى الفئران مصابة به ذاكرة خلوية سابقة. بشكل مفاجئ، تصرفت خلايا CD4 T الجديدة المكوّنة ضد H3 في الفئران التي سبق أن أصيبت بطريقة مشابهة تماماً للخلايا المعزَّزة التي تعرف السلالة الأصلية من إنفلونزا B: توسعت بسرعة، وأنتجت إشارات مضادة للفيروس قوية، وشغّلت مستقبلات الكيموكين، ثم انخفضت في العقد اللمفاوية بينما ظهرت خلايا في الرئة. كما كانت مستويات الأجسام المضادة ضد كل من البروتينات الفيروسية القديمة والجديدة أعلى أيضاً في الحيوانات ذات الخبرة العدوانية. وهذا يوحي بأن العدوى السابقة تعيد تشكيل «المناخ» داخل العقدة اللمفاوية المصرفة—من خلال جزيئات التهابية وخلايا مناعية مُسْتدعاة—بحيث يتم التعامل مع أي مستضد لقاح جديد يدخل تلك المساحة بشكل مختلف.
ماذا يعني هذا لحماية أفضل من الإنفلونزا
للغير متخصصين، الرسالة الأساسية هي أن تاريخ الجسم مع الإنفلونزا يمكن أن يتحول من تعقيد إلى ميزة. في هذا النموذج الفأري، لم يقتصر أثر لقاح بروتيني مصحوب بمحفّز نانوي دهني على زيادة الأجسام المضادة فحسب: في الحيوانات التي لديها عدوى إنفلونزا سابقة، أنتج بسرعة خلايا مساعدَة قوية من نوع T تعلمت الاستقرار في الرئة وعزّزت الأجسام المضادة حتى ضد مكونات إنفلونزا غير مرتبطة. وتشير هذه العمل إلى لقاحات إنفلونزا مستقبلية مصممة ليس فقط لملاحقة البديل الفيروسي الأحدث، بل لاستغلال الذاكرة المناعية الحالية وزرع خلايا دفاعية طويلة الأمد في الممرات الهوائية عمدًا، حيث قد توفر حماية أوسع وأكثر دواماً ضد الفيروسات التنفسية المتغيرة باستمرار.
الاستشهاد: White, C.L., Mengu, L., Sidhu, I.S. et al. Re-shaping the immune response to influenza vaccination in a host with immune memory from influenza infection. npj Vaccines 11, 73 (2026). https://doi.org/10.1038/s41541-026-01397-w
الكلمات المفتاحية: تطعيم الإنفلونزا, الذاكرة المناعية, خلايا CD4 T, مضافات اللقاح, المناعة الرئوية