Clear Sky Science · zh
体内单细胞RNA代谢标记解析再生斑马鱼心脏的早期转录反应者
为何修复受损心脏如此艰难
当人发生心肌梗死时,受损的心肌通常被不可收缩的瘢痕组织所替代,使心脏永久变弱。然而某些动物,如斑马鱼,能够在受伤后重新生长出健康的心肌。本文探讨科学家如何开始在体内以实时、逐细胞的方式观察斑马鱼心脏受损后最早被启动的基因开关——以及调节早期免疫反应如何改变愈合进程。
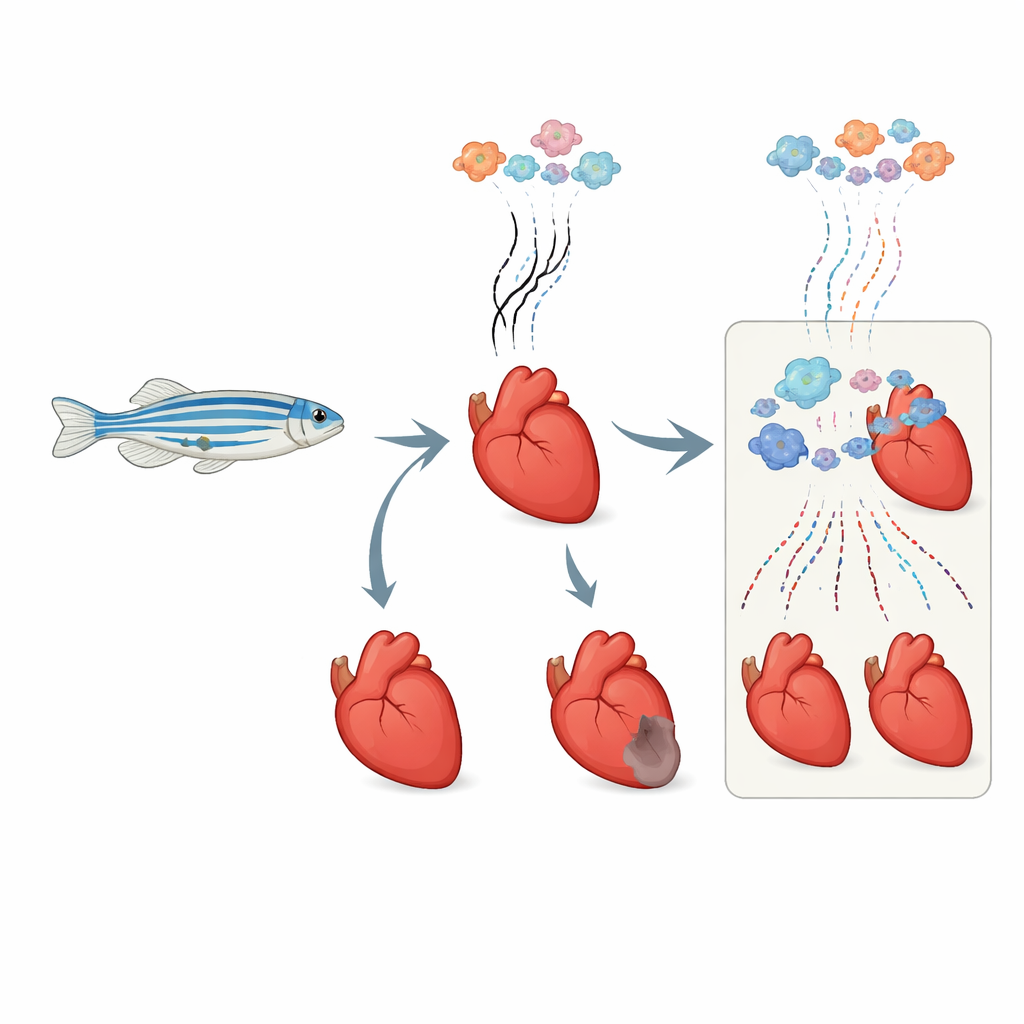
观察新鲜基因信息的出现
心脏中的每个细胞不断开启和关闭基因,产生寿命短暂的RNA信息,告诉细胞该如何行动。传统方法对全部RNA进行总体测序,会把旧的和新的信号混在一起。研究人员将一种化学“时间戳”方法——RNA代谢标记——改造为可在成年斑马鱼体内使用。他们注入了一种无害的构件,该构件只会被掺入新合成的RNA。随后,特定化学处理将这些新掺入的部分转变为在RNA测序时可见的独特特征。将此方法与单细胞分析结合,他们能够在每个单独心脏细胞中区分哪些基因信息是在受伤前已有、哪些是在受伤后新合成的。
聚焦损伤后最初数小时
研究团队聚焦于在冷冻并损伤斑马鱼心脏一部分后至关重要的最初六小时,这一操作模拟了心肌梗死。由于许多寿命较长的RNA分子在损伤前已存在,仅测量总RNA会模糊早期变化。通过标记方法,科学家逐细胞比较受伤心脏中新合成的RNA与假手术对照组的差异。这使他们能够检测到那些短暂且微弱的基因活性激增,否则这些信号会被旧信息或个体间差异淹没。
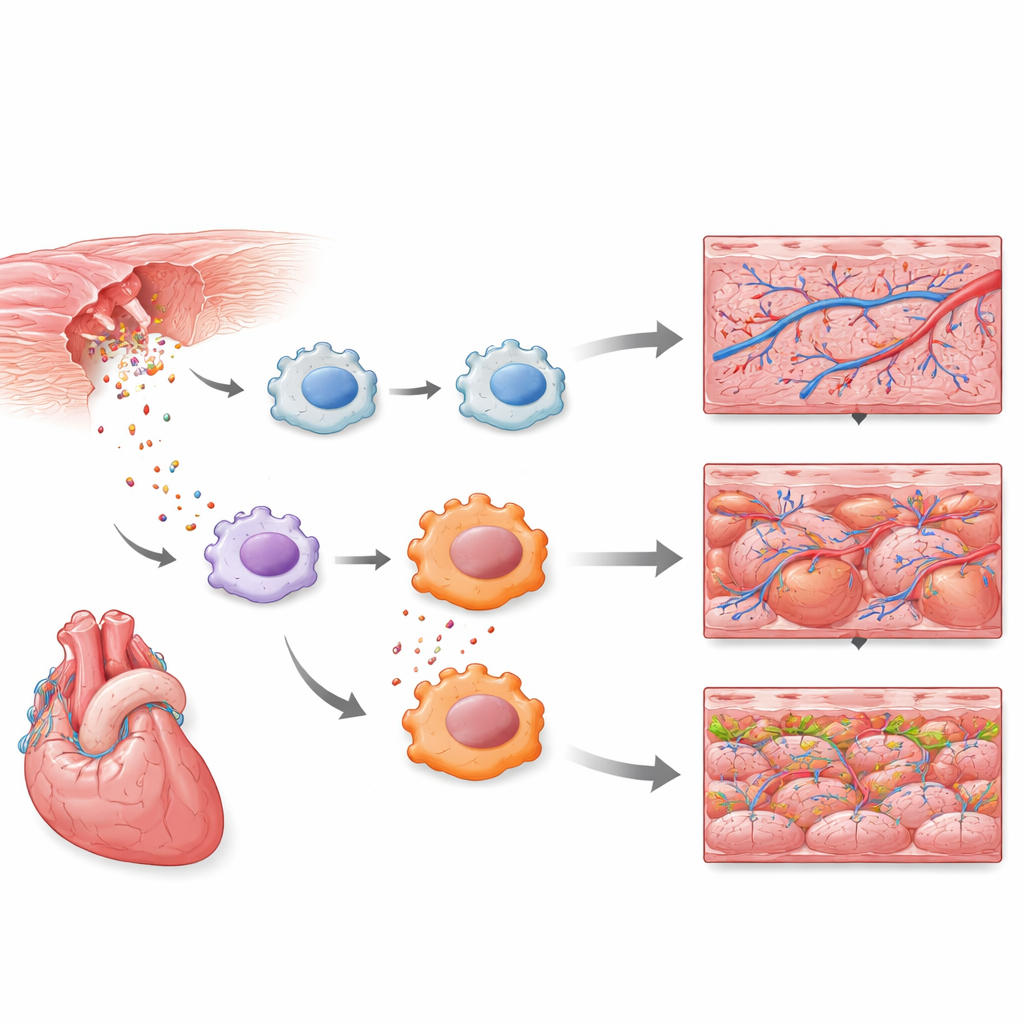
早期免疫细胞走到聚光灯下
单细胞测量显示,一类类似巨噬细胞的免疫细胞是最早的反应者之一。数小时内,这些细胞启动了先天防御程序,包括Toll样受体信号传导——一种已知的感知危险和感染的警报通路。一个涵盖多日再生过程的更大参考图谱证实,中性粒细胞(另一类白细胞)也在早期做出强烈反应。综合来看,这些结果表明,心脏修复的第一波并非仅由肌肉或血管等结构细胞驱动,而是在特定免疫细胞类型中发生的一次精确定时的炎症活动突发所引导。
微调炎症以促进修复
炎症是一把双刃剑:过少会延缓对坏死组织的清理,而过多或持续过久则会造成额外损伤和瘢痕。根据他们的单细胞数据,研究人员测试了在巨噬细胞中选择性降低一个关键免疫信号会发生什么。他们构建了这样一种斑马鱼:在经处理后,只有巨噬细胞内可被激活表达一种MyD88的显性负变体——MyD88是Toll样受体通路中的关键中继。当这道刹车被启动时,损伤部位积聚的强烈炎性巨噬细胞减少了。值得注意的是,这些鱼的受损心脏在早期显示出更快的再生迹象:创缘周围冠状血管生长更多、心肌细胞的分裂增加,而其他愈合步骤并未明显受损。
对未来心脏修复的意义
这项工作表明,现在可以在体内以小时级别和单细胞分辨率观察到对心脏损伤响应中哪些基因被激活。研究强调,先天免疫细胞的早期激活并非简单的开关式事件,而是一个可以调节的过程,其强度和时机能够加快或减缓再生。尽管斑马鱼心脏的再生能力远强于人类心脏,但这一原理可能具有普适性:细致调整特定的免疫信号——而非完全阻断炎症——有朝一日或能帮助诱导受损的哺乳动物心脏实现更好的恢复。
引用: Mintcheva, J., Tseng, TL., Goumenaki, P. et al. In vivo single-cell RNA metabolic labeling resolves early transcriptional responders in the regenerating zebrafish heart. Nat Commun 17, 4073 (2026). https://doi.org/10.1038/s41467-026-72781-2
关键词: 心脏再生, 斑马鱼, 单细胞RNA, 免疫反应, Toll样受体信号传导