Clear Sky Science · it
La marcatura metabolica dell’RNA in vivo a singola cellula risolve i primi rispondenti trascrizionali nel cuore di zebrafish in rigenerazione
Perché riparare un cuore rotto è così difficile
Quando una persona subisce un infarto, il muscolo danneggiato viene solitamente sostituito da tessuto cicatriziale che non si contrae, lasciando il cuore permanentemente indebolito. Tuttavia alcuni animali, come il zebrafish, possono ricrescere tessuto cardiaco sano dopo una lesione. Questo articolo esplora come gli scienziati hanno cominciato a osservare, in tempo reale e cellula per cellula, i primissimi interruttori genetici che si attivano nel cuore del zebrafish dopo il danno—e come modulare una reazione immunitaria precoce possa cambiare l’esito della guarigione.
Osservare i messaggi genetici freschi mentre compaiono
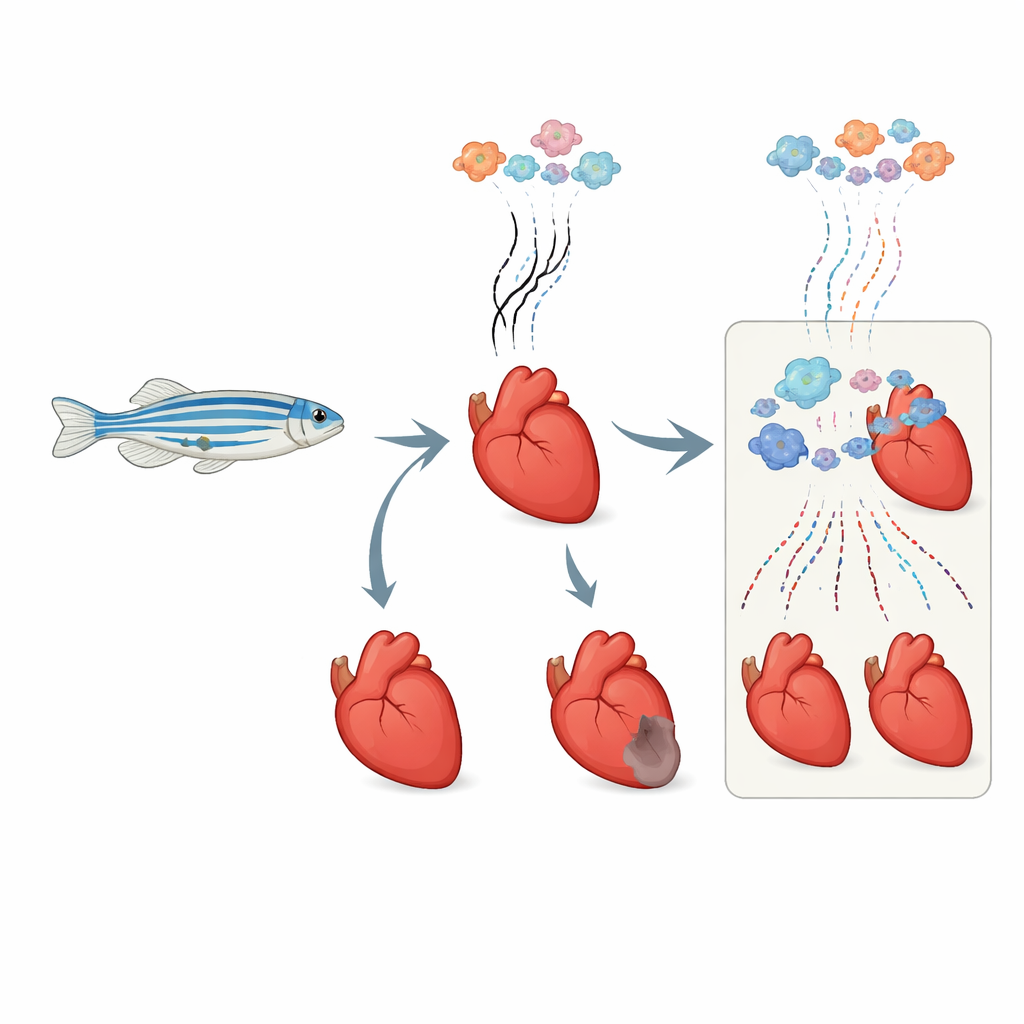
Ogni cellula del cuore accende e spegne costantemente geni, producendo messaggi RNA di vita breve che dicono alla cellula cosa fare. I metodi tradizionali leggono tutto l’RNA in massa, mescolando segnali vecchi e nuovi. I ricercatori hanno adattato un metodo chimico “timestamp”, chiamato marcatura metabolica dell’RNA, per l’uso in zebrafish adulti vivi. Hanno iniettato un blocco da costruzione innocuo che viene incorporato solo negli RNA appena sintetizzati. Successivamente, un trattamento chimico specifico trasforma quegli elementi nuovi in una forma che appare come una firma distinta quando l’RNA viene sequenziato. Combinando questo con l’analisi a singola cellula, hanno potuto separare, in ciascuna cellula cardiaca individuale, quali messaggi genici erano presenti prima della lesione e quali erano stati appena prodotti dopo.
Avvicinarsi alle prime ore dopo il danno
Il gruppo si è concentrato sulle prime sei ore cruciali dopo il congelamento e il danneggiamento di una porzione del cuore del zebrafish, una procedura che imita un infarto. Poiché molte molecole di RNA a lunga durata erano già presenti prima della lesione, misurare semplicemente l’RNA totale avrebbe offuscato i cambiamenti precoci. Con il loro approccio di marcatura, gli scienziati hanno confrontato l’RNA appena prodotto nei cuori danneggiati con quello nei controlli sham-operati, cellula per cellula. Ciò ha permesso loro di rilevare anche esplosioni sottili e di breve durata dell’attività genica che altrimenti sarebbero state sommerse dai messaggi più vecchi o dalle differenze tra singoli animali.
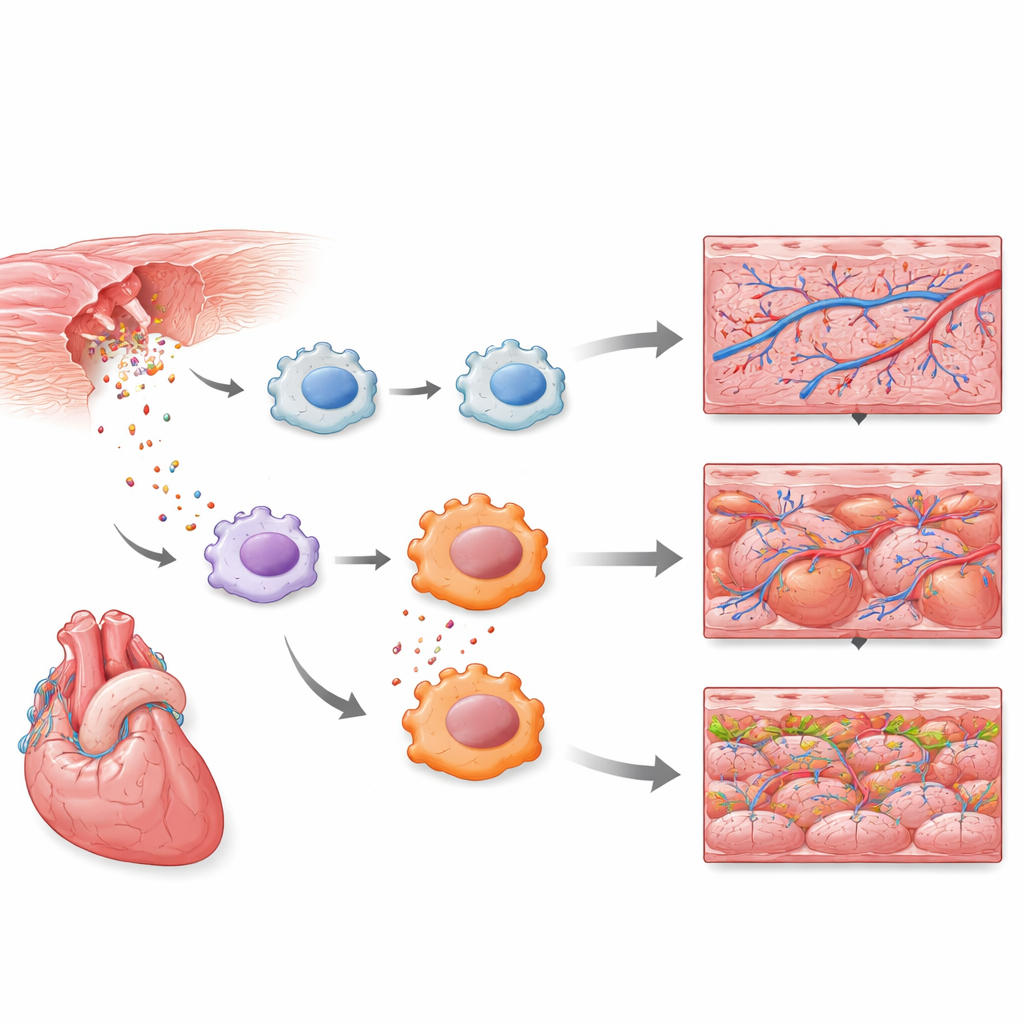
Le prime cellule immunitarie al centro della scena
Le misure a singola cellula hanno rivelato che una sottopopolazione di cellule immunitarie simili a macrofagi è stata tra le primissime a rispondere. Nel giro di poche ore, queste cellule hanno attivato programmi di difesa innata, inclusa la segnalazione dei recettori Toll-like, una via di allarme ben nota che rileva pericolo e infezione. Una mappa di riferimento più ampia delle cellule cardiache lungo molti giorni di rigenerazione ha confermato che anche i neutrofili, un altro tipo di globulo bianco, montano una forte risposta precoce. Nel complesso, questi risultati mostrano che la prima ondata di riparazione cardiaca è guidata non solo da cellule strutturali come muscolo e vasi sanguigni, ma da un’esplosione di attività infiammatoria precisamente temporizzata in tipi specifici di cellule immunitarie.
Affinare l’infiammazione per favorire la riparazione
L’infiammazione è una spada a doppio taglio: troppo poca può ritardare la rimozione del tessuto morto, mentre troppa o troppo prolungata può provocare danni aggiuntivi e cicatrizzazione. Guidati dai dati a singola cellula, i ricercatori hanno testato cosa succede se attenuano selettivamente un segnale immunitario chiave nei macrofagi. Hanno creato zebrafish in cui una versione dominante-negativa di MyD88—un relè essenziale nelle vie dei recettori Toll-like—poteva essere attivata solo nei macrofagi dopo il trattamento. Quando questo freno è stato inserito, si è osservata una minore accumulazione di macrofagi fortemente infiammatori nel sito della lesione. Colpisce che i cuori danneggiati in questi pesci abbiano mostrato segnali precoci di rigenerazione più rapidi: maggiore crescita dei vasi coronarici intorno alla ferita e aumento della divisione delle cellule muscolari cardiache, senza evidenti danni ad altri stadi della guarigione.
Cosa significa per le future terapie cardiache
Questo lavoro dimostra che è ormai possibile osservare, nel giro di ore e con risoluzione a singola cellula, quali geni si attivano in risposta al danno cardiaco in un animale vivo. I risultati sottolineano che l’attivazione precoce delle cellule immunitarie innate non è semplicemente un fenomeno tutto-o-nulla, ma un processo modulabile la cui intensità e tempistica possono accelerare o rallentare la rigenerazione. Sebbene i cuori dei zebrafish siano molto più rigenerativi di quelli umani, il principio potrebbe essere trasferibile: regolare con attenzione segnali immunitari specifici—piuttosto che bloccare l’infiammazione in modo indiscriminato—potrebbe un giorno aiutare a indirizzare i cuori dei mammiferi feriti verso una migliore ripresa.
Citazione: Mintcheva, J., Tseng, TL., Goumenaki, P. et al. In vivo single-cell RNA metabolic labeling resolves early transcriptional responders in the regenerating zebrafish heart. Nat Commun 17, 4073 (2026). https://doi.org/10.1038/s41467-026-72781-2
Parole chiave: rigenerazione cardiaca, zebrafish, RNA a singola cellula, risposta immunitaria, segnalazione dei recettori Toll-like