Clear Sky Science · es
Etiquetado metabólico de ARN monocelular in vivo resuelve los primeros respondedores transcripcionales en el corazón regenerante del pez cebra
Por qué reparar un corazón roto es tan difícil
Cuando una persona sufre un infarto, el músculo dañado suele ser reemplazado por tejido cicatricial que no puede latir, dejando el corazón debilitado de forma permanente. Sin embargo, algunos animales, como el pez cebra, pueden regenerar músculo cardíaco sano tras una lesión. Este artículo explora cómo los científicos están empezando a observar, en tiempo real y célula a célula, los primeros interruptores genéticos que se activan en un corazón de pez cebra después del daño —y cómo ajustar una reacción inmune temprana puede cambiar el curso de la curación.
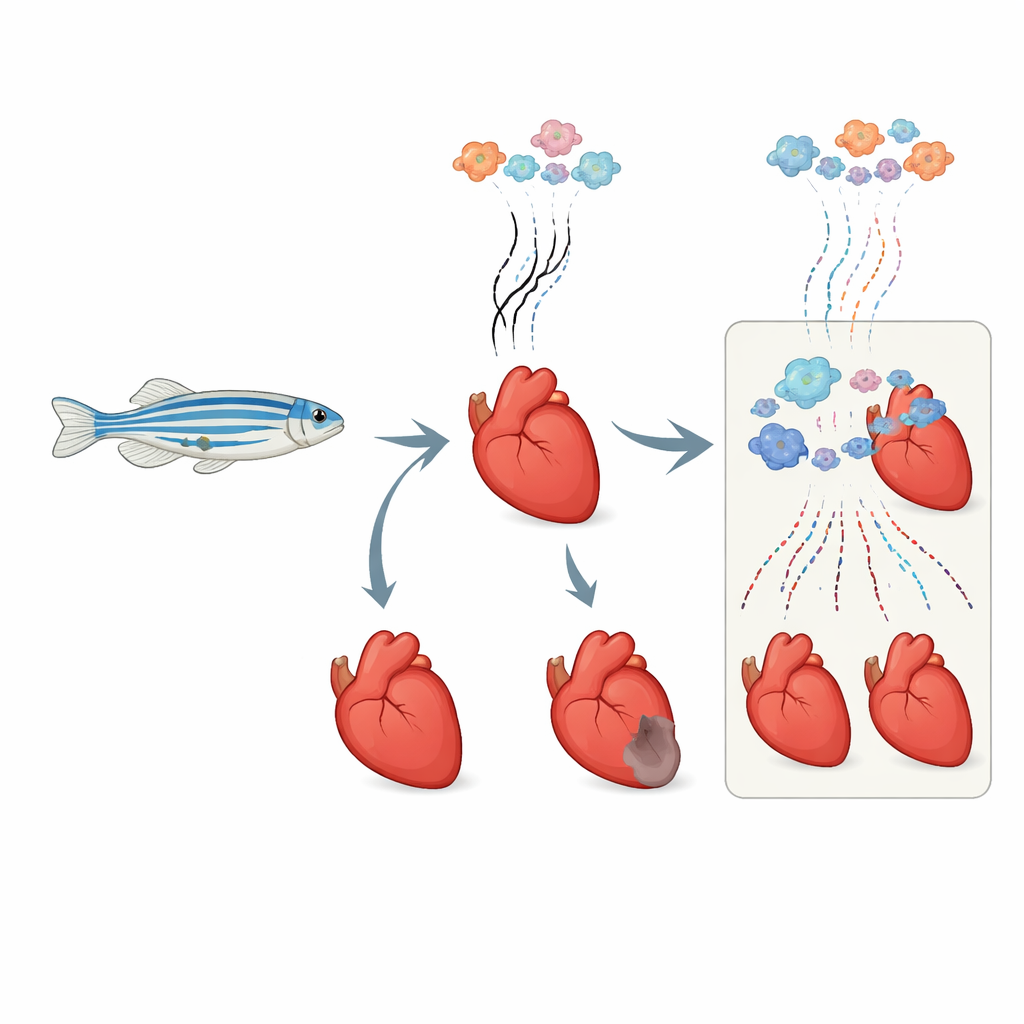
Observando los mensajes genéticos recién producidos
Cada célula del corazón enciende y apaga genes constantemente, produciendo mensajes de ARN de corta vida que indican qué debe hacer la célula. Los métodos tradicionales leen todo el ARN en conjunto, mezclando señales antiguas y nuevas. Los investigadores adaptaron un método químico de “marcador temporal”, llamado etiquetado metabólico de ARN, para su uso en peces cebra adultos vivos. Inyectaron un componente inocuo que se incorpora solo en el ARN recién sintetizado. Más tarde, un tratamiento químico específico convierte esas piezas nuevas en una forma que aparece como una firma distinta cuando se secuencia el ARN. Al combinar esto con análisis unicelular, pudieron separar, en cada célula cardíaca individual, qué mensajes génicos estaban presentes antes de la lesión y cuáles se habían producido recientemente después.
Acercándose a las primeras horas tras el daño
El equipo se centró en las cruciales primeras seis horas después de congelar y dañar una porción del corazón del pez cebra, un procedimiento que emula un infarto. Debido a que muchas moléculas de ARN de larga vida ya estaban presentes antes de la lesión, medir solo el ARN total difuminaría los cambios tempranos. Con su enfoque de marcado, los científicos compararon el ARN recién sintetizado en corazones lesionados con el de controles simulados, célula por célula. Esto les permitió detectar incluso estallidos sutiles y efímeros de actividad génica que de otro modo se perderían entre mensajes más antiguos o entre diferencias entre animales individuales.
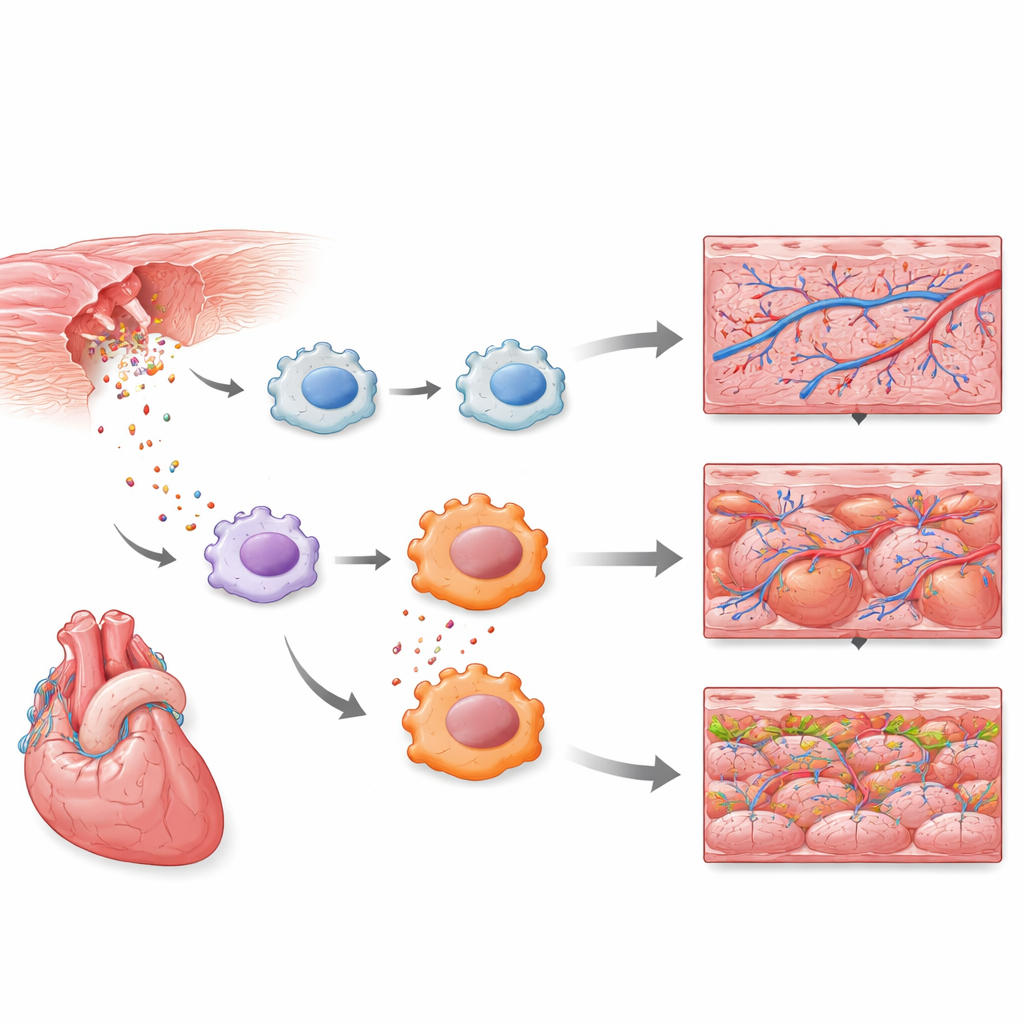
Las células inmunes tempranas toman el protagonismo
Las medidas unicelulares revelaron que un subconjunto de células inmunes semejantes a macrófagos se encontraban entre los respondedores más tempranos. En cuestión de horas, estas células activaron programas de defensa innata, incluida la señalización del receptor tipo Toll, una vía de alarma bien conocida que detecta peligro e infección. Un mapa de referencia más amplio de las células cardíacas a lo largo de varios días de regeneración confirmó que los neutrófilos, otro tipo de glóbulo blanco, también montan una respuesta temprana intensa. En conjunto, estos resultados muestran que la primera ola de reparación cardíaca no está impulsada solo por células estructurales como el músculo y los vasos sanguíneos, sino por un pulso inflamatorio cronometrado con precisión en tipos celulares inmunes específicos.
Afinar la inflamación para ayudar a la reparación
La inflamación es un arma de doble filo: muy poca puede retrasar la limpieza del tejido muerto, mientras que demasiada o prolongada puede causar daño adicional y cicatrización. Guiados por sus datos unicelulares, los investigadores probaron qué sucede si atenúan selectivamente una señal inmune clave en macrófagos. Crearon peces cebra en los que una versión dominante-negativa de MyD88 —un relé esencial en las vías de receptores tipo Toll— podía activarse solo en macrófagos tras un tratamiento. Cuando se activó este freno, se acumularon menos macrófagos fuertemente inflamatorios en el sitio de la lesión. De forma llamativa, los corazones dañados en estos peces mostraron marcadores tempranos de regeneración más rápidos: mayor crecimiento de vasos coronarios alrededor de la herida y aumento de la división de las células del músculo cardíaco, sin perjuicios evidentes en otros pasos de la curación.
Qué significa esto para la reparación cardíaca futura
Este trabajo demuestra que ahora es posible observar, en cuestión de horas y con resolución unicelular, qué genes se activan en respuesta al daño cardíaco en un animal vivo. Los hallazgos subrayan que la activación temprana de células inmunes innatas no es simplemente un fenómeno de todo o nada, sino un proceso modulable cuya intensidad y temporización pueden acelerar o ralentizar la regeneración. Aunque los corazones de pez cebra son mucho más regenerativos que los humanos, el principio puede ser aplicable: ajustar con cuidado señales inmunes específicas —en lugar de bloquear la inflamación por completo— podría algún día ayudar a inducir una mejor recuperación en corazones de mamíferos lesionados.
Cita: Mintcheva, J., Tseng, TL., Goumenaki, P. et al. In vivo single-cell RNA metabolic labeling resolves early transcriptional responders in the regenerating zebrafish heart. Nat Commun 17, 4073 (2026). https://doi.org/10.1038/s41467-026-72781-2
Palabras clave: regeneración cardíaca, pez cebra, ARN monocelular, respuesta inmune, señalización del receptor tipo Toll