Clear Sky Science · sv
In vivo enkelcells-RNA-metabolisk märkning avslöjar tidiga transkriptionella respondenter i den regenererande zebrafiskhjärtat
Varför det är så svårt att laga ett brustet hjärta
När en person får en hjärtinfarkt ersätts den skadade muskeln oftast av ärrvävnad som inte kan slå, vilket lämnar hjärtat permanent försvagat. Ändå kan vissa djur, som zebrafisk, återväxa frisk hjärtmuskel efter skada. Den här artikeln beskriver hur forskare börjar kunna följa, i realtid och cell för cell, de allra första genetiska strömbrytarna som slås på i ett zebrafiskhjärta efter skada — och hur man genom att justera en tidig immunreaktion kan ändra läkningsförloppet.
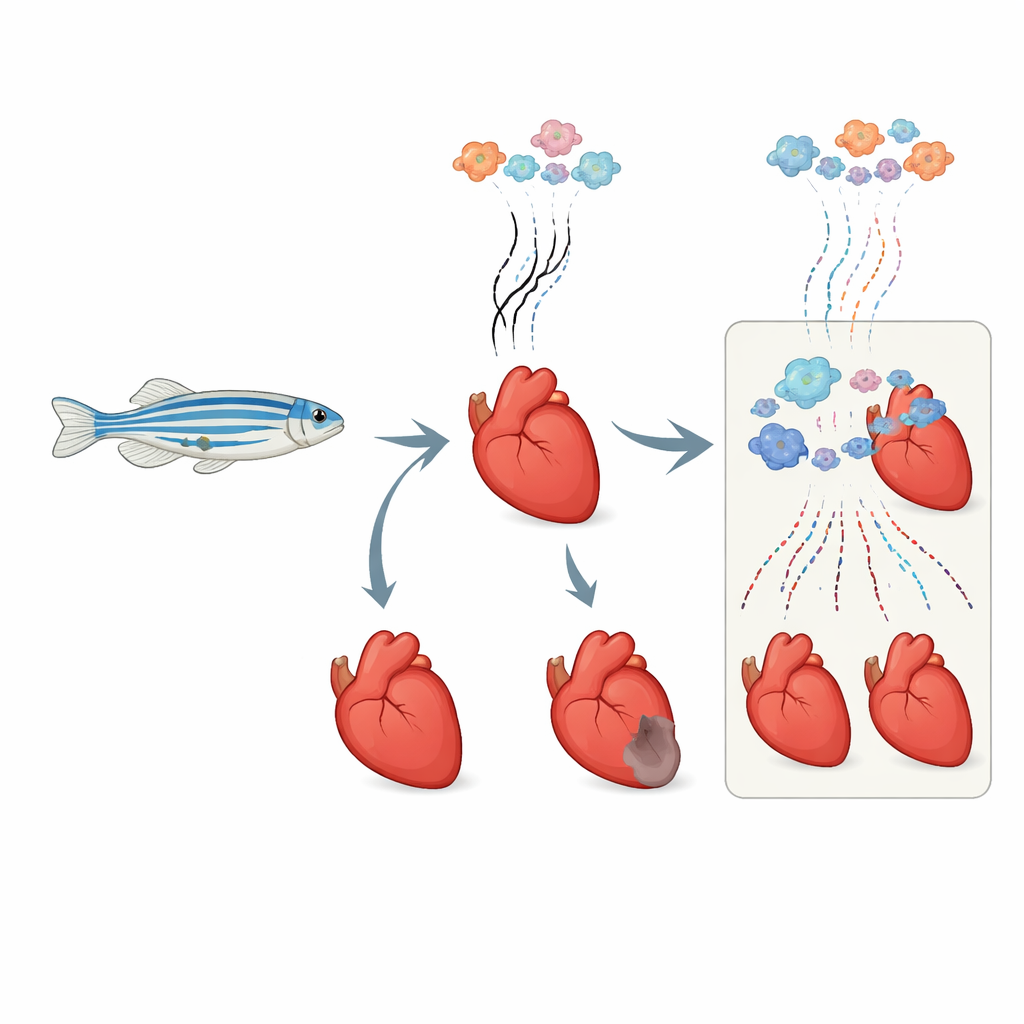
Att följa nya genetiska budskap när de uppstår
Varje cell i hjärtat slår ständigt på och av gener och producerar kortlivade RNA-meddelanden som talar om för cellen vad den ska göra. Traditionella metoder läser av all RNA i bulk och blandar gamla och nya signaler. Forskarna anpassade en kemisk “tidsstämpel”-metod, kallad RNA-metabolisk märkning, för användning i levande vuxna zebrafiskar. De injicerade en ofarlig byggsten som bara införlivas i nyligen syntetiserat RNA. Senare omvandlar en specifik kemisk behandling dessa nya delar till en form som ger ett särskiljande signatur när RNA-sekvenseras. Genom att kombinera detta med enkelcellsanalys kunde de i varje enskild hjärtcell skilja mellan vilka genmeddelanden som fanns före skadan och vilka som nyligen skapats därefter.
Inzoomning på de första timmarna efter skada
Teamet fokuserade på de avgörande första sex timmarna efter att en del av zebrafiskhjärtat frusits och skadats, en procedur som efterliknar en hjärtinfarkt. Eftersom många långlivade RNA-molekyler redan fanns innan skadan skulle enbart mätning av total RNA sudda ut tidiga förändringar. Med sin märkningsteknik jämförde forskarna nyligen syntetiserat RNA i skadade hjärtan med sham-opererade kontroller, celltyp för celltyp. Detta gjorde det möjligt för dem att upptäcka även subtila och kortlivade utbrott av genaktivitet som annars skulle drunkna i äldre budskap eller i skillnader mellan enskilda djur.
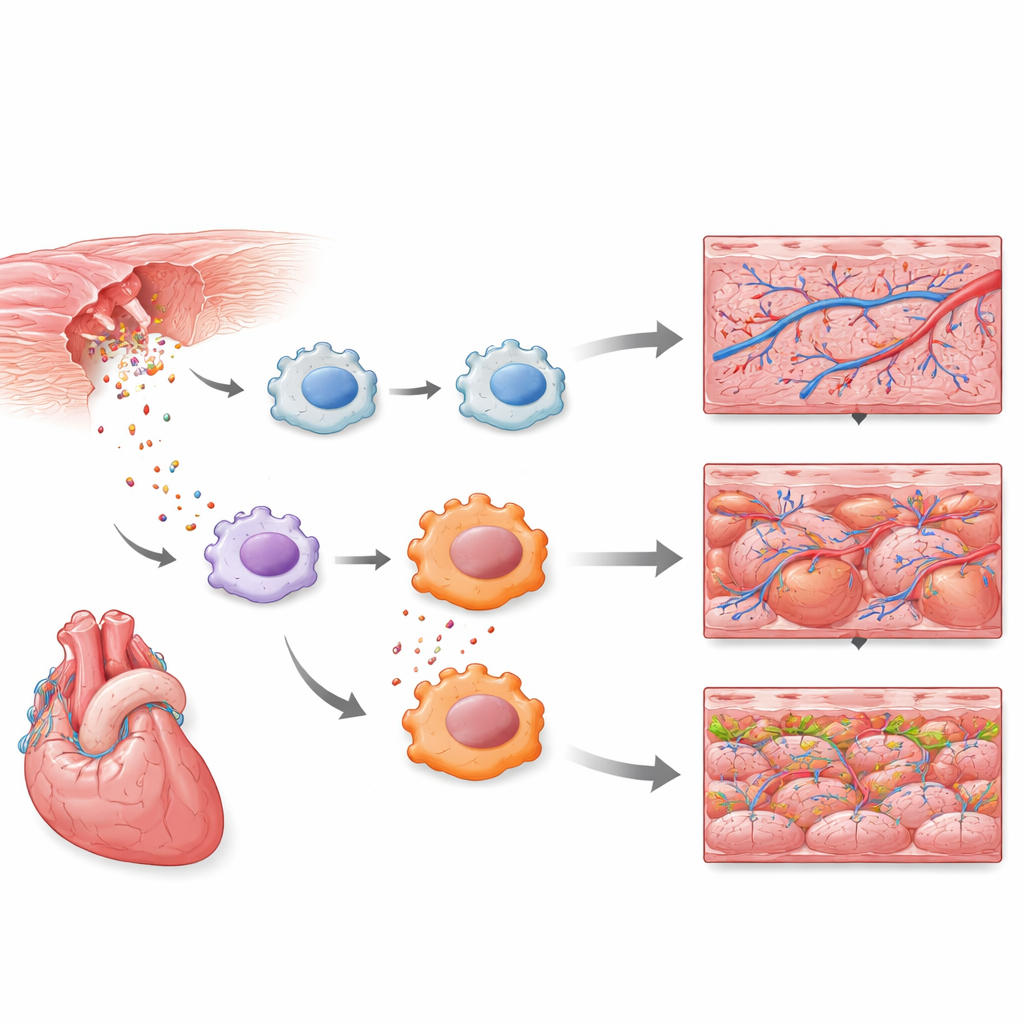
Tidiga immunceller träder in i strålkastarljuset
Mätningarna på enkelcellsnivå visade att en undergrupp av immunceller som liknar makrofager var bland de allra första respondenterna. Inom några timmar slog dessa celler på medfödda försvarsprogram, inklusive Toll-liknande receptorsignalering, en välkänd larmväg som känner av fara och infektion. En större referenskarta över hjärtceller under flera dagars regeneration bekräftade att neutrofiler, en annan typ av vita blodkroppar, också ger en stark tidig respons. Tillsammans visar resultaten att den första vågen av hjärtreparation styrs inte bara av strukturella celler som muskel och blodkärl, utan av en noggrant tidsbestämd inflammatorisk aktivitet i specifika immuncellstyper.
Finjustera inflammation för att underlätta reparation
Inflammation är ett tveeggat svärd: för lite kan fördröja bortstädningen av död vävnad, medan för mycket eller för långvarig inflammation kan orsaka extra skada och ärrbildning. Med ledning av sina enkelcellsdata testade forskarna vad som händer om de selektivt dämpar en nyckelsignal i makrofager. De skapade zebrafiskar där en dominant-negativ version av MyD88 — en viktig länk i Toll-liknande receptorvägar — kunde slås på endast i makrofager efter behandling. När denna broms aktiverades samlades färre starkt inflammatoriska makrofager vid skadestället. Anmärkningsvärt visade de skadade hjärtana hos dessa fiskar snabbare tidiga tecken på regeneration: mer tillväxt av kranskärl runt såret och ökad delning av hjärtmuskelceller, utan uppenbar skada på andra steg i läkningsprocessen.
Vad detta betyder för framtida hjärtreparation
Denna studie visar att det nu är möjligt att övervaka, inom timmar och med enkelcellsupplösning, vilka gener som slås på som svar på hjärtskada i ett levande djur. Resultaten understryker att tidig aktivering av medfödda immunceller inte är ett enkelt av-eller på-fenomen, utan en ställbar process vars styrka och timing kan påskynda eller bromsa regeneration. Även om zebrafiskhjärtan är långt mer regenerativa än människohjärtan kan principen vara överförbar: att noggrant justera specifika immunsignaler — snarare än att helt blockera inflammation — skulle en dag kunna hjälpa till att få skadade däggdjurs hjärtan att återhämta sig bättre.
Citering: Mintcheva, J., Tseng, TL., Goumenaki, P. et al. In vivo single-cell RNA metabolic labeling resolves early transcriptional responders in the regenerating zebrafish heart. Nat Commun 17, 4073 (2026). https://doi.org/10.1038/s41467-026-72781-2
Nyckelord: hjärtmuskelregeneration, zebrafisk, enkelcells-RNA, immunsvar, Toll-liknande receptor-signalering