Clear Sky Science · nl
In vivo enkelcel RNA-metabole labeling brengt vroege transcriptionele responders in het regenererende zebravis‑hart in kaart
Waarom het zo moeilijk is een gebroken hart te herstellen
Bij een hartaanval wordt het beschadigde spierweefsel meestal vervangen door littekenweefsel dat niet kan samentrekken, waardoor het hart blijvend verzwakt raakt. Sommige dieren, zoals zebravissen, kunnen echter gezond hartspierweefsel opnieuw opbouwen na schade. Dit artikel onderzoekt hoe wetenschappers beginnen te observeren, in realtime en cel voor cel, welke eerste genetische schakelaars in een zebravishart na beschadiging omslaan — en hoe het bijstellen van een vroege immuunreactie het verloop van het herstel kan veranderen.
Verse genetische boodschappen zien verschijnen
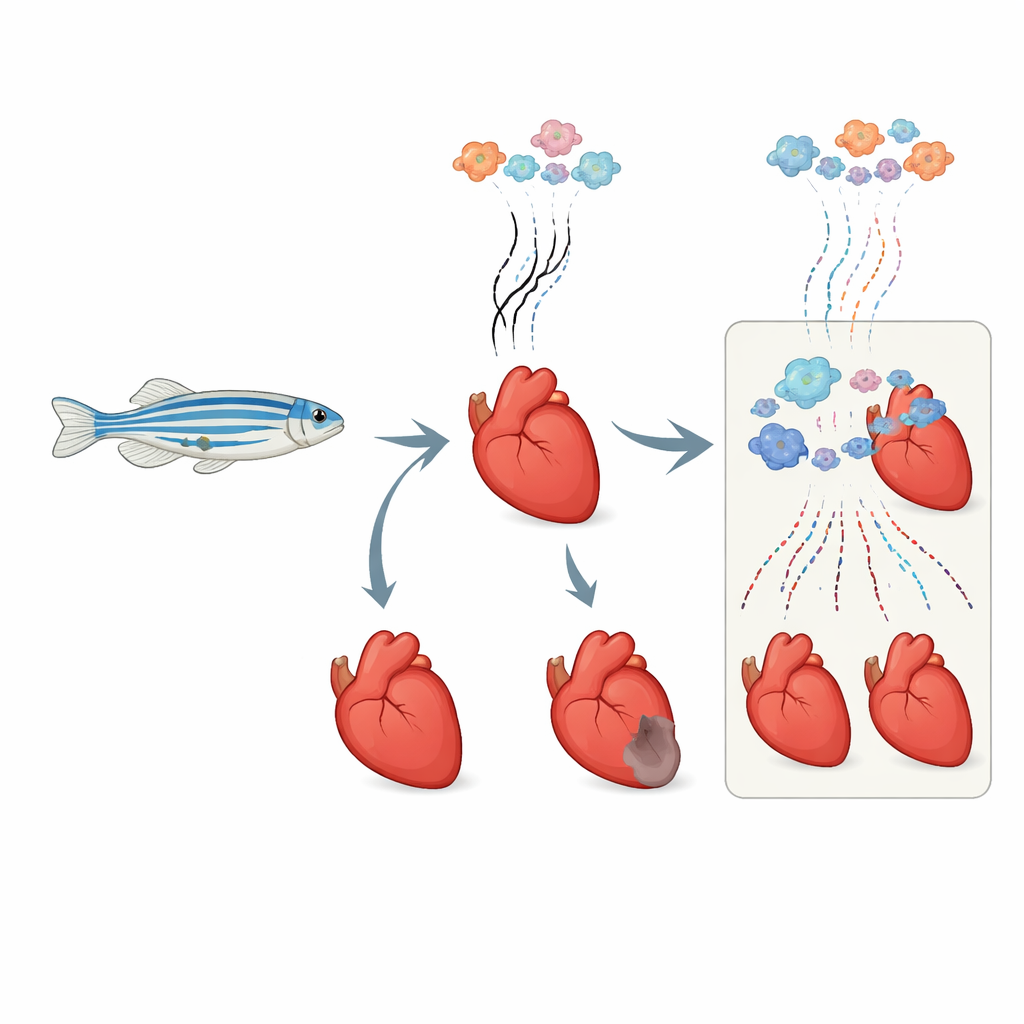
Elke cel in het hart schakelt constant genen aan en uit en produceert kortlevende RNA‑boodschappen die de cel instrueren wat te doen. Traditionele methoden lezen alle RNA in bulk uit, waardoor oude en nieuwe signalen vermengd raken. De onderzoekers pasten een chemische “tijdstempel”-methode, RNA‑metabole labeling, aan voor gebruik in levende volwassen zebravissen. Ze injecteerden een onschadelijk bouwblok dat alleen in nieuwgemaakt RNA wordt opgenomen. Later zorgt een specifieke chemische behandeling ervoor dat die nieuwe stukken een herkenbare signatuur krijgen bij sequencing van het RNA. Door dit te combineren met enkelcelsanalyse konden ze in elke individuele hartcel onderscheiden welke genboodschappen er al voor de verwonding waren en welke pas daarna vers waren gemaakt.
Inzoomen op de eerste uren na beschadiging
Het team concentreerde zich op de cruciale eerste zes uur nadat een deel van het zebravishart werd bevroren en beschadigd, een procedure die een hartaanval nabootst. Omdat veel langlevende RNA‑moleculen al vóór de beschadiging aanwezig waren, zouden alleen totaalmetingen van RNA vroege veranderingen vervagen. Met hun labelingsmethode vergeleken de onderzoekers het nieuwgemaakte RNA in beschadigde harten met dat in sham‑geopereerde controles, per celtype. Hierdoor konden ze zelfs subtiele en kortstondige uitbarstingen van genactiviteit detecteren die anders zouden worden overstemd door oudere boodschappen of door verschillen tussen individuele dieren.
Vroege immuuncellen treden op de voorgrond
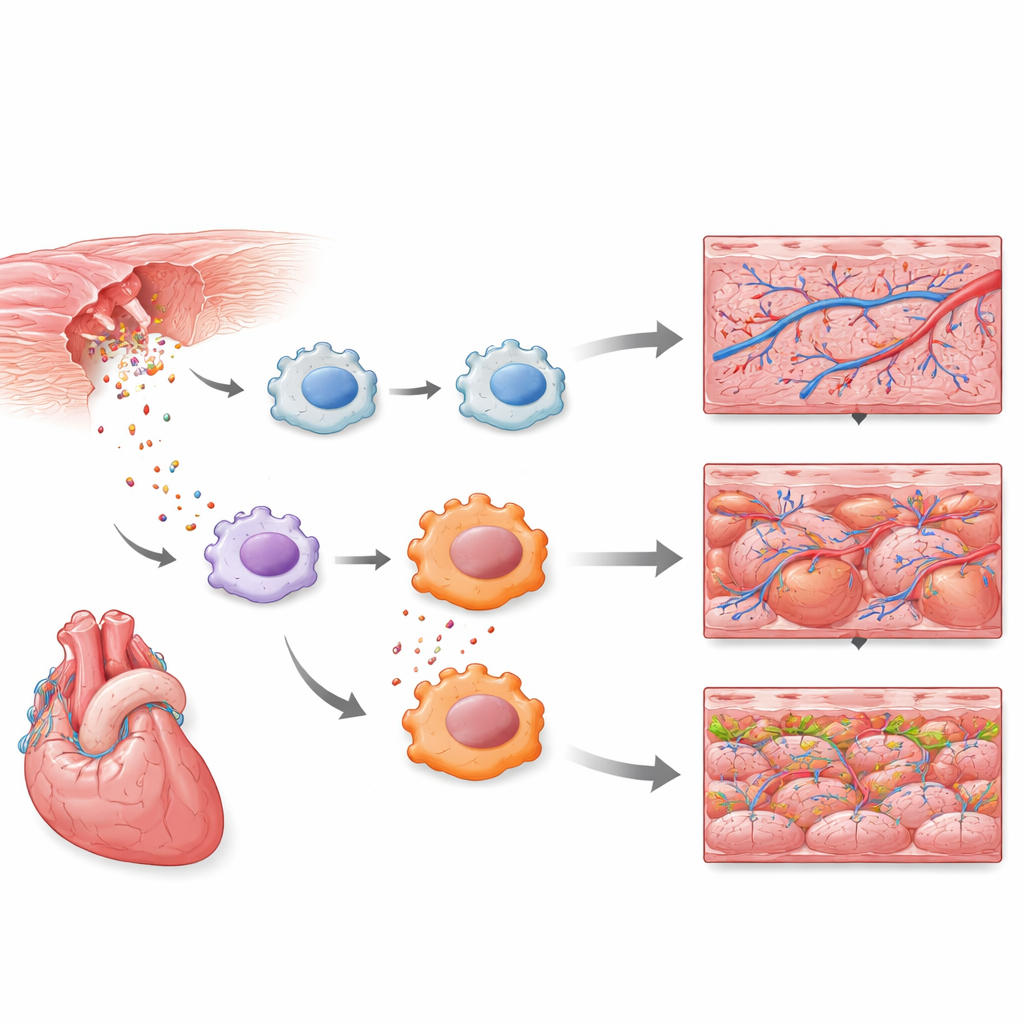
De enkelcelmetingen toonden dat een subset van immuuncellen die leek op macrofagen tot de allereerste responders behoorde. Binnen enkele uren zetten deze cellen innaten verdedigingsprogramma’s aan, waaronder Toll‑like receptor‑signalering, een bekend alarmsysteem dat gevaar en infectie detecteert. Een groter referentieoverzicht van hartcellen gedurende meerdere dagen van regeneratie bevestigde dat neutrofielen, een ander type witte bloedcel, ook een sterke vroege respons laten zien. Gezamenlijk laten deze resultaten zien dat de eerste golf van hartherstel niet alleen wordt aangedreven door structurele cellen zoals spier- en bloedvatcellen, maar door een nauw getimede ontstekingsuitbarsting in specifieke immuunceltypen.
Inflammatie bijstellen om herstel te bevorderen
Ontsteking is een tweesnijdend zwaard: te weinig vertraagt het opruimen van dood weefsel, terwijl te veel of te langdurig extra schade en littekenvorming kan veroorzaken. Geleid door hun enkelcelgegevens testten de onderzoekers wat er gebeurt als ze één belangrijk immuunsignaal in macrofagen selectief afzwakken. Ze creëerden zebravissen waarin een dominant-negatieve versie van MyD88 — een essentiële schakel in Toll‑like receptorpaden — alleen in macrofagen kon worden ingeschakeld na behandeling. Toen deze rem werd geactiveerd, stapelden zich minder sterk ontstekingsbevorderende macrofagen op op de plaats van de verwonding. Opvallend was dat beschadigde harten in deze vissen snellere vroege kenmerken van regeneratie lieten zien: meer groei van kransslagvaten rond de wond en verhoogde celdeling van hartspiercellen, zonder duidelijke nadelige effecten op andere stappen van het herstel.
Wat dit betekent voor toekomstig hartherstel
Dit werk laat zien dat het nu mogelijk is om binnen enkele uren en op enkelcelresolutie te zien welke genen reageren op hartschade in een levend dier. De bevindingen benadrukken dat vroege activatie van de aangeboren immuuncellen geen simpele aan‑of‑uit‑gebeurtenis is, maar een instelbaar proces waarvan sterkte en timing regeneratie kunnen versnellen of vertragen. Hoewel zebravisharten veel regeneratiever zijn dan menselijke harten, zou het principe overdraagbaar kunnen zijn: het zorgvuldig bijstellen van specifieke immuunsignalen — in plaats van ontsteking volledig te blokkeren — zou op termijn kunnen helpen beschadigde zoogdierharten naar beter herstel te leiden.
Bronvermelding: Mintcheva, J., Tseng, TL., Goumenaki, P. et al. In vivo single-cell RNA metabolic labeling resolves early transcriptional responders in the regenerating zebrafish heart. Nat Commun 17, 4073 (2026). https://doi.org/10.1038/s41467-026-72781-2
Trefwoorden: hartregeneratie, zebravis, enkelcel RNA, immuunrespons, Toll‑like receptor signalering