Clear Sky Science · pl
Oznaczanie metaboliczne RNA in vivo w pojedynczych komórkach ujawnia wczesne odpowiedzi transkrypcyjne w regenerującym się sercu zebrafisha
Dlaczego naprawa uszkodzonego serca jest tak trudna
Kiedy u człowieka dochodzi do zawału, uszkodzony mięsień zazwyczaj zastępowany jest tkanką bliznowatą, która nie kurczy się, co pozostawia serce trwale osłabione. Tymczasem niektóre zwierzęta, jak zebrafish, potrafią odrosnąć zdrową tkankę sercową po urazie. Artykuł ten opisuje, jak naukowcy zaczynają obserwować, w czasie rzeczywistym i komórka po komórce, pierwsze przełączniki genetyczne, które się włączają w sercu zebrafisha po uszkodzeniu — oraz jak modulacja wczesnej reakcji immunologicznej może zmienić przebieg gojenia.
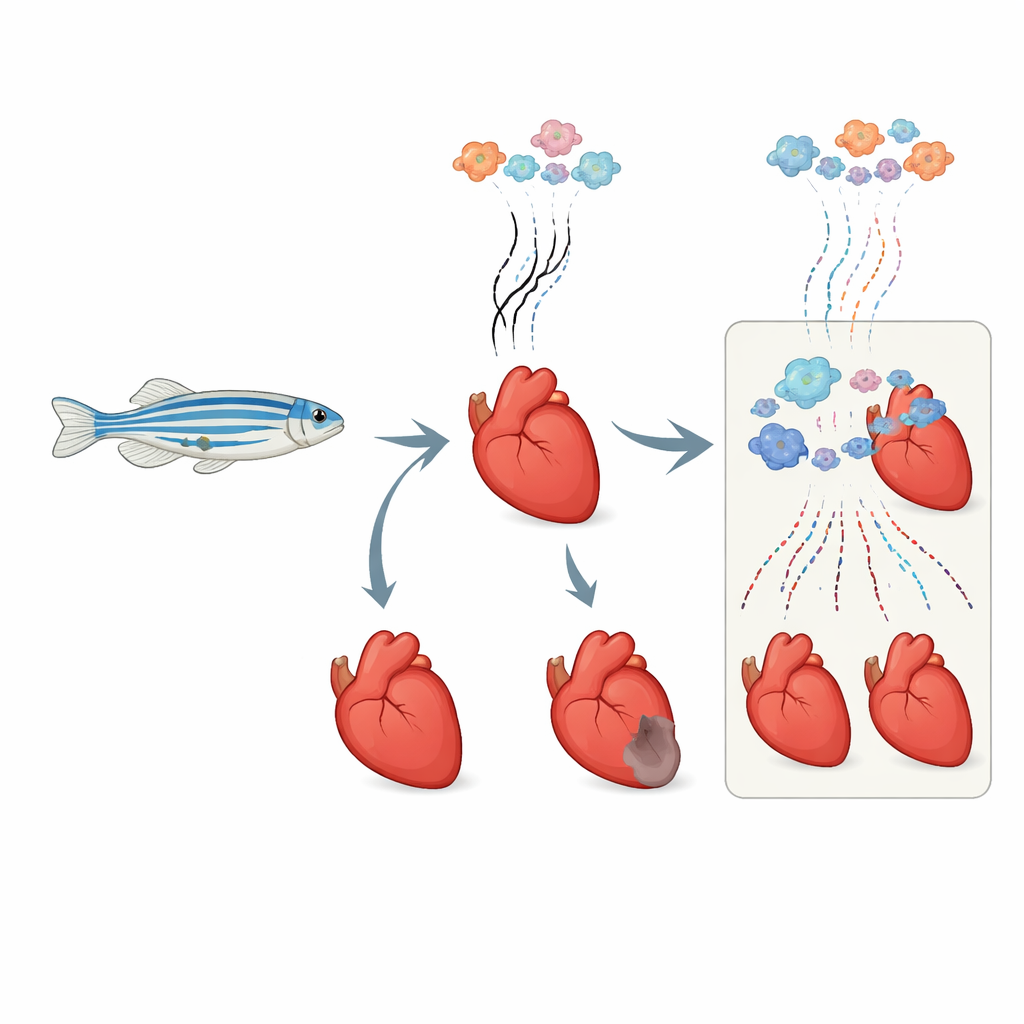
Obserwowanie świeżych komunikatów genetycznych w chwili ich pojawiania się
Każda komórka w sercu nieustannie włącza i wyłącza geny, produkując krótkotrwałe komunikaty RNA, które mówią komórce, co robić. Tradycyjne metody odczytują całe RNA w masie, mieszając sygnały stare i nowe. Badacze zaadaptowali chemiczną metodę „znacznikowania czasowego”, zwaną metabolicznym znakowaniem RNA, do użycia u żywych dorosłych zebrafish. Wstrzyknęli nieszkodliwy element budulcowy, który włącza się tylko do nowo powstałego RNA. Później specyficzne traktowanie chemiczne przekształca te nowe fragmenty w formę, która ujawnia się jako odrębne signature podczas sekwencjonowania RNA. Łącząc to z analizą pojedynczych komórek, mogli rozdzielić, w każdej pojedynczej komórce serca, które komunikaty genowe były obecne przed urazem, a które powstały świeżo po.
Przybliżenie się do pierwszych godzin po uszkodzeniu
Zespół skupił się na kluczowych pierwszych sześciu godzinach po zamrożeniu i uszkodzeniu części serca zebrafisha, procedurze naśladującej zawał. Ponieważ wiele długowiecznych cząsteczek RNA było już obecnych przed urazem, samo mierzenie całkowitego RNA zacierałoby wczesne zmiany. Dzięki podejściu znakowania naukowcy porównali nowo powstałe RNA w sercach po urazie z kontrolami operacyjnymi, typ komórki po typie komórki. Pozwoliło im to wykryć nawet subtelne i krótkotrwałe wybuchy aktywności genów, które inaczej zostałyby zagłuszone przez starsze komunikaty lub różnice między poszczególnymi osobnikami.
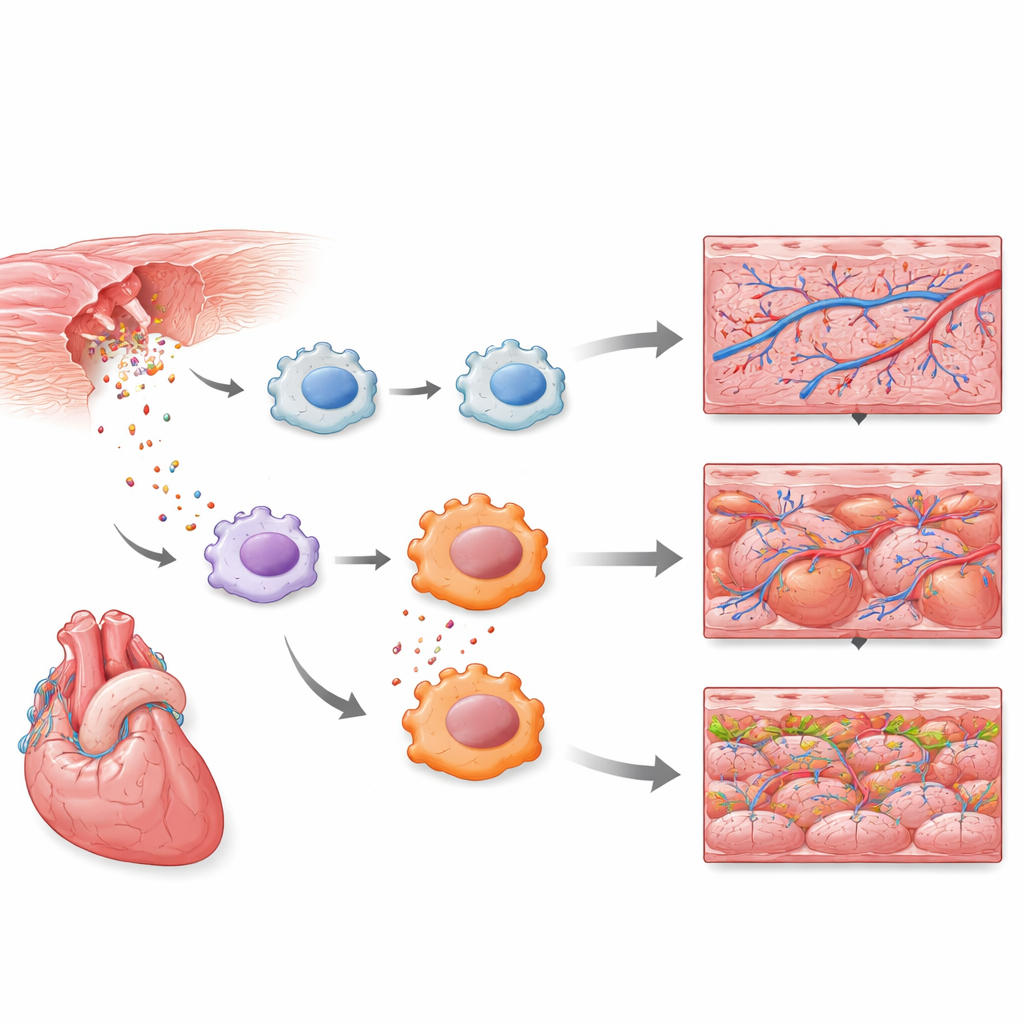
Wczesne komórki odpornościowe wchodzą na scenę
Pomiary pojedynczych komórek ujawniły, że podzbiór komórek odpornościowych przypominających makrofagi był jednymi z najwcześniejszych responderów. W ciągu kilku godzin te komórki uruchomiły programy obronne wrodzonej odporności, w tym sygnalizację receptorów Toll-podobnych — dobrze znany szlak alarmowy wyczuwający zagrożenie i infekcję. Większa mapa referencyjna komórek serca obejmująca wiele dni regeneracji potwierdziła, że neutrofile, inny rodzaj białych krwinek, również wykazują silną wczesną odpowiedź. Razem wyniki te pokazują, że pierwsza fala naprawy serca jest napędzana nie tylko przez komórki strukturalne, takie jak mięsień i naczynia krwionośne, lecz przez precyzyjnie wyczaszowaną falę aktywności zapalnej w określonych typach komórek odpornościowych.
Dostrajanie zapalenia, by wspomóc naprawę
Zapalenie to broń obosieczna: za słabe może opóźnić oczyszczanie martwej tkanki, natomiast zbyt silne lub przedłużone może powodować dodatkowe uszkodzenia i bliznowacenie. Kierując się danymi z analizy pojedynczych komórek, badacze sprawdzili, co się stanie, jeśli selektywnie stłumią jeden kluczowy sygnał immunologiczny w makrofagach. Stworzyli zebrafishy, w których dominująca negatywna wersja MyD88 — istotnego przekaźnika w szlakach receptorów Toll-podobnych — mogła być włączona wyłącznie w makrofagach po podaniu odpowiedniego czynnika. Gdy hamulec ten został załączony, w miejscu urazu gromadziło się mniej makrofagów o silnie zapalnym profilu. Co uderzające, uszkodzone serca tych ryb wykazywały szybsze wczesne cechy regeneracji: większy wzrost naczyń wieńcowych wokół rany i zwiększoną proliferację komórek mięśnia sercowego, bez widocznych negatywnych skutków dla innych etapów gojenia.
Co to oznacza dla przyszłej naprawy serca
Praca ta pokazuje, że teraz możliwe jest obserwowanie, w ciągu godzin i z rozdzielczością pojedynczej komórki, które geny włączają się w odpowiedzi na uszkodzenie serca u żywego zwierzęcia. Wyniki podkreślają, że wczesna aktywacja komórek odpornościowych wrodzonych nie jest prostym zjawiskiem włącz/wyłącz, lecz procesem regulowanym, którego siła i czas mogą przyspieszać lub spowalniać regenerację. Choć serca zebrafisha są znacznie bardziej regeneratywne niż serca ludzkie, zasada ta może być przenoszalna: ostrożne dostosowywanie konkretnych sygnałów immunologicznych — zamiast całkowitego blokowania zapalenia — mogłoby kiedyś pomóc sprowokować lepsze odzyskiwanie funkcji u uszkodzonych ssaczych serc.
Cytowanie: Mintcheva, J., Tseng, TL., Goumenaki, P. et al. In vivo single-cell RNA metabolic labeling resolves early transcriptional responders in the regenerating zebrafish heart. Nat Commun 17, 4073 (2026). https://doi.org/10.1038/s41467-026-72781-2
Słowa kluczowe: regeneracja serca, zebrafish, RNA pojedynczych komórek, odpowiedź immunologiczna, szlak sygnalizacji receptorów Toll-podobnych