Clear Sky Science · fr
Marquage métabolique in vivo de l’ARN à l’échelle unicellulaire permet d’identifier les premiers répondeurs transcriptionnels dans le cœur de zebrafish en régénération
Pourquoi réparer un cœur abîmé est si difficile
Lorsqu’une personne fait une crise cardiaque, le muscle endommagé est généralement remplacé par du tissu cicatriciel qui ne bat pas, laissant le cœur durablement affaibli. Pourtant certains animaux, comme le zebrafish, peuvent régénérer du muscle cardiaque sain après une lésion. Cet article explore comment les scientifiques commencent à observer, en temps réel et cellule par cellule, les tout premiers interrupteurs génétiques qui s’activent dans le cœur du zebrafish après une blessure — et comment moduler une réaction immunitaire précoce peut influer sur le cours de la guérison.
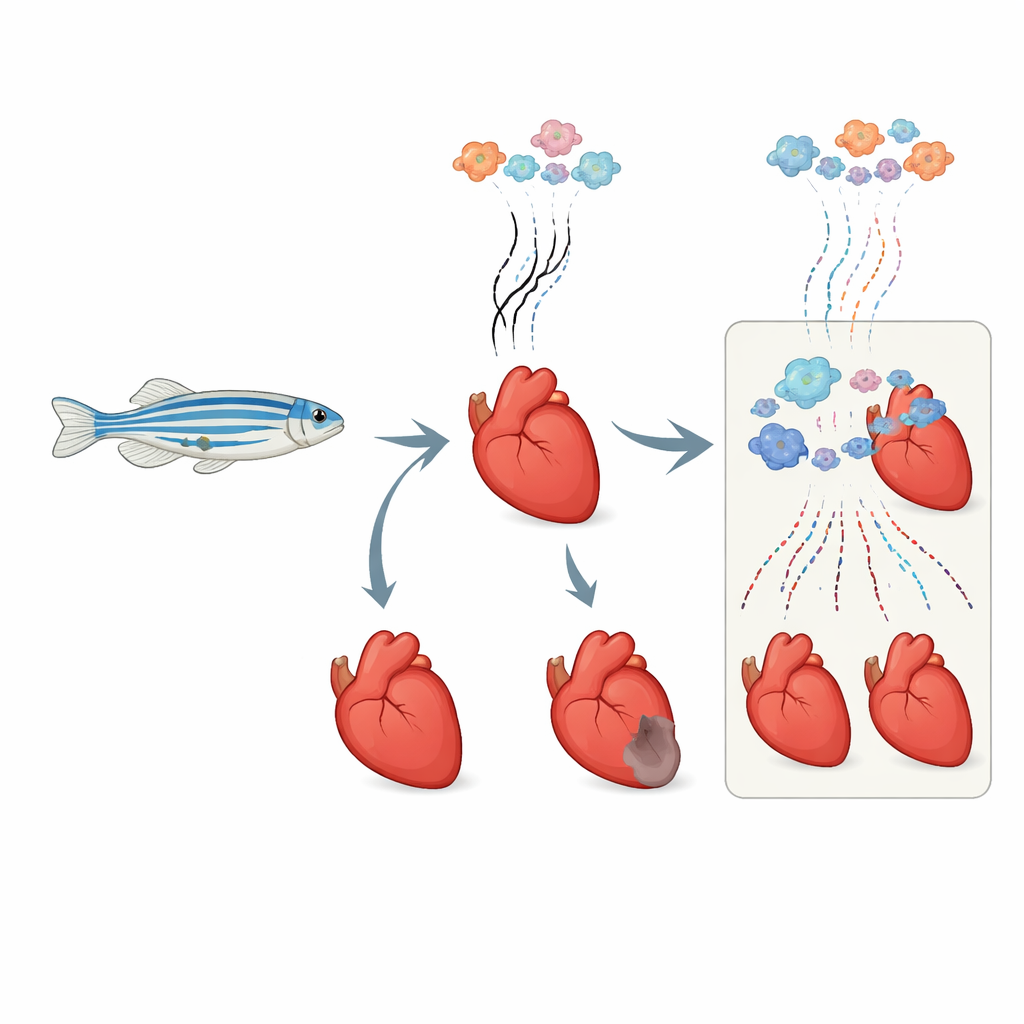
Observer les nouveaux messages génétiques dès leur apparition
Chaque cellule du cœur active et désactive constamment des gènes, produisant des messages d’ARN de courte durée qui indiquent à la cellule quoi faire. Les méthodes traditionnelles lisent tout l’ARN en vrac, mêlant signaux anciens et récents. Les chercheurs ont adapté une méthode chimique de « timestamp », appelée marquage métabolique de l’ARN, pour l’utiliser chez des zebrafish adultes vivants. Ils ont injecté un précurseur inoffensif qui s’incorpore uniquement dans l’ARN fraîchement synthétisé. Ensuite, un traitement chimique spécifique transforme ces nouvelles unités en une forme qui apparaît comme une signature distincte lors du séquençage de l’ARN. En combinant cela avec l’analyse unicellulaire, ils ont pu distinguer, dans chaque cellule cardiaque individuelle, quels messages génétiques étaient présents avant la lésion et lesquels avaient été produits ensuite.
Se concentrer sur les premières heures après la lésion
L’équipe s’est focalisée sur les six premières heures cruciales après le gel et la lésion d’une portion du cœur de zebrafish, une procédure qui imite une crise cardiaque. Parce que de nombreux ARN de longue durée étaient déjà présents avant la blessure, la simple mesure de l’ARN total aurait estompé les changements précoces. Grâce à leur approche de marquage, les scientifiques ont comparé l’ARN nouvellement synthétisé dans les cœurs lésés à celui des témoins opérés en simulation, cellule par cellule. Cela leur a permis de détecter même des poussées subtiles et transitoires d’activité génique qui auraient autrement été noyées par des messages plus anciens ou par des différences entre animaux individuels.
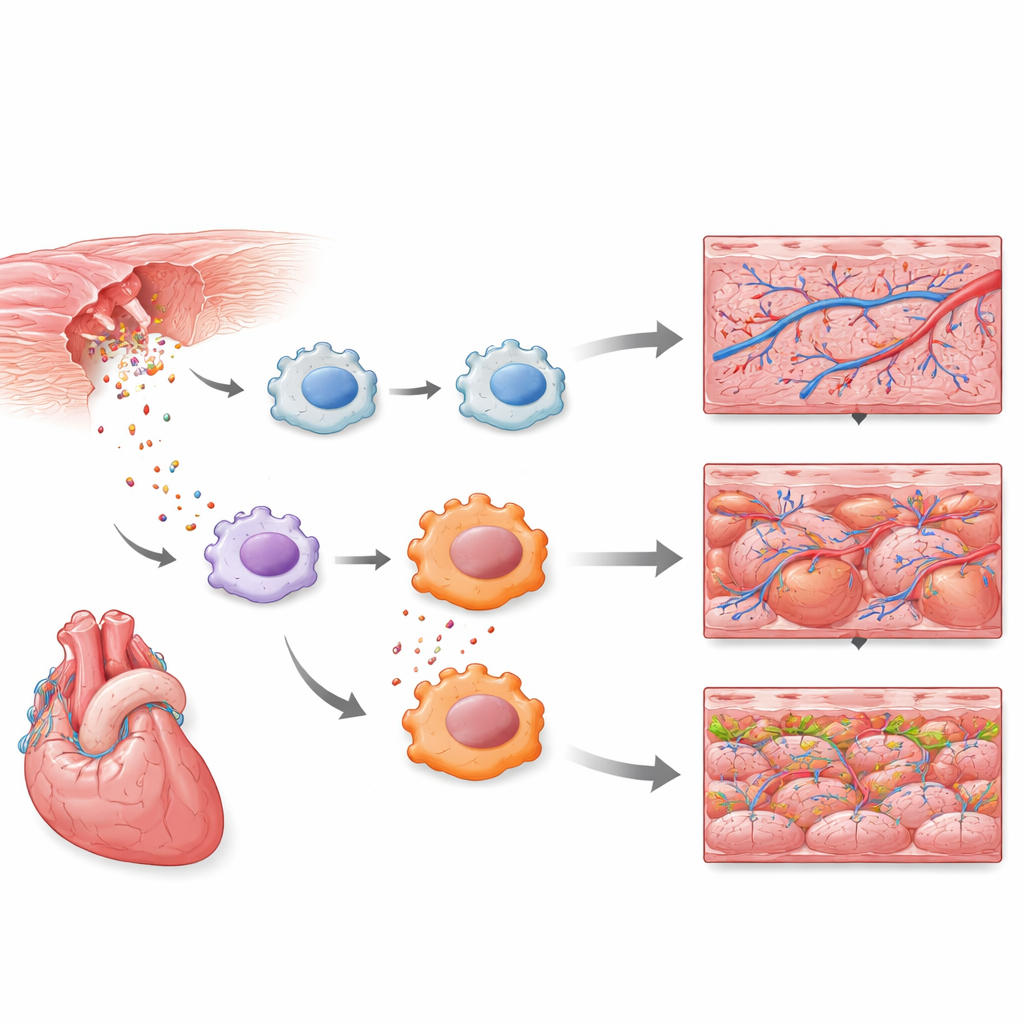
Les cellules immunitaires précoces montent sur le devant de la scène
Les mesures unicellulaires ont révélé qu’un sous-ensemble de cellules immunitaires ressemblant à des macrophages faisait partie des tout premiers répondeurs. En quelques heures, ces cellules ont activé des programmes de défense innée, y compris la signalisation via les récepteurs de type Toll, une voie d’alarme bien connue qui détecte le danger et l’infection. Une carte de référence plus large des cellules cardiaques sur plusieurs jours de régénération a confirmé que les neutrophiles, un autre type de globule blanc, déclenchent eux aussi une forte réponse précoce. Ensemble, ces résultats montrent que la première vague de réparation cardiaque n’est pas portée uniquement par des cellules structurelles comme les cellules musculaires et les vaisseaux sanguins, mais par une poussée d’activité inflammatoire précisément synchronisée dans des types cellulaires immunitaires spécifiques.
Affiner l’inflammation pour favoriser la réparation
L’inflammation est une arme à double tranchant : trop peu peut retarder l’élimination des tissus morts, tandis qu’un excès ou une inflammation prolongée peut causer des dommages supplémentaires et de la fibrose. Guidés par leurs données unicellulaires, les chercheurs ont testé ce qui se passe s’ils atténuent sélectivement un signal immunitaire clé dans les macrophages. Ils ont créé des zebrafish dans lesquels une version à effet dominant négatif de MyD88 — un relais essentiel des voies des récepteurs de type Toll — pouvait être activée uniquement dans les macrophages après traitement. Quand ce frein a été engagé, moins de macrophages fortement inflammatoires se sont accumulés au site de la lésion. Fait remarquable, les cœurs endommagés de ces poissons présentaient des signes précoces de régénération plus rapides : une plus grande croissance des vaisseaux coronaires autour de la plaie et une augmentation de la division des cellules musculaires cardiaques, sans atteinte évidente aux autres étapes de la cicatrisation.
Ce que cela implique pour la réparation cardiaque future
Ce travail montre qu’il est désormais possible d’observer, en quelques heures et avec une résolution unicellulaire, quels gènes s’activent en réponse à une lésion cardiaque chez un animal vivant. Les résultats soulignent que l’activation précoce des cellules immunitaires innées n’est pas simplement un phénomène binaire, mais un processus modulable dont l’intensité et le timing peuvent accélérer ou ralentir la régénération. Bien que le cœur du zebrafish soit bien plus régénératif que le cœur humain, le principe pourrait être transposable : ajuster finement des signaux immunitaires spécifiques — plutôt que d’éliminer l’inflammation — pourrait un jour aider à orienter les cœurs de mammifères blessés vers une meilleure récupération.
Citation: Mintcheva, J., Tseng, TL., Goumenaki, P. et al. In vivo single-cell RNA metabolic labeling resolves early transcriptional responders in the regenerating zebrafish heart. Nat Commun 17, 4073 (2026). https://doi.org/10.1038/s41467-026-72781-2
Mots-clés: régénération cardiaque, zebrafish, ARN unicellulaire, réponse immunitaire, signalisation des récepteurs de type Toll