Clear Sky Science · de
In vivo-Einzelzell-RNA-Stoffwechselmarkierung klärt frühe transkriptionelle Reaktionen im regenerierenden Zebrafischenherzen auf
Warum es so schwer ist, ein gebrochenes Herz zu reparieren
Wenn ein Mensch einen Herzinfarkt erleidet, wird das geschädigte Muskelgewebe meist durch Narbengewebe ersetzt, das nicht schlägt, wodurch das Herz dauerhaft geschwächt bleibt. Einige Tiere, etwa Zebrafische, können jedoch nach einer Verletzung gesundes Herzmuskelgewebe nachwachsen lassen. Dieser Artikel beleuchtet, wie Forschende beginnen, in Echtzeit und Zelle für Zelle die allerersten genetischen Schalter zu beobachten, die sich in einem Zebrafischherzen nach einer Schädigung umlegen — und wie das Anpassen einer frühen Immunreaktion den Verlauf der Heilung beeinflussen kann.
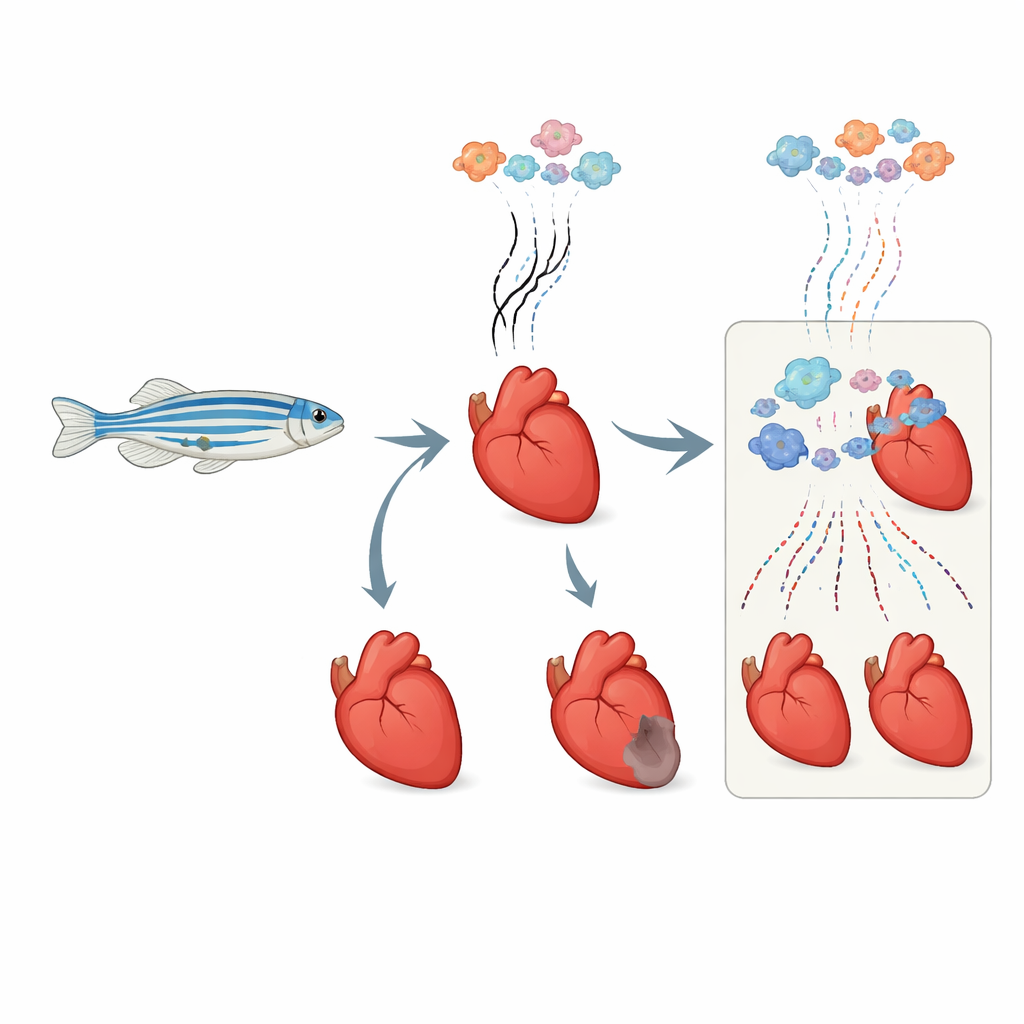
Frische genetische Botschaften beim Auftauchen beobachten
Jede Zelle im Herzen schaltet ständig Gene an und aus und produziert kurzlebige RNA-Botschaften, die der Zelle sagen, was zu tun ist. Traditionelle Methoden lesen die gesamte RNA im Bulk aus und vermischen damit alte und neue Signale. Die Forschenden adaptierten eine chemische „Zeitstempel“-Methode, genannt RNA-Stoffwechselmarkierung, für den Einsatz in lebenden erwachsenen Zebrafischen. Sie injizierten einen harmlosen Baustein, der nur in neu gebildete RNA eingebaut wird. Später verwandelt eine spezifische chemische Behandlung diese neuen Bausteine in eine Form, die beim RNA-Sequenzieren als charakteristische Signatur sichtbar wird. In Kombination mit Einzelzellanalysen konnten sie so in jeder einzelnen Herz-Zelle trennen, welche Genbotschaften vor der Verletzung vorhanden waren und welche danach frisch hergestellt wurden.
Hineinzoomen in die ersten Stunden nach der Schädigung
Das Team konzentrierte sich auf die entscheidenden ersten sechs Stunden nach dem Einfrieren und Beschädigen eines Herzabschnitts des Zebrafischs, einem Verfahren, das einen Herzinfarkt nachahmt. Da viele langlebige RNA-Moleküle bereits vor der Verletzung vorhanden waren, würden reine Messungen der Gesamt-RNA frühe Veränderungen verwischen. Mit ihrer Markierungsmethode verglichen die Forschenden neu gebildete RNA in verletzten Herzen mit der in Schein-operierten Kontrollen, Zelltyp für Zelltyp. Das erlaubte ihnen, selbst subtile und kurzlebige Schübe von Genaktivität zu entdecken, die sonst durch ältere Botschaften oder Unterschiede zwischen einzelnen Tieren überlagert würden.
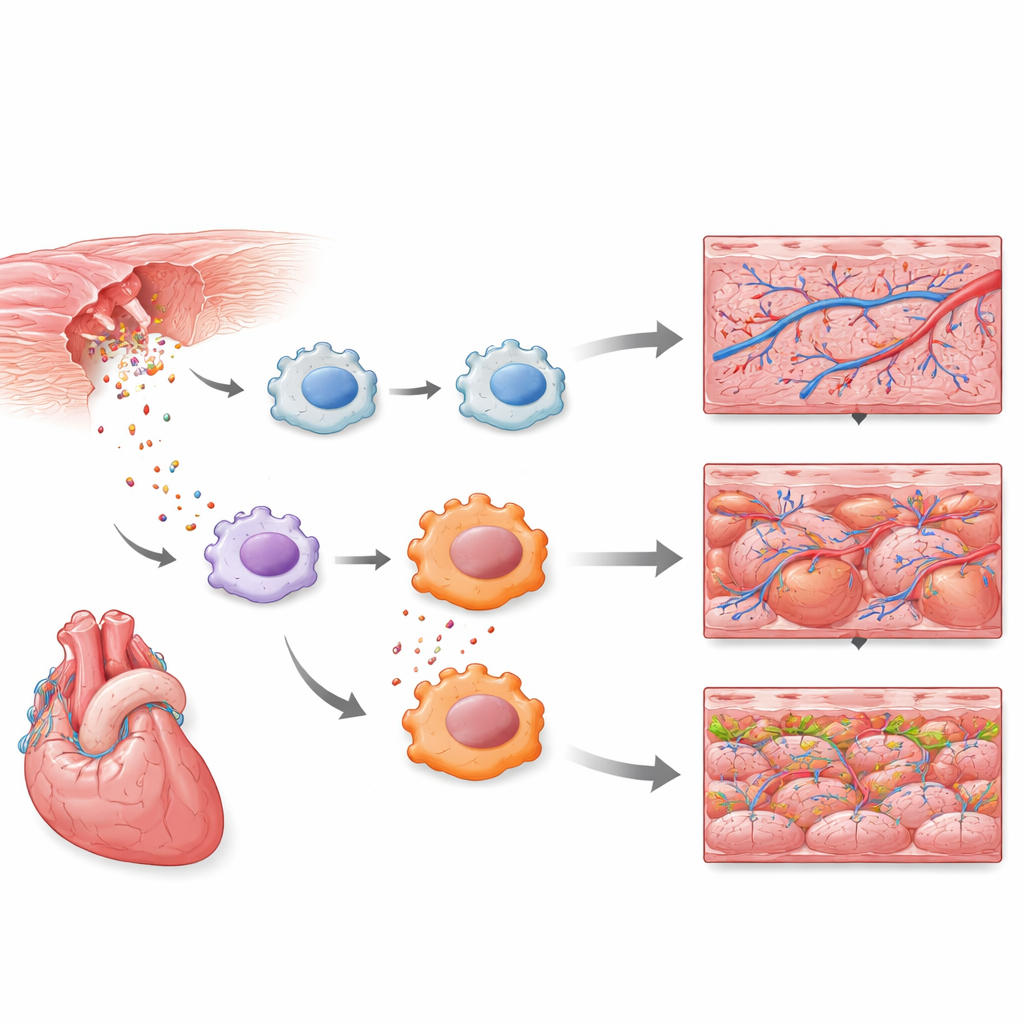
Frühe Immunzellen treten ins Rampenlicht
Die Einzelzellmessungen zeigten, dass eine Untergruppe von Immunzellen, die Makrophagen ähneln, zu den allerersten Reagierenden gehörte. Innerhalb weniger Stunden schalteten diese Zellen angeborene Abwehrprogramme an, darunter die Toll-like-Rezeptor-Signalgebung, einen bekannten Alarmweg, der Gefahr und Infektion erkennt. Eine größere Referenzkarte der Herz-Zellen über viele Tage der Regeneration bestätigte, dass auch Neutrophile, eine andere Art weißer Blutkörperchen, eine starke frühe Reaktion zeigen. Zusammengenommen zeigen diese Ergebnisse, dass die erste Welle der Herzreparatur nicht nur von strukturellen Zellen wie Muskel- und Blutgefäßzellen getragen wird, sondern von einem zeitlich präzise abgestimmten Ausbruch entzündlicher Aktivität in spezifischen Immunzelltypen.
Feinabstimmung der Entzündung zur Unterstützung der Reparatur
Entzündung ist ein zweischneidiges Schwert: Zu wenig davon kann die Beseitigung toter Gewebe verzögern, während zu viel oder zu langanhaltend zusätzlichen Schaden und Vernarbung verursachen kann. Geleitet von ihren Einzelzelldaten prüften die Forschenden, was passiert, wenn sie ein zentrales Immunsignal in Makrophagen selektiv dämpfen. Sie erzeugten Zebrafische, in denen eine dominant-negative Version von MyD88 — ein wichtiger Vermittler in Toll-like-Rezeptor-Wege — nur nach Behandlung in Makrophagen eingeschaltet werden konnte. Als diese Bremse aktiviert wurde, sammelten sich weniger stark entzündliche Makrophagen an der Verletzungsstelle an. Bemerkenswerterweise zeigten die beschädigten Herzen dieser Tiere schnellere frühe Anzeichen der Regeneration: stärkere Auswüchse der Herzkranzgefäße um die Wunde und vermehrte Teilung von Herzmuskelzellen, ohne offensichtliche Schäden an anderen Heilungsschritten.
Was das für die zukünftige Herzreparatur bedeutet
Diese Arbeit zeigt, dass es jetzt möglich ist, innerhalb von Stunden und mit Einzelzellauflösung zu beobachten, welche Gene als Reaktion auf Herzschädigung in einem lebenden Tier aktiviert werden. Die Ergebnisse heben hervor, dass die frühe Aktivierung angeborener Immunzellen kein einfaches An-oder-Aus ist, sondern ein einstellbarer Prozess, dessen Stärke und Timing die Regeneration beschleunigen oder verlangsamen können. Auch wenn Zebrafischherzen weitaus regenerationsfähiger sind als menschliche Herzen, könnte das Prinzip übertragbar sein: Das gezielte Anpassen spezifischer Immunsignale — statt die Entzündung pauschal zu blockieren — könnte eines Tages helfen, verletzte Säugetierherzen zu einer besseren Erholung zu bewegen.
Zitation: Mintcheva, J., Tseng, TL., Goumenaki, P. et al. In vivo single-cell RNA metabolic labeling resolves early transcriptional responders in the regenerating zebrafish heart. Nat Commun 17, 4073 (2026). https://doi.org/10.1038/s41467-026-72781-2
Schlüsselwörter: Herzregeneration, Zebrafisch, Einzelzell-RNA, Immunantwort, Toll-like-Rezeptor-Signalgebung