Clear Sky Science · zh
一种组织内在机制使HIV-1颗粒对TLR触发的先天免疫反应更敏感
我们的组织如何悄然抵抗HIV
HIV通常因其如何削弱免疫系统而成为新闻焦点,但这项研究颠倒了叙事:它探问我们的组织本身会做些什么来反击。在淋巴结和其他器官深处,免疫细胞和病毒在由胶原等蛋白构成的三维网状结构中移动。该研究表明,这种网状结构并非仅是被动的支架。相反,它能主动削弱HIV感染细胞的能力,同时使病毒更容易被我们的先天免疫识别。
细胞之间的隐秘世界
在我们体内,细胞被一种称为细胞外基质的复杂网络包围,主要由胶原纤维构成。研究者用不同类型的胶原制成简化的“类组织”凝胶来模拟这种环境,然后让HIV颗粒在这些三维凝胶中移动,并与保存在普通液体培养中的病毒进行比较。他们发现,短暂且物理性的与胶原纤维接触就足以显著降低病毒感染新细胞的能力——他们将这种现象称为病毒粒子感染性的细胞外限制。该效应出现迅速,依赖于与基质的直接接触,并在不同HIV株和多种富含胶原的材料中均被观察到,但在像琼脂糖这样的非粘附性凝胶中未见此现象。
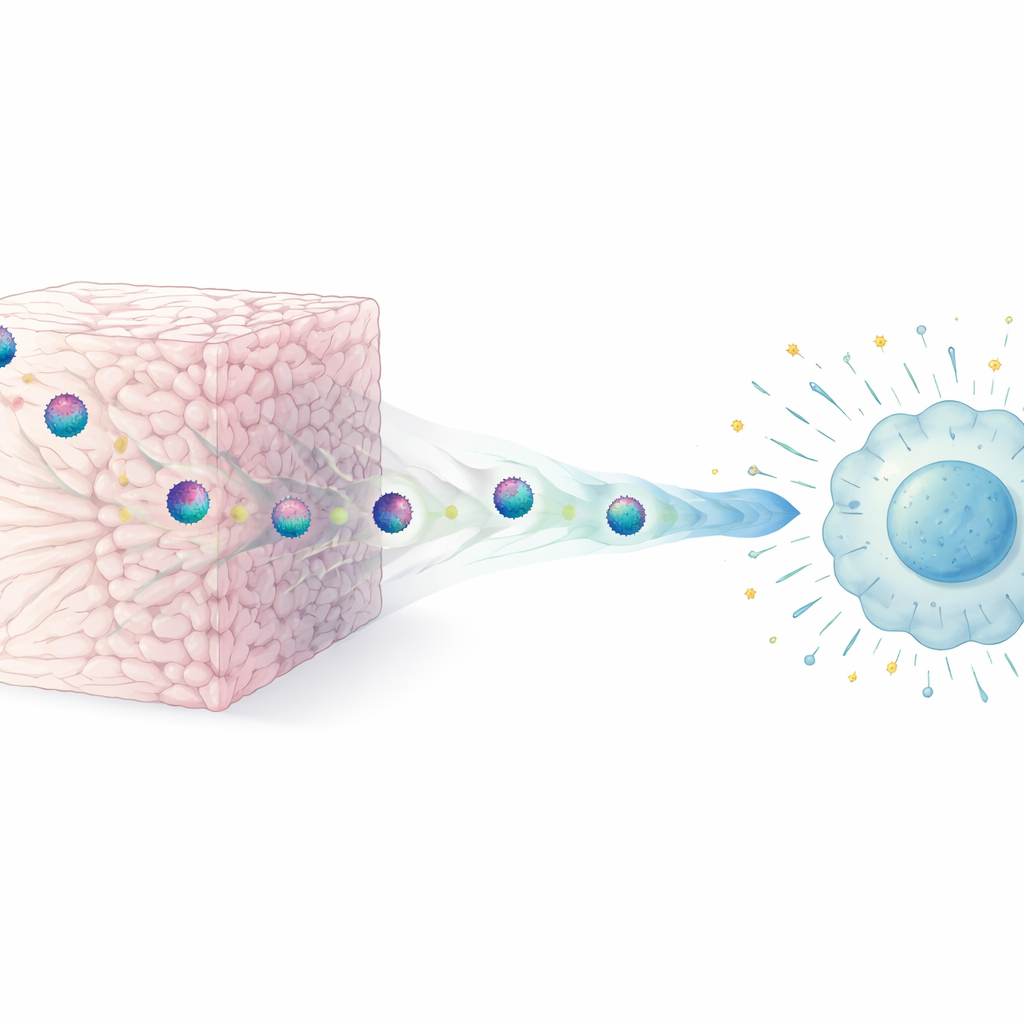
胶原如何驯服病毒
一个显而易见的担忧是胶原可能只是简单地破坏病毒颗粒。通过高分辨率电子显微镜,团队证明情况并非如此:从胶原凝胶中出来的HIV颗粒在结构上看起来正常,具有完整的膜和核心。胶原也没有剥离病毒表面蛋白。相反,关键的变化是功能性的。经胶原处理的病毒仍能与靶细胞结合,但融合效率大大降低,意味着进入细胞在非常早期的步骤就被阻断。人工的“增强感染性”纳米纤维能帮助病毒与细胞融合,这类纤维可以恢复经胶原处理的HIV的感染性,进一步支持了基质主要干扰融合过程而非整体破坏病毒的观点。
从沉默颗粒到免疫警报
最令人惊讶的发现是,胶原接触不仅削弱了感染,它还将HIV转变为对先天免疫细胞,尤其是单核来源巨噬细胞,更强的警报信号。当这些细胞暴露于经胶原处理的HIV时,产生的炎性分子(如IL-6、IL-8和TNF)远高于暴露于普通病毒时,尽管实际感染水平仅被适度降低。详细的基因表达分析显示,被胶原“预处理”病毒触发的巨噬细胞打开了广泛的抗病毒程序,包括许多已知的免疫限制因子和有助于协调更广泛免疫反应的警示信号。
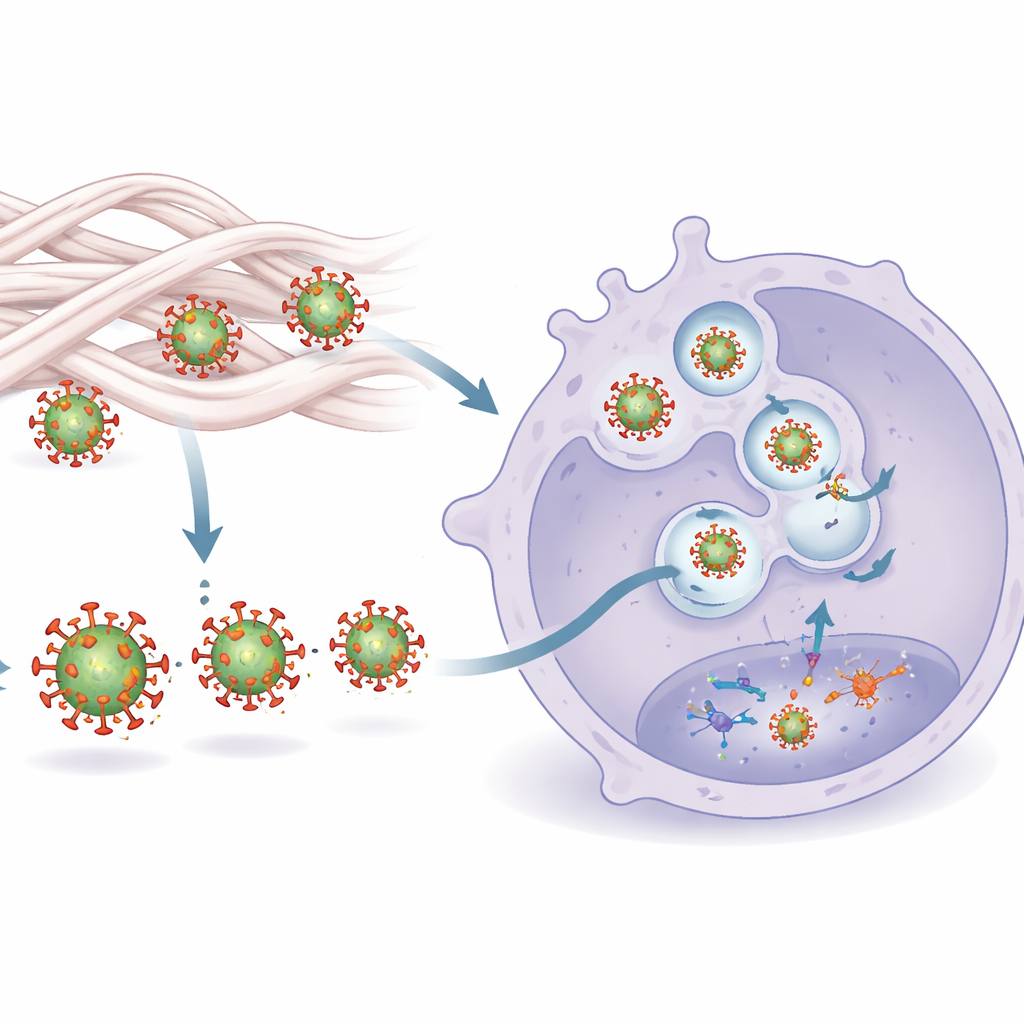
感知如何被开启
研究将这种增强的感知追溯到一个两步机制。首先,与胶原接触会微妙地重塑HIV外衣蛋白Env。这些构象变化使Env更容易被巨噬细胞表面的一个传感器,Toll样受体2(TLR2),识别。其次,一旦在表面被识别,病毒更有效地被转运到含有另一种传感器TLR8的内吞隔室,TLR8可以探测病毒的RNA基因组。阻断TLR2或TLR8中的任一者都能关闭胶原引发的细胞因子激增,表明两种信号都是必需的。显微镜观察证实,胶原处理的病毒与可溶性TLR2结合更强,并更有可能最终进入富含TLR8的内体,从而触发强烈的抗病毒级联反应。
这对HIV感染者有什么意义
对普通读者来说,核心信息是:在HIV感染过程中,我们的组织并非中立的战场。赋予器官结构的这些纤维可以直接阻碍HIV的扩散能力,并同时帮助免疫细胞更清晰地识别病毒。这种“组织内在”的防御发生在细胞之外,补充了细胞内更为人所知的抗病毒蛋白。这项工作也提示了双刃剑效应:帮助控制病毒的同样炎性信号,随着时间推移可能会导致HIV感染者常见的组织瘢痕化和慢性炎症。理解细胞外基质如何调节这种平衡,或许能开启在增强保护性免疫的同时限制长期损伤的新途径。
引用: Sid Ahmed, S., Zimmermann, L., Imle, A. et al. A tissue-intrinsic mechanism sensitizes HIV-1 particles for TLR-triggered innate immune responses. Nat Commun 17, 4209 (2026). https://doi.org/10.1038/s41467-026-72586-3
关键词: HIV 先天免疫, 细胞外基质, 胶原与病毒, Toll样受体, 组织抗病毒防御